下列有关说法正确的是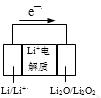
| A.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)将减小 |
B.一定温度下,反应“2HI(g)  H2(g)+I2(g) △H>0”能自发进行,则该反应△S>0 H2(g)+I2(g) △H>0”能自发进行,则该反应△S>0 |
| C.向滴有酚酞的Na2CO3溶液中滴加BaCl2溶液,红色逐渐褪去,说明BaCl2溶液显酸性 |
| D.上图电池放电时的正极反应式:2Li++Li2O2+2e—=2Li2O |
已知25 ℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,向100 mL该条件下的CaSO4饱和溶液中,加入400 mL 0.01 mol·L-1的Na2SO4溶液,针对此过程的下列叙述正确的是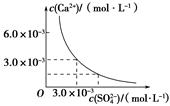
| A.溶液中无沉淀析出,但最终溶液中c(SO42-)较原来大 |
| B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42-)都变小 |
| C.溶液中析出CaSO4沉淀,溶液中c(Ca2+)、c(SO42-)都变小 |
| D.溶液中析出CaSO4沉淀,最终溶液中c(SO42-)较原来大 |
已知:25 ℃时,Ksp[Mg(OH)2] = 5.61×10-12,Ksp(MgF2)= 7.42×10-11。下列说法正确的是
| A.25 ℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大 |
| B.25 ℃时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大 |
| C.25 ℃时,Mg(OH)2固体在20 mL 0.01 mol/L氨水中的Ksp比在20 mL 0.01 mol/L NH4Cl溶液中的Ksp小 |
| D.25 ℃时,在Mg(OH)2的悬浊液加入NaF溶液后,Mg(OH)2不可能转化成为MgF2 |
下列有关电解质溶液中粒子浓度关系正确的是
| A.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 |
| B.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl-)=c(I-) |
| C.0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7):c(NH3·H2O)>c(NH4+)>c(Cl-)>c(OH-) |
| D.含等物质的量的NaHC2O4和Na2C2O4的溶液: 2c(Na+)=3[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
饱和氯水中存在平衡:①C12+H2O H++Cl—+HClO,②HClO
H++Cl—+HClO,②HClO H++ClO—,取饱和氯水分别进行下列实验,相应结论错误的是
H++ClO—,取饱和氯水分别进行下列实验,相应结论错误的是
| A.逐滴加入氨水中,所得溶液中c(H+)逐渐增大 |
| B.继续通入过量C12,①、②均向右移动,溶液pH减小 |
| C.加入CaCO3悬浊液中,CaCO3的溶解平衡向右移动 |
| D.加入一定量NaOH溶液中,所得溶液中离子浓度的关系可能为c(Cl-)+ c(ClO-)= c(Na+) |
氯化铜溶液中含有少量氯化铁杂质,若要制得纯净的氯化铜(Fe(OH)3沉淀的pH是3.7,Cu(OH)2沉淀的pH是6.0),向溶液中加入下列试剂,不能达到目的的是
| A.NaOH | B.CuO | C.Cu(OH)2 | D.Cu(OH)2CO3 |
常温时,将足量的AgCl固体分别加入同体积的下列各溶液中,溶解的AgCl最少的是
| A.1 mol·L-1的MgCl2溶液 | B.2 mol·L-1的NaCl溶液 |
| C.1.4 mol·L-1的BaCl2溶液 | D.1 mol·L-1的AlCl3溶液 |
常温下,Ksp(CaS04)=9×l0-6,常温下CaS04在水中的沉淀溶解平衡曲线如图。下列说法正确的是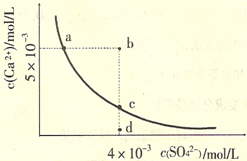
| A.常温下CaSO4饱和溶液中,c(Ca2+)、c(SO42-)对应曲线上任意一点 |
| B.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×l0-3mol/L |
| C.d点溶液通过蒸发可以变到c点 |
| D.a点对应的Ksp等于c点对应的Ksp |
下列说法正确的是
| A.NaHCO3溶液加水稀释,c(Na+)/c(HCO3-)的比值保持增大 |
| B.浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32-)+c(HCO3-)] |
| C.在高锰酸钾溶液中,H+、K+、SO42-、葡萄糖分子可以大量共存 |
| D.已知:Ksp(AgCl)=1.8×10-10, Ksp(Ag2Cr2O4)=2.0×10-12,则Ag2CrO4的溶解度小于AgCl |
下列有关说法正确的是
| A.为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解 |
| B.实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
C.N2(g)+3H2(g) 2NH3(g) ΔH<0,其他条件不变升高温度,平衡时氢气转化率增大 2NH3(g) ΔH<0,其他条件不变升高温度,平衡时氢气转化率增大 |
| D.吸热反应“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的ΔS<0 |
下列说法正确的是
| A.放热反应一定能自发的进行 |
| B.SO2能使品红溶液和溴水褪色,说明SO2具有漂白性 |
| C.将AlCl3溶液和Al2(SO4) 3溶液分别蒸干灼烧,所得产物均为Al2O3 |
D.由反应AgCl(s) +KI(aq) 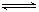 Ag I(s) + KCl (aq) 可知Ksp(AgCl)>Ksp(Ag I) Ag I(s) + KCl (aq) 可知Ksp(AgCl)>Ksp(Ag I) |
中学化学涉及多种常数,下列说法正确的是
| A.对于合成氨反应,只要温度恒定,不论化学方程式怎样书写,平衡常数不变 |
B.某温度下,2L密闭容器中加入4 mol a和2 mol b发生反应:3A(g)+2B(g) 4C(1)+2D(g),则该反应的化学平衡常数表达式为 4C(1)+2D(g),则该反应的化学平衡常数表达式为 |
| C.室温下向一定量的稀氨水中加入水稀释后,溶液中[c(H+)·c(NH3·H2O)]/ c(NH4+)不变 |
| D.难溶电解质AB2饱和溶液中,c(A2+)=xmol·L-1,c(B-)="y" mo·L-1,则Ksp值为4xy2 |
已知25℃时,Mg( OH)2的溶度积常数Ksp="5.6" ×l0-12.取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得溶液的pH=13.0,则下列说法不正确的是
| A.所得溶液中的c (H+) =10-13 mol.L-1 |
| B.所得溶液中由水电离产生的c(OH -)= 10-13 mol.L-1 |
| C.所得溶液中的c (Mg2+) =5.6×l0-10 mol.L-1 |
| D.所加烧碱溶液的pH=13.0 |
下表提供的玻璃仪器(非玻璃仪器任选)及现象描述均符合相应实脸目的的是
| 选项 |
实验目的 |
玻璃仪器 |
实验现象 |
| A |
硫化锌沉淀转化为硫化铜沉淀 |
试管、胶头滴管 |
白色沉淀转化为黑色沉淀 |
| B |
验证CO2的氧化性 |
酒精灯、集气瓶、玻璃片 |
镁条剧烈燃烧,产生白色的烟雾,瓶内壁有白色粉末 |
| C |
分离乙酸乙酯与乙酸 |
分液漏斗、烧杯 |
液体分层,上层为无色油状液体,上层液体和下层液体都从分液漏斗下口放出 |
| D |
实验室制取乙烯 |
酒精灯、圆底烧瓶、导管 |
加热后液体沸腾,液体逐渐变黑,并有气体产生 |
下列有关AgCl沉淀的溶解平衡的说法,正确的是
| A.AgCl沉淀生成和沉淀溶解不断进行,但速率相等 |
| B.AgCl难溶于水,溶液中没有Ag+和Cl- |
| C.升高温度,AgCl沉淀的溶解度不变 |
| D.向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解度不变 |