下列措施对增大反应速率明显有效的是
| A.Al在氧气中燃烧生成Al2O3,将Al粉改为Al片 |
| B.Fe与稀盐酸反应制取H2时,加入少量醋酸钠粉末 |
| C.Na与水反应时增大水的用量 |
| D.Zn与稀硫酸反应时,适当提高溶液的温度 |
把铝条放入盛有过量稀盐酸的试管中,不影响氢气产生速率的因素是
| A.盐酸的浓度 | B.铝条的表面积 | C.溶液的温度 | D.加少量Na2SO4固体 |
决定化学反应速率的主要因素是
| A.催化剂 | B.参加反应的物质本身的性质 |
| C.反应物的浓度 | D.温度、压强以及反应物的接触面 |
对于反应 A + B 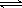 C,下列条件的改变一定能使化学反应加快的是
C,下列条件的改变一定能使化学反应加快的是
| A.升高体系的温度 | B.增加A的物质的量 |
| C.减少C的物质的量 | D.增大体系的压强 |
决定化学反应速率的主要因素是
| A.反应物的浓度 | B.反应温度 | C.使用催化剂 | D.反应物的性质 |
下列过程中,需要增大化学反应速率的是( )
| A.钢铁腐蚀 | B.食物腐败 | C.塑料老化 | D.工业合成氨 |
用铁片与2mol/L稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是
| A.滴加NaCl溶液 | B.加热 |
| C.换用4mol/L硫酸 | D.换用铁粉 |
在相同条件下,取等量H2O2做H2O2分解的对比实验,其中(1)加入MnO2催化,(2)不加MnO2催化。下图是反应放出O2的体积随时间的变化关系示意图,其中正确的是( )
用铁片与稀硫酸反应时,下列措施不能使反应速率加快的是
| A.加热 | B.不用铁片,改用铁粉 |
| C.滴加少量的CuSO4溶液 | D.不用稀硫酸,改用98%浓硫酸 |
下列措施对增大反应速率明显有效的是( )
| A.Na与水反应时增大水的用量 |
| B.Fe与稀硫酸反应制取氢气时,改用浓硫酸 |
| C.在H2SO4与Na2CO3两溶液反应时,增大压强 |
D.反应N2+3H2 2NH3恒容增加氮气 2NH3恒容增加氮气 |
下列事实能说明影响化学反应速率的决定因素是反应物本身性质的是( )
| A.Cu能与浓硝酸反应,而不能与浓盐酸反应 |
| B.Cu与浓硝酸反应比与稀硝酸反应快 |
| C.N2与O2在常温常压下不能反应,放电时可反应 |
| D.Cu与浓硫酸能反应,而与稀硫酸不反应 |
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得下图,则曲线a、b、c、d所对应的实验组别可能是
| 组别 |
c(HCl)(mol/L) |
温度(℃) |
状态 |
| 1 |
2.0 |
25 |
块状 |
| 2 |
2.5 |
30 |
块状 |
| 3 |
2. 5 |
50 |
粉末状 |
| 4 |
2.5 |
30 |
粉末状 |
A.4-3-2-1 B.1-2-3-4 C.3-4-2-1 D.1-2-4-3