某同学在用稀硫酸与锌粒(黄豆粒大小)制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有 ;
(2)硫酸铜溶液可以加快氢气生成速率的原因是 ;
(3)要加快上述实验中气体产生的速率,还可采取的措施有 、 。(例举两种措施)
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。
请完成此实验设计,其中:V1= ,V6= ,V9= ;
| 实验 混合溶液 |
A |
B |
C |
D |
E |
F |
| 4mol/LH2SO4(mL) |
40 |
V1 |
V2 |
V3 |
V4 |
V5 |
| CuSO4(mL) |
0 |
1 |
5 |
10 |
V6 |
40 |
| H2O(mL) |
V7 |
V8 |
V9 |
V10 |
15 |
0 |
该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。
但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。
下图为某化学反应的速率与时间的关系示意图。在t1 时刻升高温度或增大压强,速率的变化都符合示意图的反应是( )
| A.2SO2(g)+O2(g) ⇌2SO3(g);ΔH<0 |
| B.4NH3(g)+5O2(g) ⇌4NO(g)+6H2O(g);ΔH<0 |
| C.H2(g)+I2(g) ⇌2HI(g); ΔH>0 |
| D.C(s)+H2O(g) ⇌CO(g)+H2(g);ΔH>0 |
可逆反应mA(g)+nB(g)  pC(g)+qD(g)的v-t图象如图,如若其它条件不变,只是在反应前加入合适的催化剂,其v-t图象如图。:则
pC(g)+qD(g)的v-t图象如图,如若其它条件不变,只是在反应前加入合适的催化剂,其v-t图象如图。:则
①a1>a2②a1<a2③b1>b2④b1<b2⑤t1>t2⑥t1=t2 ⑦两图中阴影部分面积相等⑧右图中阴影部分面积更大,以上说法中正确的是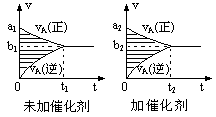
| A.②④⑤⑦ | B.①④⑥⑧ | C.②③⑤⑧ | D.①③⑥⑦ |
硫代硫酸钠(Na2S2O3)俗称大苏打,主要用于照相业作定影剂。Na2S2O3易溶于水,在酸性溶液中会迅速发生反应。
(1)完成Na2S2O3溶液与稀硫酸混合反应的化学方程式:
H2SO4+Na2S2O3= Na2SO4+H2O+ +
该反应可用于探究外界条件对反应速率的影响,完成有关的实验设计表(已知各溶液体积均为5mL):
| 实验 编号 |
T/K |
c(Na2S2O3)/mol·L-1 |
c(H2SO4) /mol·L-1 |
实验目的 |
| ① |
298 |
0.1 |
0.1 |
实验①和②探究温度对该反应速率的影响;实验①、③和④探究反应物浓度对该反应速率的影响。 |
| ② |
308 |
|
|
|
| ③ |
|
0.2 |
|
|
| ④ |
|
0.1 |
|
(2)Na2S2O3还具有很强的还原性,Na2S2O3溶液与足量氯水反应的化学方程式为______________________。(S元素被氧化为SO42-)
某密闭容器中充入等物质的量A和B,一定温度下发生反应: A(g)+xB(g)  2C (g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如图所示。下列说法正确的是
2C (g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如图所示。下列说法正确的是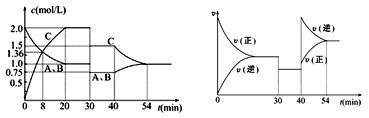
| A.30 min时降低温度,40 min时升高温度 |
| B.反应方程式中x=1,正反应为放热反应 |
| C.该反应在第8 min时达到化学平衡状态 |
| D.30~40 min间该反应使用了催化剂 |
“碘钟”实验中,3I-+S2O82-=I3-+2SO42- 的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃时进行实验,得到的数据如下表: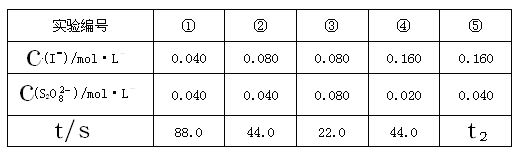
回答下列问题:
(1)该实验的目的是为了探究 因素对化学反应速率的影响。
(2)显色时间t2= 。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为 (填字母)
| A.<22.0s | B.22.0~44.0s | C.>44.0s | D.数据不足,无法判断 |
(4)通过分析比较上表数据,得到的结论是 。
如图表示反应2SO2(g)+O2(g) 2SO3(g) ΔH<0的正反应速率随时间的变化情况,试根据此曲线判断说法可能正确的是( )
2SO3(g) ΔH<0的正反应速率随时间的变化情况,试根据此曲线判断说法可能正确的是( )
| A.t1时降低温度,平衡向正反应方向移动 |
| B.t1 时减小压强,平衡向逆反应方向移动 |
| C.t1时减小SO2的浓度,增加了SO3的浓度 |
| D.t1时增加SO2和O2的浓度,平衡向正反应方向移动 |
某课外兴趣小组对双氧水(H2O2水溶液)做了如下实验探究。
(1)将质量相同但聚集状态不同的MnO2分别加入5mL 5%的双氧水中,并用带火星的木条试之。测定结果如下:
| 催化剂(MnO2) |
操作情况 |
观察结果 |
反应完成所需的时间 |
| 粉末状 |
混合不振荡 |
剧烈反应,使木条复燃 |
3.5分钟 |
| 块状 |
|
反应较慢,火星红亮但木条未复燃 |
30分钟 |
①写出H2O2反应的化学方程式 。
②实验结果说明催化剂作用的大小与 有关。
(2)取三份含有等量H2O2,但质量分数不同的双氧水,分别向其中加入1克MnO2粉末。测定结果如下:
| 双氧水体积 |
操作情况 |
反应完成所需的时间 |
收集到气体体积 |
反应后液体温度 |
| a1%的150mL |
|
11分钟 |
539mL |
24℃ |
| a2%的15mL |
混合不振荡 |
1分20秒 |
553mL |
56℃ |
| a3%的7.5mL |
|
9秒 |
562mL |
67℃ |
请简要说明:
①反应完成所需的时间不同的原因 。
②反应后液体温度不同的原因 。
③收集到气体体积不同的原因 。
(3)向含有酚酞的NaOH稀溶液中,逐滴滴入10%的双氧水,红色褪去。
①已知双氧水显弱酸性,试写出H2O2的电离方程式: 。
②小组讨论红色褪去的原因时,甲同学认为是双氧水显酸性所致;乙同学认为是双氧水有较强氧化性所致。请你设计一个简单实验来说明是甲对还是乙对。(简要文字说明)
某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
[实验原理]2KMnO4 + 5H2C2O4 + 3H2SO4 ="==" K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
[实验内容及记录]
| 实验编号 |
室温下,试管中所加试剂及其用量 / mL |
室温下溶液颜色褪至无色所需时间 / min |
|||
| 0.6 mol/L H2C2O4溶液 |
H2O |
0.2mol/L KMnO4溶液 |
3 mol/L 稀硫酸 |
||
| 1 |
3.0 |
2.0 |
3.0 |
2.0 |
4.0 |
| 2 |
3.0 |
3.0 |
2.0 |
2.0 |
5.2 |
| 3 |
3.0 |
4.0 |
1.0 |
2.0 |
6.4 |
请回答:
(1)根据上表中的实验数据,可以得到的结论是 。
(2)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率为:υ(KMnO4) = 。
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
①该小组同学提出的假设是 。
②请你帮助该小组同学完成实验方案,并填写表中空白。
| 实验编号 |
室温下,试管中所加试剂及其用量 / mL |
再向试管中加入少量固体 |
室温下溶液颜色褪至无色所需时间 / min |
|||
| 0.6 mol/L H2C2O4溶液 |
H2O |
0.2 mol/L KMnO4溶液 |
3 mol/L 稀硫酸 |
|||
| 4 |
3.0 |
2.0 |
3.0 |
2.0 |
|
t |
③若该小组同学提出的假设成立,应观察到的现象是 。
某校某班化学兴趣小组进行了下列两项试验活动:(1)探究草酸(H2C2O4)与高锰酸钾溶液在不同条件下反应的快慢;(2)测定草酸晶体的纯度。已知:① 在酸性环境下的还原产物是
在酸性环境下的还原产物是 ;②草酸是二元弱酸。
;②草酸是二元弱酸。
Ⅰ.探究草酸与高锰酸钾溶液在不同条件下反应的快慢
取4支试管,分别加入 的草酸溶液
的草酸溶液 ,按下表中四种方案分别加入相应的试剂,使其发生反应。四支试管中均可观察到有气泡产生,且溶液的颜色变化都为:紫红色→红色→橙红色→橙色→黄色→无色,溶液褪为无色所需的时间如下表所示(表中“—”表示未加入该试剂)。
,按下表中四种方案分别加入相应的试剂,使其发生反应。四支试管中均可观察到有气泡产生,且溶液的颜色变化都为:紫红色→红色→橙红色→橙色→黄色→无色,溶液褪为无色所需的时间如下表所示(表中“—”表示未加入该试剂)。
| 实验 编号 |
反应温度 (利用水浴加热) |
稀硫酸溶液 |
 固体 固体 |
  溶液 溶液 |
褪色时间 |
| 1 |
65℃ |
— |
— |
1.0mL |
100s |
| 2 |
65℃ |
10滴 |
— |
1.0mL |
90s |
| 3 |
75℃ |
10滴 |
— |
1.0mL |
40s |
| 4 |
75℃ |
10滴 |
加入少许 |
1.0mL |
3s |
根据以上4组实验,可以得出的结论主要有_______________________________。
Ⅱ.测定草酸晶体的纯度
用托盘天平称取草酸晶体 样品
样品 ;配制成
;配制成 溶液;每次移取25.00mL该溶液于锥形瓶中,用0.10mol/L酸性高锰酸钾溶液滴定;滴定实验重复操作2—3次。请回答:
溶液;每次移取25.00mL该溶液于锥形瓶中,用0.10mol/L酸性高锰酸钾溶液滴定;滴定实验重复操作2—3次。请回答:
(1)实验中需要用到的玻璃仪器除了玻璃棒、烧杯、锥形瓶、胶头滴管、250mL容量瓶外还需要的一种玻璃仪器是____________。(填仪器名称)
(2)上述 溶液与酸性
溶液与酸性 溶液反应的离子方程式为_________。
溶液反应的离子方程式为_________。
(3)若滴定过程中平均消耗酸性高锰酸钾溶液VmL,则草酸晶体的纯度为_______(以含W、V的表达式表示)。
某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3的用量为25.0 mL、大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验 编号 |
T/K |
大理石 规格 |
HNO3浓度(mol·L-1) |
实验目的 |
| ① |
298 |
粗颗粒 |
2.00 |
(Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 探究温度对该反应速率的影响; (Ⅲ)实验①和 探究大理石规格(粗、细)对该反应速率的影响;) |
| ② |
|
|
|
|
| ③ |
|
|
|
|
| ④ |
|
|
|
(2)实验①中CO2质量随时间变化的关系见下图:依据反应方程式 CaCO3+HNO3=
CaCO3+HNO3= Ca(NO3)2+
Ca(NO3)2+ CO2↑+
CO2↑+ H2O,计算实验①在70~90 s范围内HNO3的平均反应速率为 。(可用分数表示)
H2O,计算实验①在70~90 s范围内HNO3的平均反应速率为 。(可用分数表示)
(3)请在答题卡的框图中,画出实验②、③和④中CO2质量随时间变化关系的预期结果示意图。
下列说法正确的是
| A.向等体积的20%的H2O2溶液和10%的H2O2溶液中分别滴加等体积的0.1mol•L—1 FeCl3溶液和0.1 mol•L—1CuCl2溶液,前者产生气泡快,这个实验可以充分证明催化剂具有选择性 |
| B.利用水解反应可以制取某些无机化合物如TiO2、SnO2等 |
| C.将0.1 mol•L—1醋酸加水稀释,溶液中各离子浓度均减小 |
| D.室温下同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7 |
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
(1)实验一:取等物质的量浓度等体积H2O2溶液分别进行下列实验,实验报告如下表所示。
| 序号 |
条件 |
现象 |
结论 |
|
| 温度/℃ |
催化剂 |
|||
| 1 |
40 |
FeCl3溶液 |
|
|
| 2 |
20 |
FeCl3溶液 |
|
|
| 3 |
20 |
MnO2 |
|
|
| 4 |
20 |
无 |
|
|
试回答:
①实验1、2研究的是 对H2O2分解速率的影响。
②实验2、3的目的是 。
(2)实验二:经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
① 定性分析:如图甲可通过观察________________________________,定性比较得出结论。
有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是__________________________。
②定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是 。
(3)实验三:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显但不久突然褪色,反应速率明显加快。
①针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是_____的影响。
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是 。
A、硫酸钾 B、硫酸锰 C、水 D、氯化锰
“碘钟”实验中,3I-+S2O42-的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
| |
① |
② |
④ |
⑤ |
⑥ |
| c(I-)/mol·L-1 |
0.040 |
0.080 |
0.080 |
0.160 |
0.120 |
| c(S2O42-)/mol·L-1 |
0.040 |
0.040 |
0.080 |
0.020 |
0.040 |
| t /s |
88.0 |
44.0 |
22.0 |
44.0 |
t2 |
回答下列问题:(1)该实验的目的是 。
(2)显色时间t2= 。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为 (填字母)
A.<22.0s B.22.0~44.0s C.>44.0s D.数据不足,无法判断
(4)通过分析上表数据,得出的结论是