教材中用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
| 实验序号 |
A溶液 |
B溶液 |
| ① |
20 mL 0.1 mol·L-1H2C2O4溶液 |
30 mL 0.01 mol·L-1KMnO4溶液 |
| ② |
20 mL 0.2 mol·L-1 H2C2O4溶液 |
30 mL 0.01 mol·L-1KMnO4溶液 |


(1) 该实验探究的是 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是 - (填实验序号)。
(2)若实验①在2 min末收集了4.48 mL CO2(标准状况下),
则在2 min末,c(MnO4-)= mol/L。
(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定 来比较化学反应速率。
(4)小组同学发现反应速率总是如右图,其中t1~t2时间内速 率变快的主要原因可能是:①该反应放热、② 。
催化剂在生产和科技领域起到重大作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题: 
(1)定性分析:如图甲可通过观察 ,定性比较得出结论。同学X观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果,其结论________(填“合理”或“不合理”),理由是____________________________。
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是 。
(3)加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如右图所示。
①实验时放出气体的总体积是 mL。
②放出1/3气体所需时间为 min。
③计算H2O2的初始物质的量浓度_____________。 (请保留两位有效数字)
④A、B、C、D各点反应速率快慢的顺序为_____>____>____>____。
⑤ 解释④反应速率变化的原因 ___ _____。
催化剂在生产和科技领域起到重大作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
(1)定性分析:如图甲可通过观察 ,定性比较得出结论。同学乙观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果,其结论__________(填“合理”或“不合理”),理由是____________________________。
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是 。
(3)加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如下图所示。
①实验时放出气体的总体积是 mL。
②放出1/3气体所需时间为 min。
③计算H2O2的初始物质的量浓度______。(请保留两位有效数字)
④A、B、C、D各点反应速率快慢的顺序为_____>____>___> ____。
⑤解释反应速率变化的原因 。
在密闭系统中有反应C(s)+CO2(g) 2CO(g),能使反应速率加快的措施是( )
2CO(g),能使反应速率加快的措施是( )
①通过减小容器体积增大压强 ②升高温度 ③将炭粉碎
④通入CO2 ⑤增加炭的量 ⑥恒容条件下通入N2
| A.①②③⑥ | B.①②④⑥ |
| C.①②③④ | D.①②③④⑤ |
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。
(1)甲同学研究的实验报告如下表:
| 实 验 步 骤 |
现 象 |
结 论 |
| ①分别取等体积的2 mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg。 |
反应快慢: Mg>Fe>Cu |
反应物的性质越活泼,反应速率越快。 |
该同学的实验目的是研究____________对反应速率的影响;根据控制变量法,要得出正确的实验结论,还需控制的实验条件是保持______________条件相同。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用下图装置进行定量实验。完成该实验应选用的实验药品是_____________;应该测定的实验数据是________________________。
实验二:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是______________的影响。
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是______。
A、硫酸钾 B、硫酸锰 C、水 D、氯化锰
向一密闭容器中加入2mol A、0.6molC和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知t3-t4阶段为使用催化剂;图一中t0-t1阶段c(B)未画出。
(1)若t1=15min,则t0-t1阶段以C浓度变化表示的反应速率为v(C)= 。
(2)t4-t5阶段改变的条件为 ,B的起始物质的量为 。
该反应方程式可表示为
各阶段平衡时对应的平衡常数如下表所示:
| t1—t2 |
t2—t3 |
t3—t4 |
t4—t5 |
t5—t6 |
| K1 |
K2 |
K3 |
K4 |
K5 |
则K1= (保留两位小数),K1、K2、K3、K4、K5之间的关系为
K1 K2 K3 K4 K5 (用“>”、“<”或“=”连接)
(3)在相同条件下,若起始时容器中加入a molA、bmolB和cmolC,要达到t1时刻同样的平衡(各物质的百分含量相同),a、b、c要满足的条件为 。
(含a,b,c的代数式表示)
一定条件下,可逆反应N2 +3H2 2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是
2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是
| A.加催化剂,V正、V逆 都发生变化,且变化的倍数相等 |
| B.加压,V正、V逆 都增大,且V正 增大的倍数大于V逆 增大的倍数 |
| C.降温,V正、V逆 都减小,且V正 减小的倍数大于V逆 减小的倍数 |
| D.增大氮气的浓度,V正、V逆 都增大,且V正 增大倍数大于V逆 增大倍数;N2 转换率减小,H2转化率增大 |
向一体积不变的密闭容器中加入2mol A、0.6mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知t3~t4阶段为使用催化剂;图一中t0~t1阶段c(B)未画出。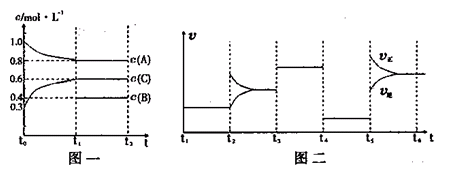
下列说法不正确的是( )
A.此温度下该反应的化学方程式2A(g)+B(g) 2C(g)
2C(g)
B.t4~t5阶段改变的条件为减小压强
C.B的起始物质的量为1.0mol
D.在相同条件下,若起始时容器中加入a mol A、bmol B和cmol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为a+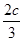 =2.4 和 b+
=2.4 和 b+ =1.2
=1.2
相同体积,相同pH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是 ( )

某探究小组利用丙酮的溴代反应(CH3COCH3+Br2 CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系。反应速率
CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系。反应速率 通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据
通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据
| 实验序号 |
初始浓度c/mol·L—1 |
溴颜色消失所需时间t/s |
|
| ① ② ③ ④ |
CH3COCH3 |
HC1 |
Br2 |
| 0.80 1.60 0.80 0.80 |
0.20 0.20 0.40 0.20 |
0.0010 0.0010 0.0010 0.0020 |
290 145 145 580 |
分析实验数据所得出的结论不正确的是( )
A.增大 增大 B.实验②和③的
增大 B.实验②和③的 相等
相等
C.增大
 增大 D.增大
增大 D.增大 ,
, 增大
增大
在2L带气压计的恒容密闭容器中通入2molX(g)和1molY(g),发生反应:
2X(g)+Y(g) 2Z(g);△H<0若达到平衡时气体总物质的量变为原来的0.85倍。请回答下列问题。
2Z(g);△H<0若达到平衡时气体总物质的量变为原来的0.85倍。请回答下列问题。
(1)平衡时Z的物质的量为___________;若反应经历5min达到平衡,则Y的平均反应速率为____________。
(2)相同条件下进行反应,在t1时刻,只改变下列某一种条件,其曲线图像如图甲。
A.升温 B.降温 C.加压 D.减压 E.加催化剂
若c=0.90mol,t1时刻改变的条件是_________(填选项编号,下同),t2_______5min (填“>”,“<”或“=”下同)。
(3)若其他条件不变,原容器为恒压容器,达到平衡后Z的物质的量______0.9mol (填“>”,“<”或“=”)。
(4)若将物质的量均为3.00mol物质X、Y混合于5L容器中发生反应,在反应过程中Z的物质的量分数随温度变化如图乙。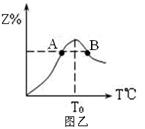
①A、B两点Z物质正反应速率的大小关系是_________;
②温度T<T0时,Z%逐渐增大的原因是______________。
某学习小组为了探究 BrO3- + 5Br- + 6H+ = 3Br2 + 3H2O 反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:
 实验编号 实验编号相关数据 |
① |
② |
③ |
④ |
⑤ |
| c(H+)/ mol · L-1 |
0.008 |
0.008 |
0.004 |
0.008 |
0.004 |
| c(BrO3-)/ mol· L-1 |
0.001 |
0.001 |
0.001 |
0.002 |
0.002 |
| c(Br-)/ mol· L-1 |
0.10 |
0.20 |
0.20 |
0.10 |
0.40 |
| v / mol· L-1· s-1 |
2.4×10-8 |
4.8×10-8 |
1.2×10-8 |
4.8×10-8 |
v1 |
下列结论不正确的是
A.若温度升高到40℃,则反应速率增大
B.实验②、④,探究的是c(BrO3-)对反应速率的影响
C.若该反应速率方程为v = k ca(BrO3-)cb(Br-)cc(H+)(k为常数),则c = 2
D.实验⑤中,v1 = 4.8×10-8 mol· L-1· s-1
已知反应:3I-(aq)+S2O82-(aq)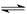 I3-(aq)+2SO42- (aq)
I3-(aq)+2SO42- (aq)
(1)写出反应的平衡常数表达式K= ;
(2)右图表示反应过程中有关物质的能量,则反应的 0(填“>”、“<”或“=”);
0(填“>”、“<”或“=”);
(Ⅰ)、(Ⅱ)两线中,使用催化剂的是 线;
(3)反应中发生反应的I-与被氧化的I-的物质的量比为 ;
(4)反应的速率可以用 与加入的淀粉溶液反应显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,记录的数据如下:
与加入的淀粉溶液反应显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,记录的数据如下:
| 实验编号 |
① |
② |
③ |
④ |
⑤ |
| c(I-)/mol·L-1 |
0.040 |
0.080 |
0.080 |
0.160 |
0.160 |
c( )/mol·L-1 )/mol·L-1 |
0.040 |
0.040 |
0.080 |
0.080 |
0.040 |
| t/s |
88 |
44 |
22 |
11 |
t1 |
则:该实验的目的是 ,显色时间t1= 分析表中数据,得出的结论是 。
用来表示可逆反应:2A(g)+B(g) 2C(g)△H<0 的正确图象是下图中的
2C(g)△H<0 的正确图象是下图中的



A B C D