可逆反应2SO2(g)+O2(g) 2SO3(g),在不同条件下测得化学反应速率最快的为
2SO3(g),在不同条件下测得化学反应速率最快的为
| A.v(O2)=3 mol·L-1·min-1 |
| B.v (SO2) =4 mol·L-1·min-1 |
| C.v (SO3) =0.1 mol·L-1·s-1 |
| D.v (O2) =0.1 mol·L-1·s-1 |
在氢气和碘蒸气反应生成碘化氢的反应中,碘化氢的生成速率与碘的减少速率之比是( )。
| A.1 :1 | B.1 :2 | C.2 :1 | D.4 :1 |
对于反应A2+3B2=2C来说,以下化学反应速率的表示中,反应速率最快的是
A.v(A2)=" 1.5" mol/ (L·s) B.v(B2)=" 4.8" mol/ (L·min)
C.v(C)=" 1.6" mol/ (L·s) D.v(B2)=" 1.7" mol/ (L·s)
在1L的密闭容器中充入1mol  和3 mol
和3 mol  ,在一定条件下反应2min后,则得
,在一定条件下反应2min后,则得 ,总质量为13.6g,如用
,总质量为13.6g,如用 的浓度变化来表示其反应速率,其反应速率为[单位:mol/(L·min)]( )
的浓度变化来表示其反应速率,其反应速率为[单位:mol/(L·min)]( )
| A.0.2 | B.0.4 | C.0.6 | D.0.8 |
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g) 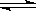 SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如右所示。由图可得出的正确结论是( )
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如右所示。由图可得出的正确结论是( )

| A.反应在c点达到平衡状态 |
| B.反应物浓度:a点小于b点 |
| C.反应物的总能量低于生成物的总能量 |
| D.Δt1=Δt2时,SO2的转化率:a~b段小于b~c段 |
在25℃时,取PH均等于2的盐酸和醋酸溶液各100ml,先分别加水稀释至2 倍体积,再分别加入过量的锌粉。下列说法正确的是( )
| A.醋酸与锌反应放出氢气多 | B.两种酸放出氢气一样多 |
| C.醋酸与锌反应速率大 | D.两种酸与锌反应的速率一样大 |
运用相关化学知识进行判断,下列结论错误的是
| A.某吸热反应能自发进行,因此该反应是熵增反应 |
| B.NH4F 水溶液中含有 HF,因此 NH4F 溶液不能存放于玻璃试剂瓶中 |
| C.可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 |
| D.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成 H2 的速率 |
使反应4NH3(g)+3O2(g)⇌2N2(g)+6H2O在2L的密闭容器中进行,半分钟后N2的物质的量增加了0.6mol.此反应的平均速率v(X)为
| A.v(NH3)="0.02" mol•L﹣1•s﹣1 | B.v(O2)="0.01" mol•L﹣1•s﹣1 |
| C.v(N2)="0.02" mol•L﹣1•s﹣1 | D.v(H2O)="0.02" mol•L﹣1•s﹣1 |
已知:4NH3+5O2=4NO+6H2O,若反应速率分别用ν(NH3)、ν(O2)、ν(NO)、ν(H2O)表示,则正确的关系是
| A.5ν(NH3)=4ν(O2) | B.5ν(O2)=6ν(H2O) |
| C.2ν(NH3)=3ν(H2O) | D.5ν(O2)=4ν(NO) |
25℃、101kPa 下:①2Na(s)+1/2O2(g)=Na2O(s) △H1=-414KJ/mol
②2Na(s)+O2(g)=Na2O2(s) △H2=-511KJ/mol
下列说法正确的是( )
| A.①和②产物的阴阳离子个数比不相等 |
| B.①和②生成等物质的量的产物,转移电子数不同 |
| C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D.25℃、101kPa下,Na2O2(s)+2Na(s)=2Na2O(s)△H=-317kJ/mol |
反应2SO2+O2 2SO3在密闭容器中进行。下列关于该反应的说法错误的是
2SO3在密闭容器中进行。下列关于该反应的说法错误的是
| A.升高温度能加快反应速率 | B.使用恰当的催化剂能加快反应速率 |
| C.增大O2的浓度能加快反应速率 | D.SO2与O2能100%转化为SO3 |
在2A+B  3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A.v(A)=0.5 mol·L-1·s-1
B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1
D.v(D)=1.6 mol·L-1·min-1
已知4NH3+5O2 4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是( )
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是( )
A. v(NH3)=v(O2) v(NH3)=v(O2) |
B. v(O2)=v(H2O) v(O2)=v(H2O) |
C. v(NH3)=v(H2O) v(NH3)=v(H2O) |
D. v(O2)=v(NO) v(O2)=v(NO) |