已知:MnO2+4HCl MnCl2+Cl2↑+2H2O,一定质量的二氧化锰溶解在100mL过量的浓盐酸中,当反应生成4.48L氯气(标况)时,剩余溶液中盐酸的浓度为1mol/L(所设反应前后体积不变),请计算:
MnCl2+Cl2↑+2H2O,一定质量的二氧化锰溶解在100mL过量的浓盐酸中,当反应生成4.48L氯气(标况)时,剩余溶液中盐酸的浓度为1mol/L(所设反应前后体积不变),请计算:
(1)反应耗用MnO2的质量;(2)被氧化的HCl物质的量;(3)跟浓盐酸的物质的量浓度。
某同学按下述操作配制100 mL 0.20 mol·L-1Na2SO4溶液,请回答有关问题。
| (1)实验步骤 |
有关问题 |
| ①计算所需Na2SO4的质量 |
需要称量Na2SO4的质量为________g |
| ②称量Na2SO4固体 |
称量需要用到的主要仪器是:托盘天平 |
| ③将Na2SO4加入100 mL烧杯中,并加入适量水 |
用玻璃棒搅拌至完全溶解,冷却至室温 |
| ④将烧杯中溶液转移至仪器A中(已检查不漏水) |
仪器A是________________; |
| ⑤洗涤烧杯,转移,定容 |
|
| ⑥摇匀、装瓶、贴上标签 |
(2)取出该Na2SO4溶液10 mL加水稀释到100 mL,稀释后溶液中Na+的物质的量浓度是__________。
(3)在实验中,以下操作对实验结果没有影响的是__________。
A.没有将洗涤液转移到容量瓶中
B.定容时仰视刻度线
C.转移前没有将使用的容量瓶烘干
D.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
(4)请写出检验溶液中的SO42-的具体操作:__________________________。
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸的物质的量浓度为__________mol·L-1。
(2)下列容量瓶的使用方法中,不正确的是____________
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(3)某学生欲用上述浓盐酸和蒸馏水配制480 mL物质的量浓度为0.200 mol·L-1的稀盐酸。
① 该学生需要用量筒量取________mL上述浓盐酸进行配制。
② 在配制过程中,下列实验操作会使所配制的稀盐酸的物质的量浓度偏大的有___________
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容。
B.用量筒量取浓盐酸时俯视观察凹液面
C.在容量瓶中定容时俯视刻度线。
D.定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线。
把500mLNH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( )
A.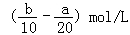 |
B.(2b﹣a)mol/L |
C.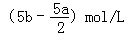 |
D.(10b﹣5a)mol/L |
NA代表阿伏加德罗常数,下列说法正确的是:( )
| A.标准状况下,22.4LSO3所含原子数为4NA |
| B.1.0L浓度为1.0 mol/L的一元酸溶液中含有NA个氢离子 |
| C.7.8g Na2O2加入过量水中,反应转移的电子数为0.2 NA |
| D.同温同压下,原子数均为NA的氢气和氦气具有不同的体积 |
在体积相同的两个密闭容器中分别充满O2、O3气体,当两个容器内温度和气体密度相等时,说法正确的是 ( )
| A.两种气体的压强相等 | B.O2比O3质量小 |
| C.两种气体的分子数目相等 | D.两种气体的氧原子数目相等 |
有某温度下KCl饱和溶液m1 g,溶质质量分数为ω1%。对其蒸发结晶或降温结晶,若析出KCl的质量、所得母液质量及溶质质量分数用m g、m2 g和ω2%表示,分析正确的是
| A.原条件下KCl的溶解度小于ω1 g | B. m1∙ω1%- m = m2∙ω2% |
| C.ω1一定大于ω2 | D. m1 - m2 ≤ m |
NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
| B.二氧化碳通过Na2O2粉末,反应后固体物质减轻 |
| C.1 mol Na2O2固体中含离子总数为4 NA |
| D.在过氧化钠与水的反应中,每生成0.1 mol氧气,转移电子的数目为0.4 NA |
焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质: NH4Cl、FeCl3、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是_________(写化学式)。
(2)写出并配平该反应的化学方程式,并标出电子转移的方向和数目:_________________;
(3)在反应:5S2O82-+2Mn2++8H2O=10SO42-+2MnO4-+16H+中,得电子的元素为__________________,5molS2O82-参加反应时转移电子物质的量为_____________。
设NA为阿伏加德罗常数的值,下列说法不正确的是
| A.物质的量浓度为1 mol/L的K2SO4溶液中,含2 mol K+ |
| B.把40 g NaOH固体溶于水得到1 L溶液,所得溶液中NaOH的物质的量浓度为1 mol·L-1 |
| C.常温常压下,71 g Cl2含有2 NA个Cl原子 |
| D.标准状况下,11.2 L N2中含有的电子数为7NA |
某同学利用Cl2氧化K2MnO4制备KMnO4的装置如图所示(夹持装置略):
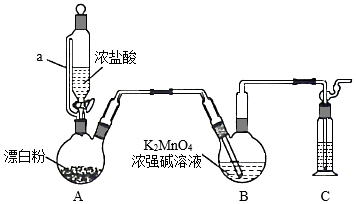
已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3MnO42﹣+2H2O═2MnO4﹣+MnO2↓+4OH﹣
回答下列问题:
(1)装置A中a的作用是 ;装置C中的试剂为 ;装置A中制备Cl2的化学方程式为 。
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是 。
(3)KMnO4常作氧化还原滴定的氧化剂,滴定时应将KMnO4溶液加入 酸式 (填“酸式”或“碱式”)滴定管中;在规格为50.00 mL的滴定管中,若KMnO4溶液起始读数为15.00 mL,此时滴定管中KMnO4溶液的实际体积为 (填标号)。
A.15.00 mL B.35.00 mL C.大于35.00 mL D.小于15.00 mL
(4)某FeC2O4•2H2O样品中可能含有的杂质为Fe2(C2O4)3、H2C2O4•2H2O,采用KMnO4滴定法测定该样品的组成,实验步骤如下:
Ⅰ.称取mg样品于锥形瓶中,加入稀H2SO4溶解,水浴加热至75℃.用c mol•L﹣1的KMnO4溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗KMnO4溶液V1mL。
Ⅱ.向上述溶液中加入适量还原剂将Fe3+完全还原为Fe2+,加入稀H2SO4酸化后,在75℃继续用KMnO4溶液滴定至溶液出现粉红色且30s内不褪色,又消耗KMnO4溶液V2 mL。
样品中所含H2C2O4•2H2O(M=126g•mol﹣1)的质量分数表达式为 。
下列关于样品组成分析的说法,正确的是 (填标号)。
A. 3时,样品中一定不含杂质
B. 越大,样品中H2C2O4•2H2O含量一定越高
C.若步骤Ⅰ中滴入KMnO4溶液不足,则测得样品中Fe元素含量偏低
D.若所用KMnO4溶液实际浓度偏低,则测得样品中Fe元素含量偏高
用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A.常温常压下,11.2 L CO和CO2混合气体中含有的碳原子数目为0.5NA |
| B.标准状况下,7.1 g氯气与足量氢氧化钠溶液反应转移的电子数为2NA |
| C.92 g NO2和N2O4的混合气体中含有的原子总数为6NA |
| D.100g 17%的氨水,溶液中含有的NH3分子数为NA |
汽车发生强烈碰撞时,安全气囊内的NaN3发生化学反应生成氯化钠(Na3N)与氮气,所产生的气体快速充满气囊,可以达到保护车内人员的目的。
(1)请写出上述反应方程式: ;它的基本反应类型是 。
(2)若安全气囊内含有195gNaN3,其物质的量为 。
(3)若195gNaN3完全分解,在标准状况下,气囊膨胀的体积约为 。
(4)28gKOH固体必须溶解在 g水中,才能使每200个水分子中有1个K+。
(5)Mg能在O2、N2、CO2中燃烧,写出镁在CO2中燃烧的化学方程式 。
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
| 成分 |
质量(g) |
摩尔质量(g ·mol-1) |
| 蔗糖 |
25.00 |
342 |
| 硫酸钾 |
0.87 |
174 |
| 阿司匹林 |
0.17 |
180 |
| 高锰酸钾 |
0.316 |
158 |
| 硝酸银 |
0.075 |
170 |
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是__________。
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)硫酸钾在水中的电离方程式为______________________。
(3)配制1L上述“鲜花保鲜剂”所需的仪器有:量筒、玻璃棒、药匙、烧杯、__________、__________、_________。(在横线上填写所缺仪器的名称),需要高锰酸钾________mol
(4)在溶液配制过程中,下列操作对配制结果没有影响的是___________。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为_______ mol/L。