若NA代表阿伏伽德罗常数的值,下列说法正确的是
| A.等物质的量的N2与O2中的所含分子数均为NA |
| B.标准状况下,5.6LCCl4含有的分子数为0.25NA |
| C.常温常压下,22CO2含有的原子数为1.5NA |
| D.1mol/LNaOH溶液中含有的Na+的数目为NA |
实验室欲用Na2CO3﹒10H2O晶体配制1mol/L的Na2CO3溶液100mL,下列说法正确的是
| A.要完成实验需称取10.6gNa2CO3﹒10H2O晶体 |
| B.本实验需用到的仪器是天平、药匙、玻璃棒、烧杯、100mL容量瓶 |
| C.定容时俯视刻度线会导致浓度偏高 |
| D.配制时若容量瓶不干燥,含有少量蒸馏水会导致浓度偏低 |
设阿伏加德罗常数为NA,则下列说法正确的是
| A.11.2L NH3中含有的氢原子数为1.5NA |
| B.0.2mol/L AlCl3溶液含有0.2NA个Al3+ |
| C.常温常压下,18g水的原子数为3NA |
| D.O2与O3的混合物32g,含有分子数为NA |
NA表示阿伏伽德罗常数的值,下列说法中正确的是
| A.常温常压下,氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24L |
| B.0.1mol/L的NaHSO4溶液中含有阳离子的物质的量为0.2mol |
| C.7.8gNa2S和7.8gNa2O2中含有的阴离子 数目均为0.1NA |
| D.1.8g18O2分子与1.8g18O3分子中含有的中子数不相同 |
右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是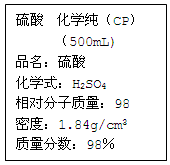
| A.该硫酸的物质的量浓度为9.2mol/L |
| B.1mol Zn与足量该硫酸反应产生2g氢气 |
| C.配制200mL 4.6mol/L的稀硫酸需取该硫酸50mL |
| D.该硫酸与等质量的水混合后所得溶液的浓度大于9.2mol/L |
下列叙述中,正确的是(NA代表阿伏加德罗常数)
| A.0.1 mol NH4+中,含有的质子数为NA |
| B.标准状况下,22.4 L水中含有的水分子数为NA |
| C.常温、常压下,22 g CO2中含有的氧原子数为NA |
| D.0.5 mol/L Na2SO4溶液中,含有的离子总数为1.5NA |
下列测定常温下1mo1氢气体积的操作中,使结果偏大的是
| A.镁带中混有与酸不反应的杂质 | B.装置接口连接处有气体泄漏 |
| C.液体量瓶刻度读数未扣去硫酸的体积 | D.硫酸注入量不足,镁带未反应完全 |
某盐的混合物中含有0.2mol/L Na+、0.4mol/L Mg2+、0.4mol/L Cl﹣,则SO42﹣为
| A.0.1 mol/L | B.0.2 mol/L | C.0.3 mol/L | D.0.4 mol/L |
用NA表示阿伏加德罗常数,下列叙述不正确的是
| A.标准状况下,22.4LSO3含有的分子数NA |
| B.常温常压下,4.4gCO2的物质的量一定为0.1mol |
| C.标准状况下,氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24L |
| D.7.8gNa2S和7.8gNa2O2中含有的阴离子数目均为0.1NA |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A.标准状况下,22.4LH2O含有的分子数NA |
| B.常温常压下,1.06gNa2CO3含有的Na+数为0.02NA |
| C.通常状况下, NA个CO2分子占有的体积为22.4L |
| D.物质的量浓度为0.5mol/L的MgCl2溶液中含有Cl-数目为NA |
水泥是重要的建筑材料。水泥熟料的主要成分为 、 ,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
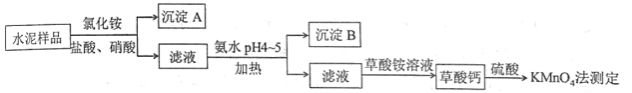
回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是__________,还可使用___________代替硝酸。
(2)沉淀A的主要成分是_________________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为____________________________________。
(3)加氨水过程中加热的目的是___________。沉淀B的主要成分为_____________、____________(写化学式)。
(4)草酸钙沉淀经稀 处理后,用 标准溶液滴定,通过测定草酸的量可间接获知钙的含 量,滴定反应为: 。实验中称取 水泥样品,滴定时消耗了 的 溶液 ,则该水泥样品中钙的质量分数为______________。
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.71g氯气中氯原子数为 NA |
| B.标准状况下,22.4 LNH3所含的电子数为10NA |
| C.5.6g Fe在足量氯气中燃烧转移的电子数为2NA |
| D.标准状况下,11.2 L H2O中含有分子的数目为0.5NA |
设NA为阿伏加德罗常数的数值.下列说法正确的是
| A.1mol甲苯含有6NA个C﹣H键 |
| B.18g H2O含有10NA个质子 |
| C.标准状况下,22.4L氨水含有NA个NH3分子 |
| D.56g铁片投入足量浓H2SO4中生成NA个SO2分子 |
掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置:
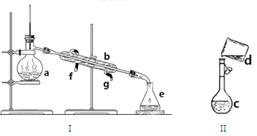
(1)写出下列仪器的名称:A. B. C.___________
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是 ,将仪器补充完整后进行实验,温度计水银球的位置在 处。冷凝水的进出方向为 。
(3)现需配制0.1mol/LNaOH溶液450mL,装置II是某同学转移溶液的示意图。
①图中的错误是 。除了图中给出的的仪器和托盘天平外,为完成实验还需的仪器有: 。
②根据计算得知,所需NaOH的质量为 g