下列说法正确的是
① 标准状况下,6.02×1023个分子所占的体积约是22.4L
②0.5molH2所占体积为11.2L
③标准状况下,1molH2O的体积为22.4L
④标准状况下,28gCO与N2的混合气体的体积约为22.4L
⑤各种气体的气体摩尔体积都约为22.4L/mol
⑥标准状况下,体积相同的气体的分子数相同
| A.①③⑤ | B.④⑥ | C.③④⑥ | D.①④⑥ |
下列说法正确的是
| A.1 mol任何气体的摩尔体积都约是22.4 L |
| B.标准状况时,体积均为22.4 L的O2与CO2含有相同的分子数 |
| C.处于标准状况的两种气体,当体积均为22.4 L时的质量完全相同 |
| D.标准状况时,2 mol任何物质的体积均约为44.8 L |
下列说法中错误的是
| A.从1 L 1mol·L-1的NaCl溶液中取出10 mL,其浓度仍是1mol·L-1 |
| B.制成0.5L 10mol·L-1的盐酸,需要氯化氢气体112L(标准状况) |
| C.0.5L 2mol·L-1 BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 |
| D.10g 98%的硫酸溶液(密度为1.84 g·cm-3)与10 mL 18.4mol·L-1的硫酸溶液的浓度不相同 |
右图是学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是

| A.该硫酸试剂的物质的量浓度为18.4 mol/L |
| B.稀释该硫酸时应把水倒入硫酸中,边倒边搅拌 |
| C.50 mL该H2SO4中加入足量的铜片并加热,被还原的H2SO4的物质的量为0.46 mol |
| D.标准状况下2.7 g Al与足量的该硫酸反应可得到H2 3.36 L |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.5.6 g Fe和足量的盐酸完全反应失去电子数为0.3 NA |
| B.64g SO2含有NA个SO2分子 |
| C.16g CH4所含的电子数为NA |
| D.标况下,4.48L的水中含有H2O分子的数目为0.2NA |
关于浓度的关系,下列说法错误的是
A.等浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-)
B.新制氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-)
C.室温下,向0.01mol/LNH4HSO4溶液中滴加NaOH溶液至中性:
c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)>c(ClO-)
D.物质的量浓度均为 的
的 和
和 混合溶液中,浓度可能的关系为:
混合溶液中,浓度可能的关系为:
c(Na+)>c(OH-)>c(HA)>c(HB)
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,11.2LSO3所含的分子数为0.5NA |
| B.12g石墨和C60的混合物中质子总数一定为6NA |
| C.25℃时,1L mol•L-1FeCl3溶液中含有0.1NA个Fe(OH)3胶体粒子 |
| D.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
在配制100mL 0.1mol/L NaCl溶液时,下列仪器不需要的是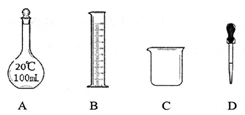
在标准状况下,进行甲、乙、丙三组实验。三组实验各取30 ml.同浓度的盐酸,加入同
一种镁、铝混合物粉末,产生气体,有关数据列表如下:

(1)甲、乙两组实验中,哪一组盐酸是不足量的? (填“甲”或“乙”)。理由是
(2)计算盐酸的物质的量浓度;(写出计算过程)
(3)求混合粉末中Mg、Al的物质的量之比?(写出计算过程)
下列各组实验中溶液最先变浑浊的是( )
| A.0.1mol/LNa2S2O3和 H2SO4 各 5mL,加水 5mL,反应温度10℃ |
| B.0.1mol/LNa2S2O3 和 H2SO4各 5mL,加水 10mL,反应温度 10℃ |
| C.0.1mol/L Na2S2O3和H2SO4各 5mL,加水 5mL,反应温度 30℃ |
| D.0.2mol/L Na2S2O3和H2SO4各 5mL,加水 10mL,反应温度 30℃ |
把3.9 g Na2O2放入100mL水中,充分反应后,计算:
(1)生成O2的体积(标准状况);
(2)反应后所得NaOH的物质的量浓度(反应前后溶液体积变化忽略不计)。
NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A.在标准状况下,分子总数为NA的H2和O2混合气体,其体积约为22.4L |
| B.5.6g铁与足量的氯气反应,转移电子数为0.2NA |
| C.11.2LH2O所含有的原子数为1.5NA |
| D.0.2mol/L的Na2CO3溶液中含有的Na+数为0.4NA |
由乙醛和丁酸、乙酸乙酯三种有机物按一定比例组成的混合物中,若含氧的质量分数为A%,则此混合物中含碳的质量分数为( )
| A.6A%/7 | B.(1-A%)/7 | C.6(1-A%)/7 | D.(100-7A/6)% |