工业上用CO和H2合成CH3OH:CO(g)+2H2(g) CH3OH(g)。反应的平衡常数如下表:
CH3OH(g)。反应的平衡常数如下表:
| 温度/℃ |
0 |
100 |
200 |
300 |
400 |
| 平衡常数 |
667 |
13 |
1.9×10-2 |
2.4×10-4 |
1×10-5 |
下列说法正确的是
A.该反应的△H> 0
B.加压、增大H2浓度和加入催化剂都能提高CO的转化率
C.工业上采用5 ×103 kPa和250℃的条件,其原因是原料气的转化率高
D.t℃时,向1 L密闭容器中投入0.1 mol CO和0.2 mol H2,平衡时CO转化率为50%,则该温度时反应的平衡常数的数值为100
在一定温度下,将等量的气体分别通入起始体积相同的密闭容器Ⅰ和Ⅱ中,使其发生反应,t0时容器Ⅰ中达到化学平衡,X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是


A.该反应的化学方程式为:3X+2Y 2Z 2Z |
| B.若两容器中均达到平衡时,两容器的体积V(Ⅰ)<V(Ⅱ),则容器Ⅱ达到平衡所需时间小于t0 |
| C.若达平衡后,对容器Ⅱ升高温度时,其体积增大,说明Z发生的反应为吸热反应 |
| D.若两容器中均达到平衡时,两容器中Z的物质的量分数相同,则Y为固态或液态 |
已知反应①:CO(g)+CuO(s)⇌CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)⇌Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)⇌CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是
A.反应①的平衡常数K1= |
B.反应③的平衡常数 |
| C.对于反应③,恒容时,温度升高,H2浓度减小,则该反应为吸热反应 |
| D.对于反应②,恒温恒容下,增大压强,H2浓度一定增大 |
已知反应2CH3OH(g) CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在2 L的密闭容器中加入a mol CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在2 L的密闭容器中加入a mol CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 |
CH3OH |
CH3OCH3 |
H2O |
| 浓度/(mol·L-1) |
0.44 |
0.6 |
0.6 |
下列说法正确的是
A.a = 1.64
B.此时刻正反应速率大于逆反应速率
C.若起始时加入2a mol CH3OH,则达到平衡时CH3OH的转化率增大
D.若混合气体的平均摩尔质量不再变化,则说明反应已达到平衡状态
现向一密闭容器中充人物质的量浓度均为0. 10 mol/L的CH4和CO2,一定条件下发生反应:CH4(g)+CO2( g)=2CO(g)+2H2 (g) △H,测得CH4的平衡转化率与温度及压强的关系如图所示。下列说法不正确的是

| A.△H>0 |
| B.1000℃,P3条件下,在Y点:v(正)<v(逆) |
| C.P4>P3>P2>Pl |
| D.1100℃,P4条件下该反应的平衡常数K="l." 64(mol/L)2 |
在恒容密闭容器中存在下列平衡:CO(g)+H2O(g) CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
A.反应CO(g)+H2O(g) CO2(g)+H2(g)的ΔH>0 CO2(g)+H2(g)的ΔH>0 |
| B.在T2时,若反应处于状态D,则一定有ν正<ν逆 |
| C.平衡状态A与C相比,平衡状态A的c(CO)小 |
| D.若T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
在一定温度下,可逆反应A(g) +3B(g) 2C(g)达到平衡的标志是
2C(g)达到平衡的标志是
A.A,B,C的分子数之比为1:3:2
B.C生成速率与A生成速率相等
C.单位时间内生成n molA同时3n mo1B
D.A,B、C的浓度不再变化
可逆反应CO(g)+H2O(g) CO2(g)+H2(g),达到平衡后,有关化学反应限度的说法正确的是
CO2(g)+H2(g),达到平衡后,有关化学反应限度的说法正确的是
| A.V正=0 | B.V逆=0 | C.V正=V逆≠0 | D.V正=V逆=0 |
一定温度下,在容积为1L的密闭容器中,存在如下关系:xH2O(g)  (H2O)x(g),反应物和生成物的物质的量随时间的变化关系如图。下列说法不正确的是
(H2O)x(g),反应物和生成物的物质的量随时间的变化关系如图。下列说法不正确的是
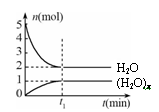
| A.x=3 |
| B.该温度下,反应的平衡常数为0.125 L2/mol2 |
| C.平衡时混合气体的平均摩尔质量是30 |
| D.t1时刻,保持温度不变,再充入1 molH2O(g), |
重新达到平衡时,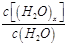
 将增大
将增大
在体积恒定的密闭容器中,一定量的SO2与1.25mol O2在催化剂作用下加热到600℃发生反应:2SO2(g)+O2(g) 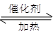 2SO3(g) △H<0。当气体的物质的量减少0.45mol时反应达到平衡,在相同的温度下测得气体压强为反应前的80%。下列有关叙述正确的是
2SO3(g) △H<0。当气体的物质的量减少0.45mol时反应达到平衡,在相同的温度下测得气体压强为反应前的80%。下列有关叙述正确的是
| A.该温度下的平衡常数为101.25 L/moL |
| B.达到平衡时,SO2的转化率是90% |
| C.降低温度,正反应速率减小程度比逆反应速率减小程度大 |
| D.将平衡混合气体通入过量BaCl2溶液中,得到沉淀的质量为231.4g |
在一个1L的密闭容器中,加入2molA和1molB,发生下述反应: 2A(g) + B(g) 3C(g) + D(s),达到平衡时,C的浓度为1.2mol/L,维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度还是1.2mol/L的是
3C(g) + D(s),达到平衡时,C的浓度为1.2mol/L,维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度还是1.2mol/L的是
| A.1mol A+0.5mol B+1.5mol C+0.1mol D |
| B.3mol C+ 0.5mol D |
| C.2mol A+1mol B+1mol D |
| D.0.5mol A+0.25mol B+2.25mol C |
下列说法不正确的是
| A.Na与H2O的反应是熵增的放热反应,该反应能自发进行 |
| B.饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同 |
| C.FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同 |
D.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s) Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 |
一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g) 2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是( )
2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是( )
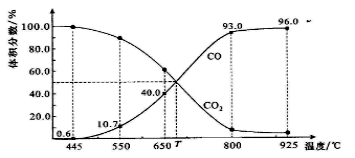
| A.550℃时,若充入惰性气体,ʋ正,ʋ逆均减小,平衡不移动 |
| B.650℃时,反应达平衡后CO2的转化率为 25.0% |
| C.T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 |
| D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数KP=24.0P总 |
已知:t ℃时,2H(g)+Y(g)  2I(g) ΔH=-196.6 kJ·mol-1,t ℃时,在一压强恒定的密闭容器中,加入4 mol H和2 mol Y反应,达到平衡后,Y剩余0.2 mol。若在上面的平衡体系中,再加入1 mol气态的I物质,t ℃时达到新的平衡,此时H物质的物质的量n(H)为( )
2I(g) ΔH=-196.6 kJ·mol-1,t ℃时,在一压强恒定的密闭容器中,加入4 mol H和2 mol Y反应,达到平衡后,Y剩余0.2 mol。若在上面的平衡体系中,再加入1 mol气态的I物质,t ℃时达到新的平衡,此时H物质的物质的量n(H)为( )
| A.0.8 mol | B.0.6 mol | C.0.5 mol | D.0.2 mol |