常温下,将0.1mol/L的醋酸溶液加水稀释,此过程中下列图像的描述不正确的是
向20 mL NaOH溶液中逐滴加入0.1 mol/L醋酸溶液,滴定曲线如右图所示。下列判断正确的是()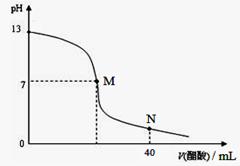
| A.在M点,两者恰好反应完全 |
| B.滴定前,酸中c(H+) 等于碱中c(OH-) |
| C.NaOH溶液的物质的量浓度为0.1 mol/L |
| D.在N点,c(CH3COO-)>c(Na+)>c(H+)>c(CH3COOH) |
某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,溶液pH随体积变化的曲线如图所示。据图判断下列说法正确的是 (  )
)
| A.Ⅱ为盐酸稀释时的pH变化曲线 |
| B.b点溶液的导电性比c点溶液的导电性强 |
C.a点K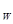 的数值比c点K 的数值比c点K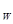 的数值大 的数值大 |
| D.b点酸的总浓度大于a点酸的总浓度 |
金属镁和0.1mol·L-1的HCl反应制取氢气,反应速率过快不易收集。为了减缓反应速率,又不减少产生氢气的量,加入下列试剂不能达到上述要求的是
| A.硫酸钠溶液 | B.醋酸钠固体 |
| C.碳酸钠固体 | D.水 |
关于浓度均为0.1 mol·L-1的三种溶液:①CH3COOH、②NaOH、③CH3COONa溶液,下列说法不正确的是
| A.c(CH3COO-):③>① |
| B.水电离出的c(OH-):②>① |
| C.①和②等体积混合后的溶液:c(OH-)=c(H+)+c(CH3COOH) |
| D.①和③无论以何种比例混合,混合后的溶液:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
含等物质的量NaOH的溶液分别用pH为2和3的CH3COOH溶液中和,设消耗CH3COOH溶液的体积依次为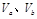 ,则两者的关系正确的是
,则两者的关系正确的是
A.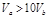 |
B.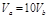 |
C.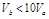 |
D.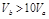 |
下列有关沉淀溶解平衡的说法中,正确的是()
A. Ksp(AB2)小于Ksp(CD),说明AB2的溶解度小于CD的溶解度
B.在氯化银的沉淀溶解平衡体系中加入蒸馏水,氯化银的Ksp增大
C.在碳酸钙的沉淀溶解平衡体系中加入稀盐酸,沉淀溶解平衡不移动
D.向氯化银沉淀溶解平衡体系中加人碘化钾固体,氯化银沉淀可转化为碘化银沉淀
已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:
Fe3+→Fe2+;MnO4-→Mn2+;Cl2→2Cl-;HNO3→NO。 如果分别用相同物质的量的这些物质氧化足量的KI,得到I2最多的是
| A.Fe3+ | B.MnO4- | C.Cl2 | D.HNO3 |
升高温度,下列常数中不一定增大的是
| A.平衡常数K | B.电离常数Ka |
| C.水的离子积常数Kw | D.盐的水解常数Kh |
含SO2的烟气会形成酸雨,工业上常利用Na2SO3溶液作为吸收液脱除烟气中的SO2。随着SO2的吸收,吸收液的pH不断变化。下列粒子浓度关系一定正确的是:
A.Na2SO3溶液中存在: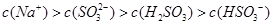 |
B.已知NaHSO3溶液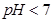 ,该溶液中: ,该溶液中: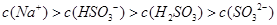 |
C.当吸收液呈中性时: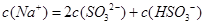 |
D.当吸收液呈酸性时: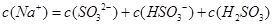 |
常温下,向20.00 mL 0.1000 mol·L—1 (NH4)2SO4溶液中逐滴加入0.2000 mol·L—1NaOH时,溶液的pH与所加NaOH溶液体积的关系如右下图所示(不考虑挥发)。下列说法正确的是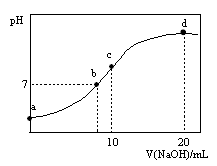
A.点a所示溶液中:c(NH )>c(SO )>c(SO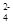 )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
B.点b所示溶液中:c(NH )=c(Na+)>c(H+)=c(OH-) )=c(Na+)>c(H+)=c(OH-) |
C.点c所示溶液中:c(SO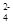 )+ c(H+)= c(NH3·H2O )+ c(OH-) )+ c(H+)= c(NH3·H2O )+ c(OH-) |
D.点d所示溶液中:c(SO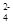 )>c(NH3·H2O )>c(OH-)>c(NH )>c(NH3·H2O )>c(OH-)>c(NH ) ) |
下列变化规律不正确的是()
| A.温度升高,水的电离平衡向右移动 |
| B.加水稀释时,醋酸钠的水解平衡向左移动 |
| C.增大压强,对醋酸的电离平衡影响不大 |
| D.向氯化铁溶液中加入氧化钠,水解平衡向右移动 |
下列溶液中Cl-浓度最大的是( )
| A.10mL 0.2mol/L的FeCl3溶液 | B.30mL 0.25mol/L的FeCl2溶液 |
| C.20mL 0.2mol/L的KCl溶液 | D.10mL 0.3mol/L的AlCl3溶液 |