在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,每摩尔CuSO4能氧化P的物质的量为
| A.1/5 mol | B.2/5 mol | C.3/5mol | D.11/5 mol |
a mol Cu与含b mol HNO3的溶液恰好完全反应,被还原的HNO3的物质的量一定是( )


| A.(b-2a) mol | B. mol | C. mol | D. mol |
已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:MnO4- → Mn2+ H2O2 → H2O HNO2 → NO IO3- → I2 如果用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
| A.MnO4- | B.H2O2 | C.HNO2 | D.IO3- |
已知Fe3O4可表示成(FeO·Fe2O3),水热法制备Fe3O4纳米颗粒的总反应为:3Fe2++2S2O +O2+4OH-=Fe3O4+S4O
+O2+4OH-=Fe3O4+S4O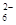 +2H2O,下列说法正确的是( )
+2H2O,下列说法正确的是( )
A.O2和S2O 是氧化剂,Fe2+是还原剂 是氧化剂,Fe2+是还原剂 |
| B.每生成1mol Fe3O4,则转移电子数为2mol |
| C.参加反应的氧化剂与还原剂的物质的最之比为1:1 |
| D.若有2mol Fe2+被氧化,则被Fe2+还原的O2为0.5mol |
已知向氯酸钠的酸性水溶液中通入二氧化硫,反应中SO2氧化过程为:SO2+2H2 O–
2 e-→SO42-+4H+;向亚氯酸钠(NaClO2)固体中通入用空气稀释的氯气,反应中还原过程为:Cl2 + 2 e- →2Cl-。在上述两个反应中均会生成产物X,则X的化学式为( )
| A.NaClO | B.NaClO4 | C.HClO | D.ClO2 |
工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为:
(1)4FeO·Cr2O3+8Na2CO3+7O2高温8Na2CrO4+2Fe2O3+8CO2
(2)2Na2CrO4+H2SO4 Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法正确的是
| A.反应(1)和(2)均为氧化还原反应 |
| B.反应(1)的氧化剂是O2,还原剂是FeO·Cr2O3 |
| C.Na2Cr2O7中Cr元素的化合价为+7 |
| D.反应(1)中生成1mol的Na2CrO4时共转移28mol电子 |
Cl2是纺织工业常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”。S2O32- 和Cl2反应的产物之一为SO42-。下列说法不正确的是
| A.该反应中还原剂是S2O32- |
| B.H2O参与该反应,且作氧化剂 |
| C.根据该反应可判断氧化性:Cl2>SO42- |
| D.上述反应中,每生成l mol SO42-,可脱去2mol Cl2 |
a mol FeS与b mol FeO投入到VL、c mol/L的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为①(a+b)×189g ②Vc-(9a+b) mol ③(a+b)mol ④Vc-(9a+b)/3mol
| A.①④ | B.②③ | C.①③ | D.②④ |
在一定温度下,1 mol金属铜与足量某浓度的硝酸完全反应,生成NO2和NO的
物质的量之比为1:3,则反应过程中转移的电子总数为
| A.2 mol | B.3 mol | C.4mol | D.5 mo1 |
研究发现用铝热法可从下列氧化物中冶炼出有关金属,若要得到等物质的量的有关金属单质,需消耗单质铝最多的是:
| A.MnO2 | B.V2O5 | C.Cr2O3 | D.WO3 |
a mol Cu与含b mol HNO3的溶液恰好完全反应,被还原的HNO3的物质的量一定是( )
Fe3+、Fe2+、NH4+、H+、H2O、NO3-六种粒子,它们都是同一氧化还原反应中的反应物或生成物。下列叙述中不正确的是( )
| A.该反应中氧化剂与还原剂的物质的量之比为1∶8 |
| B.若有1mol NO3-发生还原反应,转移的电子数为8mol |
| C.该反应说明Fe(NO3)2溶液不宜加酸酸化 |
| D.若把该反应设计成原电池,负极的反应为Fe2+-e-=Fe3+ |
已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:MnO4- → Mn2+ H2O2 → H2O HNO2 → NO IO3- → I2 如果用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
| A.MnO4- | B.H2O2 | C.HNO2 | D.IO3- |
已知反应10AgF+5Cl2+5H2O=9AgCl+AgClO3+10HF+O2,则有1molO2生成时反应所转移的电子总数为(NA表示阿伏加德罗常数的值) ( )
| A.9 NA | B.4 NA | C.10 NA | D.5 NA |