水热法制备Fe3O4纳米颗粒的反应为:
3Fe2++2S2O32-+O2+xOH-===Fe3O4+S4O62-+2H2O,下列说法中错误的是
| A.每生成1 mol Fe3O4,反应转移的电子总数为4 mol |
| B.Fe2+和S2O32-都是还原剂 |
C.1 mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为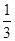 mol mol |
| D.x=4 |
16mL由NO与NH3组成的混合气体在催化剂作用下于400℃左右可发生反应6NO+4NH3====5N2+6H2O,达到平衡时在相同条件下体积变为17mL,则原混合气体中NO与NH3的体积比可能是( )
①3:1 ②3:2 ③3:4 ④3:5
| A.①② | B.①④ | C.②③ | D.③④ |
一定量的KMnO4与足量的250mL浓盐酸反应,方程式为2KMnO4+16HCl(浓)=2KCl+5Cl2↑+2MnCl2+8H2O,反应结束后,共转移电子为5mol,则还原产物中,阳离子的物质的量浓度为(溶液的体积变化忽略不计)( )
| A.1mol/L | B.2mol/L | C.4mol/L | D.8mol/L |
氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:aHClO3=bO2↑+ cCl2↑+ d HClO4 +eH2O。下列有关说法不正确的是
| A.还原产物只有Cl2 |
| B.若氯酸分解所得混合气体,lmol混合气体质量为45g,则反应方程式可表示为: 3HClO3 =2O2↑+ C12↑+ HClO4 + H2O |
| C.由非金属性Cl>S,可推知酸性HClO3>H2SO4 |
| D.若化学计量数a=8,b=3,则该反应转移电子数为20 |
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,其与水反应的化学方程式是:4K2FeO4+10H2O=4Fe(OH)3(胶体)+3O2↑+8KOH,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入一定量的KOH就可制得高铁酸钾。制备高铁酸钠的两种方法的主要反应原理如下:
湿法制备:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O
干法制备:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法中错误的是
| A.高铁酸钾处理水时,水发生氧化反应 |
| B.湿法中每生成1mol Na2FeO4共转移3mol电子 |
| C.干法中每生成1mol Na2FeO4共转移4mol电子 |
| D.K2FeO4处理水时,不仅能杀菌,并能使悬浮杂质沉降 |
已知NH4CuSO3与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体③溶液呈现蓝色。据此判断下列说法正确的是
| A.反应中硫酸作氧化剂 |
| B.NH4CuSO3中硫元素被氧化 |
| C.刺激性气味的气体是氨气 |
| D.1molNH4CuSO3完全反应转移0.5mol电子 |
SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;
②Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
下列有关说法错误的是
| A.氧化性:Cr2O72->Fe3+>SO2 |
| B.K2Cr2O7能将Na2SO3氧化成Na2SO4 |
| C.每有1 mol K2Cr2O7参加反应,转移电子的数目为6NA |
| D.若有6.72 L SO2(标准状况)参加反应,则最终消耗0.2 mol K2Cr2O7 |
在酸性条件下,向含铬废水中加入FeSO4,可将有害的Cr2O72﹣转化为 Cr3+,然后再加入熟石灰调节溶液的pH,使Cr3+ 转化为Cr(OH)3沉淀而从废水中除去。下列说法正确的是
| A.FeSO4在反应中作氧化剂 |
| B.随着反应的进行,该废水的pH会减小 |
| C.若该反应转移0.6mol e﹣,则会有0.2mol Cr2O72﹣ 被还原 |
| D.除去废水中含铬元素离子的过程包括氧化还原反应和复分解反应 |
有一混合溶液,其中只含有Fe2+、Cl-、Br-、I-(忽略水的电离),其中Cl-、Br-、I-的个数之比为2:3:3,向溶液中通入氯气,使溶液中Cl-和Br-的个数比为7:3(已知还原性I->Fe2+>Br->Cl-),则通入氯气的物质的量与溶液中剩余的Fe2+的物质的量之比为
| A.5:4 | B.4:5 | C.5:12 | D.12:5 |
工业上把Cl2通入冷NaOH溶液中制得漂白液(主要成分NaClO)。某化学小组在一定温度下将氯气缓缓通入NaOH溶液,模拟实验得到ClO-、ClO3-等离子其物质的量(mol)与反应时间t(min)的关系曲线.下列说法错误的是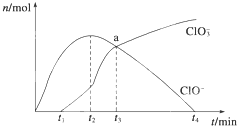
| A.参加反应所需NaOH与氯气的物质的量之比一定为2:1 |
| B.a点时溶液中n(NaCl):n(NaClO3):n(NaClO)=6:1:1 |
| C.t2~t4,ClO-离子的物质的量下降的原因可能是3ClO-=2Cl-+ClO3- |
| D.使用漂白液时,为了增强漂白效果,可以向漂白液中加入浓盐酸 |
在1000 mL含有等物质的量的HBr和H2SO3溶液中通入0.01 molCl2,有一半 变为Br2,原溶液中HBr和H2SO3的浓度都等于
变为Br2,原溶液中HBr和H2SO3的浓度都等于
A.0.007 5 mol· |
B.0.008 mol· |
C.0.075 mol· |
D.0.08 mol· |
根据表中信息判断,下列选项不正确的是
| 序号 |
反应物 |
产物 |
| ① |
KMnO4、H2O2 、H2SO4 |
K2SO4、MnSO4...... |
| ② |
Cl2、FeBr2 |
FeCl3、FeBr3 |
| ③ |
MnO4-... |
Cl2、Mn2+、H2O |
A.第①组反应的其余产物为H2O和 O2
B.第②组反应中Cl2与 FeBr2的物质的量之比为1︰2
C.第③组反应中生成1mol Cl2,转移电子2mol
D.氧化性由强到弱顺序为MnO4-> Cl2 > Fe3+ > Br2
已知S2O8n-离子和H2O2一样含有过氧键,因此也有强氧化性,S2O8n-离子在一定条件下可把Mn2+氧化成MnO4-离子,若反应后S2O8n-离子生成SO42-离子;又知反应中氧化剂与还原剂的离子数之比为5:2,则S2O8n-中的n值和S元素的化合价是
| A.2, +6 | B.2, +7 | C.4 ,+6 | D.4 , +7 |
将3.48gFe3O4完全溶解在100mL 1mol·L-1 H2SO4溶液中,然后加入K2Cr2O7溶液25mL,恰好使溶液中的Fe2+全部反应完,Cr2O72-全部转化为Cr3+,则K2Cr2O7溶液的物质的量浓度为
| A.0.033mol·L—1 | B.0.3mol·L—1 | C.0.2mol·L—1 | D.0.1mol·L—1 |