Langmuir提出等电子体的概念:原子总数相同、电子总数或价电子总数相同的粒子互为等电子体,等电子体通常具有结构相似的特征。下列各对粒子中,空间结构相似的是
| A.CS2与NO2 | B.CO2与H2O | C.SO2与O3 | D.PCl3与BF3 |
下列反应过程中,同时有离子键、极性键和非极性键的断裂和形成的是
A.NH4Cl  NH3↑+HCl↑ NH3↑+HCl↑ |
B.NH3+CO2+H2O===NH4HCO3 |
| C.2Na2O2+2H2O===4NaOH+O2 ↑ | D.2NaOH+Cl2===NaCl+NaClO+H2O |
某配合物的分子结构如图所示,其分子内不含有( )

| A.离子键 | B.共价键 | C.配位键 | D.氢键 |
根据元素周期律和化学键的相关知识,分析下面的推断中错误的是( )
| A.Al原子失电子能力比镁弱 | B.HNO3酸性比H2CO3强 |
| C.NaOH碱性比Mg(OH)2强 | D.HCl能电离产生H+和Cl—,所以HCl是离子化合物 |
下列五种物质中,①Ar ②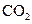 ③
③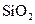 ④NaOH ⑤CaCl2
④NaOH ⑤CaCl2
只存在共价键的是 (填序号),只存在离子键的是 ,既存在离子键又
存在共价键的是 ,不存在化学键的是 。属于共价化合物的是 ,
属于离子化合物的是 。
下列说法正确的是( )
| A.离子化合物只能由金属元素和非金属元素组成 |
| B.离子化合物只能存在离子键 |
| C.盐酸能电离出氢离子和氯离子,所以HCl存在离子键 |
| D.共价化合物中不可能存在离子键 |
下列各组物质发生状态变化所克服的微粒间的相互作用属于同种类型的是( )
| A.食盐和蔗糖溶于水 | B.氯化钠和硫熔化 |
| C.碘和干冰升华 | D.二氧化硅和氧化钠熔化 |
下列每组物质发生状态变化所克服的微粒间的相互作用属于同种类型的是( )
| A.食盐和蔗糖熔化 | B.金刚石和硫熔化 |
| C.碘和干冰升华 | D.二氧化硅和氧化钠熔化 |
下列各组物质中化学键的类型完全相同的是 ( )
| A.MgCl2 NH4Cl | B.H2O O2 |
| C.NH3 H2O | D.NaCl HCl |
据权威刊物报道,1996年科学家在宇宙中发现H3分子。甲、乙、丙、丁四位学生对此报道的认识正确的是( )
| A.甲认为上述发现绝对不可能,因为H3分子违背了共价键理论 |
| B.乙认为宇宙中还可能存在另一种氢单质,因为氢元素有三种同位素必然有三种同素异形体 |
| C.丙认为H3分子实质上是H2分子与H+以特殊共价键结合的产物,应写成H3+ |
| D.丁认为如果上述的发现存在,则证明传统的价键理论有一定的局限性有待继续发展 |