(12分)某实验小组用无水乙醇、乙酸与浓硫酸制取乙酸乙酯并提纯,已知乙醇可以和氯化钙反应生成微溶的CaCl2·6C2H5OH。请回答下列问题:
(1)制备乙酸乙酯装置如图所示,虚框内玻璃仪器名称为 ;冷凝水流经冷凝管时应从 口进入(填“a”或“b”);
(2)生成乙酸乙酯的化学反应方程式为 ;
(3)下列措施可提高乙酸的转化率可采取的有( )
A.增加乙醇的用量 B.蒸出乙酸乙酯
C.增加乙酸的用量 D.冷凝管中通热水
(4)实验所得乙酸乙酯远低于理论产量的可能原因 。(写出其中两种)
(5)为了除去粗产品其中的醋酸,可向产品中加入 溶液,在分液漏斗中充分振荡,然后静置,待分层后 (填选项)。
A.直接将有机层从分液漏斗上口倒出
B.直接将有机层从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将有机层从下口放出
D.先将水层从分液漏斗的下口放出,再将有机层从上口倒出
(6)再向得到的有机物粗产品中加入饱和氯化钙溶液,振荡、分离。加入饱和氯化钙溶液的目的是 。
(7)最后,加入干燥剂除去其中的水分,再进行 (填操作),即可得到纯净的乙酸乙酯。
某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇制备环己烯
已知:
| |
密度(g/cm3) |
熔点(℃) |
沸点(℃) |
溶解性 |
| 环己醇 |
0.96 |
25 |
61 |
能溶于水 |
| 环己烯 |
0.81 |
-103 |
83 |
难溶于水 |
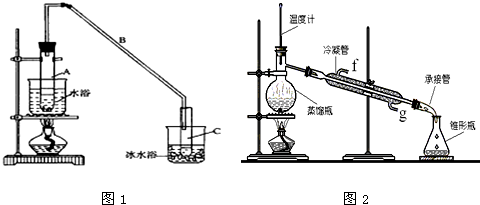
(1)制备粗品:将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.
①A中碎瓷片的作用是 ,导管B除了导气外还具有的作用是 .
②试管C置于冰水浴中的目的是 .
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等.加入饱和食盐水,振荡、静置、分层,环己烯在______层(填上或下),分液后用______(填入编号)洗涤.
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按图2所示装置蒸馏,冷却水从______口进入。蒸馏时要加入生石灰,目的是 .
③收集产品时,控制的温度应在____左右,实验制得的环己烯精品质量低于理论产量,可能的原因是____
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是______.
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点.
制备水杨酸对正辛基苯基酯( )如下:
)如下:
步骤一:将水杨酸晶体投入三颈烧瓶中,再加入氯苯,搅拌溶解后,加入无水三氯化铝。
步骤二:按图12所示装置装配好仪器,水浴加热控制温度在20~40℃之间,在搅拌下滴加SOCl2,反应制得水杨酰氯。该反应为:
 (水杨酸)+SOCl2—→
(水杨酸)+SOCl2—→ (水杨酰氯)+HCl↑+SO2↑
(水杨酰氯)+HCl↑+SO2↑

步骤三:将三颈烧瓶中的混合液升温至80℃,再加入对正辛苯酚[ ],温度控制在100℃左右,不断搅拌。
],温度控制在100℃左右,不断搅拌。
步骤四:过滤、蒸馏、减压过滤;酒精洗涤、干燥。
(1)步骤一中加入三氯化铝的作用是 。
(2)实验时,冷凝管中的水应从 进 出(选填“a”或“b”);装置c的作用是 。
(3)步骤三中发生反应的化学方程式为 。
(4)步骤四减压过滤操作中,除烧杯、玻璃棒外,还必须使用的硅酸盐材料的仪器有 。
(5)步骤四减压过滤时,有时滤纸会穿孔,避免滤纸穿孔的措施是 。
B.[实验化学]
实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的相关数据如下表。
| 化合物 |
相对分子质量 |
密度/g·cm-3 |
沸点/℃ |
溶解度/100 g水 |
| 正丁醇 |
74 |
0.80 |
118.0 |
9 |
| 冰醋酸 |
60 |
1.045 |
118.1 |
互溶 |
| 乙酸正丁酯 |
116 |
0.882 |
126.1 |
0.7 |
请回答有关问题。
Ⅰ.乙酸正丁酯粗产品的制备在三颈圆底烧瓶中进行,并使用了分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管。实验需要的药品:浓硫酸、冰醋酸和正丁醇。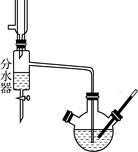
(1)有同学拟通过核磁共振氢谱鉴定所得产物中是否含有正丁醇,正丁醇的氢谱线中的几个峰的面积之比是________。
(2)反应前三颈圆底烧瓶中先加人适量沸石,然后依次加入________。
(3)分水器的作用________。
Ⅱ.乙酸正丁酯粗产品的精制。
(1)将三颈圆底烧瓶中的液体转入分液漏斗中,并用________洗涤有机层,用分液法分离上述有机层和水层,分液完成后,取出有机层的操作是________。
(2)将酯层进行蒸馏。蒸馏收集乙酸正丁酯产品。
Ⅲ.计算产率
如果实验中加入了18.5 mL正丁醇、15.4 mL冰醋酸和2 mL浓硫酸,实验后制得的乙酸正丁酯的质量为12.76 g,则乙酸正丁酯的产率为________。
B.草酸二乙酯可用于苯巴比妥等药物的中间体,实验室以草酸(HOOC—COOH)和乙醇为原料制备草酸二乙酯的实验步骤如下:
步骤1:在上图所示装置中,加入无水草酸45g,无水乙醇81g,苯200mL,浓硫酸10mL,搅拌下加热6870℃回流共沸脱水。
步骤2:待水基本蒸完后,分离出乙醇和苯。
步骤3:所得混合液冷却后依次用水、饱和碳酸氢钠溶液洗涤,再用无水硫酸钠干燥。
步骤4:常压蒸馏,收集182-184℃的馏分,得草酸二乙酯57g。
(1)步骤1中发生反应的化学方程式是 ,反应过程中冷凝水应从 (填“a”或“b”)端进入。
(2)步骤2操作为 。
(3)步骤3用饱和碳酸氢钠溶液洗涤的目的是 。
(4)步骤4除抽气减压装置外所用玻璃仪器有蒸馏烧瓶、冷凝管、接液管、锥形瓶和 。
(5)本实验中,草酸二乙酯的产率为 。
化学实验装置的科学设计是实验是否取得预期效果的关键。请回答下列有关实验装置的相关问题:
Ⅰ.下图A为“人教版”教材制备乙酸乙酯的实验装置,某同学甲认为下图B装置进行酯化反应效果比A要好,他的理由是_________________________;
某同学乙经查阅资料认为下图C装置进行酯化反应效果更好,他的理由是 ________________________。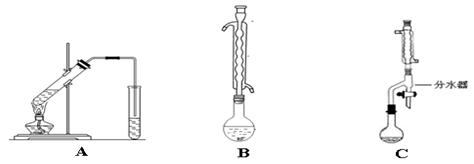
Ⅱ.某实验小组欲探究碳与浓硝酸反应的情况。甲同学设计了图1装置,认为若有红棕色气体产生就说明碳与浓硝酸发生了反应。
(1)碳与浓硝酸反应的方程式_______________________。甲同学的实验应该在___________中进行,才符合化学实验安全性的要求。
(2)乙同学认为红棕色气体不一定是碳与浓硝酸发生反应而得,所以他认为甲同学观点是错误的,他的理由是________________(用化学方程式表示),所以他认为应该检验_____________(填化学式)的产生来证明碳与浓硝酸反应。为此乙同学查阅相关资料得知“0℃时四氧化二氮为液体”,从而改进了实验装置如图2所示。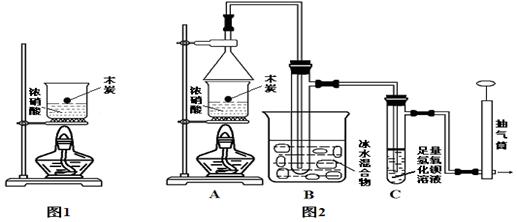
(3)为了减少干扰,对于A装置有下面4种操作方案,其中最合理的是(填写数字序号)_________。
①将木炭与浓硝酸一同放在装置中加热;②先加热木炭,再将木炭投入冷浓硝酸。③先加热木炭,再加入冷浓硝酸;④先加热浓硝酸,然后将木炭投入其中;
(4)请用平衡移动原理解释B装置的作用_________(结合方程式与文字表述)。
(5)C装置中出现的现象是_________,经检测C的溶液中还含有少量氮元素,只以NO3-形式存在,写出生成该离子的化学方程式 ________________。
苯甲酸乙酯(C9H10O2)别名为安息香酸乙酯。 它是一种无色透明液体,不溶于水,稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体,溶剂等。其制备方法为:
已知:
| 名称 |
相对分子质量 |
颜色,状态 |
沸点(℃) |
密度(g·cm-3) |
| 苯甲酸* |
122 |
无色片状晶体 |
249 |
1.2659 |
| 苯甲酸乙酯 |
150 |
无色澄清液体 |
212.6 |
1.05 |
| 乙醇 |
46 |
无色澄清液体 |
78.3 |
0.7893 |
| 环己烷 |
84 |
无色澄清液体 |
80.8 |
0.7318 |
*苯甲酸在100℃会迅速升华。
实验步骤如下:
①在圆底烧瓶中加入12.20 g苯甲酸,25 mL 95%的乙醇(过量),20 mL环己烷以及4 mL浓硫酸,混合均匀并加入沸石,按下图所示装好仪器,控制温度在65~70℃加热回流2 h。利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。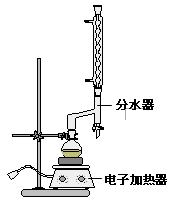
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞,继续加热,至分水器中收集到的液体不再明显增加,停止加热。
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液至呈中性。用分液漏斗分出有机层,水层用25 mL乙醚萃取分液,然后合并至有机层,加入氯化钙,静置,过滤,对滤液进行蒸馏,低温蒸出乙醚和环己烷后,继续升温,接收210~213℃的馏分。
④检验合格,测得产品体积为12.86 mL。
回答下列问题:
(1)在该实验中,圆底烧瓶的容积最适合的是 (填入正确选项前的字母)。
A.25 mL B.50 mL C.100 mL D.250 mL
(2)步骤①中使用分水器不断分离除去水的目的是 。
(3)步骤②中应控制馏分的温度在 。
A.65~70℃ B.78~80℃ C.85~90℃ D.215~220℃
(4)步骤③加入Na2CO3的作用是 ;若Na2CO3加入不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是 。
(5)关于步骤③中的萃取分液操作叙述正确的是 。
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞,分液漏斗倒转过来用力振摇
B.振摇几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振摇并放气后,手持分液漏斗静置待液体分层
D.放出液体时,应打开上口玻璃塞或将玻璃塞上的凹槽对准漏斗口上的小孔
(6)计算本实验的产率为 。
(每空2分,共10分)在试管A中加入3mL乙醇,然后边振荡管边慢慢加入2mL浓硫酸和2mL乙酸,按下图所示连接好装置进行实验,以制取乙酸乙酯。

(1)试管B中盛放的试剂是 (填名称),实验时往往在B试管中可以看到少量气泡,写出与此现象对应的离子方程式 。
(2)乙醇与乙酸反应的化学方程式是 。
(3)实验完成后,试管B的液面上有透明的不溶于水的油状液体产生。若要分离B中的液体混合物需要用到的玻璃仪器是 。
(4)用30g乙酸与46g乙醇反应,如果实验产率是理论产率的60%,则可得到的产物质量是 g。
(16分)某实验小组用无水乙醇、乙酸与浓硫酸制取乙酸乙酯并提纯,已知乙醇可以和氯化钙反应生成微溶的CaCl2·6C2H5OH。
(1)制备乙酸乙酯装置如图所示,虚框内玻璃仪器名称为 ;

(2)生成乙酸乙酯的化学反应方程式为 ;浓硫酸的作用是 ;
(3)冷凝水流经冷凝管时应从 口进入(填“a”或“b”);
(4)下列措施可提高乙酸的转化率可采取的有( )
A.增加乙醇的用量 B.蒸出乙酸乙酯
C.增加乙酸的用量 D.冷凝管中通热水
(5)实验所得乙酸乙酯远低于理论产量的可能原因 。(写出其中两种)
(6)为了除去粗产品其中的醋酸,可向产品中加入 溶液,在分液漏斗中充分振荡, 然后静置,待分层后 (填选项)。
A.直接将有机层从分液漏斗上口倒出
B.直接将有机层从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将有机层从下口放出
D.先将水层从分液漏斗的下口放出,再将有机层从上口倒出
(7)再向得到的有机物粗产品中加入饱和氯化钙溶液,振荡、分离。加入饱和氯化钙溶液的目的是 。
(8)最后,加入干燥剂除去其中的水分,再进行 (填操作),即可得到纯净的乙酸乙酯。
17.下图装置Ⅰ是实验室制乙酸乙酯的常用装置:

实验中所用的某些试剂及产物的相关数据如下:
| 物 质 |
熔点/℃ |
沸点/℃ |
||
| 乙 醇 |
-114 |
78 |
||
| 乙 酸 |
16.6 |
117.9 |
||
| 乙酸乙酯 |
-83.6 |
77.5 |
||
| 98%H2SO4 |
10 |
338 |
回答下列问题:
(1)如果用CH3CO18OH与CH3CH2OH反应,写出该反应的化学方程式 ,浓H2SO4的作用是 。
(2)要从装置Ⅰ中右侧小试管中分离出乙酸乙酯,应进行的操作是:撤出小试管,将混合液倒入 (填仪器名称),用力振荡,静置, (填现象),然后将产物从__ ___口(填“上”或“下”)倒出。
(3)采用装置Ⅱ可提高乙酸乙酯的产率,结合表格中的数据,说明该装置可提高乙酸乙酯产率的原因: 。
25.(12分)可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空:
(1)试管a中需加入浓硫酸、冰醋酸和乙醇各2mL,正确的加入顺序用操作是 。
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是 。
(3)实验中加热试管a的目的是: ; 。
(4)试管b中加有饱和Na2CO3溶液,其作用是 。
(5)反应结束后,振荡试管b,静置。反应结束后,试管B内的液体分成两层,乙酸乙酯在 层(填写“上”或“下”).若分离10mL该液体混合物需要用到的主要玻璃仪器是 .
(I)已知:R-OH+HX→R-X+H2O。右图是实验室用乙醇与浓硫酸和溴化钠反应制备溴乙烷的装置,图中省去了加热装置。
有关数据见下表:乙醇、溴乙烷、溴有关参数
| |
乙醇 |
溴乙烷 |
溴 |
| 状态 |
无色液体 |
无色液体 |
深红棕色液体 |
| 密度/g•cm-3 |
0.79 |
1.44 |
3.1 |
| 沸点/℃ |
78.5 |
38.4 |
59 |
(1)制备操作中,加入的浓硫酸必需进行稀释,其目的是 。
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(2)加热的目的是 (从速率和限度两方面回答);应采取的加热方式是 。
(3)为除去产品中的一种主要杂质,最好选择下列_____溶液来洗涤产品。
A.氢氧化钠 B.碘化钠 C.亚硫酸钠
(4)第(3)步的实验所需要的主要玻璃仪器是 。
(Ⅱ)苯甲酸甲酯( )是一种重要的工业有机溶剂。请分析下列有机物的结构简式或性质特点,然后回答问题。
)是一种重要的工业有机溶剂。请分析下列有机物的结构简式或性质特点,然后回答问题。
(1)乙中含氧官能团的名称是 。
(2)甲、乙、丙三种有机物中与苯甲酸甲酯是同分异构体的是 。与NaOH溶液在加热条件下反应消耗NaOH最多的是 。
(3)符合丙条件的结构可能有________,种,写出其中两种 。
下图装置Ⅰ是实验室制乙酸乙酯的常用装置:

实验中所用的某些试剂及产物的相关数据如下:
| 物 质 |
熔点/℃ |
沸点/℃ |
||
| 乙 醇 |
-114 |
78 |
||
| 乙 酸 |
16.6 |
117.9 |
||
| 乙酸乙酯 |
-83.6 |
77.5 |
||
| 98%H2SO4 |
10 |
338 |
回答下列问题:
(1)如果用CH3CO18OH与CH3CH2OH反应,写出该反应的化学方程式 ,浓H2SO4的作用是 。
(2)要从装置Ⅰ中右侧小试管中分离出乙酸乙酯,应进行的操作是:撤出小试管,将混合液倒入 (填仪器名称),用力振荡,静置, (填现象),然后将产物从__ __口(填“上”或“下”)倒出。
(3)采用装置Ⅱ可提高乙酸乙酯的产率,结合表格中的数据,说明该装置可提高乙酸乙酯产率的原因: 。
(14分)乙酸异戊酯( )是组成蜜蜂信息素的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图(有关的加热和夹持仪器略去)和有关数据如下:
)是组成蜜蜂信息素的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图(有关的加热和夹持仪器略去)和有关数据如下:
实验步骤:在烧瓶中加入4.4 g的异戊醇,6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热烧瓶,回流50分钟,反应液冷至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量无水硫酸镁固体,静置片刻,过滤除去硫酸镁晶体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。回答下列问题:
| |
相对分子质量 |
密度/(g·cm-3) |
沸点/℃ |
水中溶解性 |
| 异戊醇 |
88 |
0.8123 |
131 |
微溶 |
| 乙酸 |
60 |
1.0492 |
118 |
溶 |
| 乙酸异戊酯 |
130 |
0.8670 |
142 |
难溶 |
(1)写出制取乙酸异戊酯的化学方程式 。
(2)冷凝管的作用是 ,碎瓷片的作用是 。
(3)若乙酸异戊酯产率偏低,其原因可能是 。
A.原料没有充分反应
B.发生了副反应
C.在进行蒸馏纯化操作时,从143 ℃开始收集馏分
(4)在洗涤、分液操作中,应充分振荡,然后静置,待分层后 (填标号),
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(5)实验中加入少量无水硫酸镁的目的是 。
(6)本实验的产率是
A.30℅ B.40℅ C.50℅ D.60℅
实验室制取乙酸丁酯的实验装置有如右下图所示两种装置供选用。其有关物质的物理性质
如下表:
| |
乙酸 |
1-丁醇 |
乙酸丁酯 |
| 熔点(℃) |
16.6 |
-89.5 |
-73.5 |
| 沸点(℃) |
117.9 |
117 |
126.3 |
| 密度(g/cm3) |
1.05 |
0.81 |
0.88 |
| 水溶性 |
互溶 |
可溶(9g/100g水) |
微溶 |
(1)制取乙酸丁酯的装置应选用_______(填“甲”或“乙”)。不选另一种装置的理由是 。
(2)该实验生成物中除了主产物乙酸丁酯外,还可能生成的有机副产物有(写出结构简式): 、 。
(3)酯化反应是一个可逆反应,为提高1-丁醇的利用率,可采取的措施是 。
(4)从制备乙酸丁酯所得的混合物中分离、提纯乙酸丁酯时,需要经过多步操作,下列图示的操作中,肯定需要的化学操作是__________(选填答案编号)。
(5)有机物的分离操作中,经常需要使用分液漏斗等仪器。使用分液漏斗前必须 ;某同学在进行分液操作时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还可能 。