实验室合成丙酸乙酯的反应装置如下图甲,其操作过程为:在图甲装置的二口烧瓶中加入浓硫酸和乙醇的混合物,再通过恒压滴液漏斗逐步加入一定量的丙酸,同时加热回流。
(1)请写出图甲中酯化反应的化学方程式 。
(2)已知酯化反应的催化剂为 ,图甲中选用浓硫酸而不选用稀硫酸的目的是 。
,图甲中选用浓硫酸而不选用稀硫酸的目的是 。
(3)图甲中除了制得产物酯外,因反应温度控制不当,还可能发生副反应产生的有机产物有 。
(4)为了得到纯净的酯,将图甲中反应后的混合液改装成图乙装置进行蒸馏分离时,图乙方框中应选用图丙中的 冷凝管(选填“A”或“B”)。
(5)用图甲装置制取酯比用图丁装置制取酯的优点在于 。
制备水杨酸对正辛基苯基酯( )如下:
)如下:
步骤一:将水杨酸晶体投入三颈烧瓶中,再加入氯苯,搅拌溶解后,加入无水三氯化铝。
步骤二:按图12所示装置装配好仪器,水浴加热控制温度在20~40℃之间,在搅拌下滴加SOCl2,反应制得水杨酰氯。该反应为:
 (水杨酸)+SOCl2—→
(水杨酸)+SOCl2—→ (水杨酰氯)+HCl↑+SO2↑
(水杨酰氯)+HCl↑+SO2↑

步骤三:将三颈烧瓶中的混合液升温至80℃,再加入对正辛苯酚[ ],温度控制在100℃左右,不断搅拌。
],温度控制在100℃左右,不断搅拌。
步骤四:过滤、蒸馏、减压过滤;酒精洗涤、干燥。
(1)步骤一中加入三氯化铝的作用是 。
(2)实验时,冷凝管中的水应从 进 出(选填“a”或“b”);装置c的作用是 。
(3)步骤三中发生反应的化学方程式为 。
(4)步骤四减压过滤操作中,除烧杯、玻璃棒外,还必须使用的硅酸盐材料的仪器有 。
(5)步骤四减压过滤时,有时滤纸会穿孔,避免滤纸穿孔的措施是 。
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题: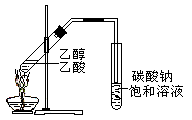
(1)写出制取乙酸乙酯的化学反应方程式 。
(2)浓硫酸的作用是:① ;② 。
(3)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
(4)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
(5)某同学将收集到的乙酸乙酯滴入饱和NaHCO3溶液中,观察到有少量气泡产生,可得出的结论是 ,该过程中发生反应的化学方程式是 。
(14分)4,7—二甲基香豆素(熔点:132.6℃)是一种重要的香料,广泛分布于植物界中,由间—甲苯酚为原料的合成反应如下: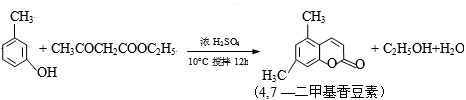
实验装置图如下: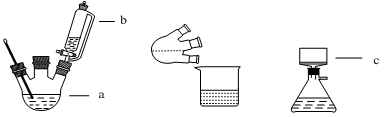
主要实验步骤:
步骤1:向装置a中加入60mL浓硫酸,并冷却至0℃以下,搅拌下滴入间—甲苯酚30mL(0.29mol)和乙酰乙酸乙酯26.4mL (0.21mol)的混合物。
步骤2:保持在10℃下,搅拌12h,反应完全后,将其倒入冰水混合物中,然后抽滤、水洗得粗产品
步骤3:粗产品用乙醇溶解并重结晶,得白色针状晶体并烘干,称得产品质量为33.0g。
(1)简述装置b中将活塞上下部分连通的目的 。
(2)浓H2SO4需要冷却至0℃以下的原因是 。
(3)反应需要搅拌12h,其原因是 。
(4)本次实验产率为 (百分数保留一位小数)
(5)实验室制备乙酸乙酯的化学反应方程式 ,用 (填药品名称)收集粗产品,用 (填操作名称)的方法把粗产品分离。
(每空2分,共10分)在试管A中加入3mL乙醇,然后边振荡管边慢慢加入2mL浓硫酸和2mL乙酸,按下图所示连接好装置进行实验,以制取乙酸乙酯。

(1)试管B中盛放的试剂是 (填名称),实验时往往在B试管中可以看到少量气泡,写出与此现象对应的离子方程式 。
(2)乙醇与乙酸反应的化学方程式是 。
(3)实验完成后,试管B的液面上有透明的不溶于水的油状液体产生。若要分离B中的液体混合物需要用到的玻璃仪器是 。
(4)用30g乙酸与46g乙醇反应,如果实验产率是理论产率的60%,则可得到的产物质量是 g。
(1)实验室用下图所示装置制备少量乙酸乙酯。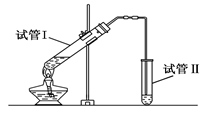
①写出制备乙酸乙酯的化学方程式_______________________。
②试管Ⅱ中盛的试剂是____________________________。
③若要把制得的乙酸乙酯分离出来,应采用的实验操作是________。
(2)已知乳酸的结构简式为 。试回答:
。试回答:
①乳酸分子中含有________和_________两种官能团(写名称);
②乳酸与足量金属钠反应的化学方程式为_____________________________;
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示的装置制取乙酸乙酯。回答下列问题:
(1)写出制取乙酸乙酯的化学反应方程式
(2)饱和碳酸钠溶液的主要作用是 。
| A.中和乙酸 | B.吸收乙醇 |
| C.降低酯的溶解度使分层清晰 | D.有利于酯的水解 |
(3)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
(4)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有 。(填序号)
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
苯甲酸甲酯是一种重要的工业原料,有机化学中通过酯化反应原理,可以进行苯甲酸甲酯的合成。有关物质的物理性质、实验装置如下所示:
| |
苯甲酸 |
甲醇 |
苯甲酸甲酯 |
| 熔点/℃ |
122.4 |
-97 |
-12.3 |
| 沸点/℃ |
249 |
64.3 |
199.6 |
| 密度/g.cm-3 |
1.2659 |
0.792 |
1.0888 |
| 水溶性 |
微溶 |
互溶 |
不溶 |
实验一:制取苯甲酸甲酯:在大试管中加入15g苯甲酸和一定量的甲醇,边振荡边缓慢加入一定量浓硫酸,按图A连接仪器并实验。

(1)苯甲酸与甲醇反应的化学方程式为______________________。
(2)大试管Ⅰ中除了装有15g苯甲酸和一定量的甲醇和沸石外还需要加入一定量浓硫酸,浓硫酸的作用是 。
(3)实验室制取乙酸乙酯时,为了除去乙酸乙酯中混有的乙酸所用试剂为 。
实验二:提纯苯甲酸甲酯:该实验要先把图A中制备的苯甲酸甲酯水洗提纯,再利用图B装置进行蒸馏提纯
(4)水洗提纯时所进行的操作为(填操作名称) 。
(5)用图B装置进行蒸馏提纯时,当温度计显示 时,可用锥形瓶收集苯甲酸甲酯。
B.草酸二乙酯可用于苯巴比妥等药物的中间体,实验室以草酸(HOOC—COOH)和乙醇为原料制备草酸二乙酯的实验步骤如下:
步骤1:在上图所示装置中,加入无水草酸45g,无水乙醇81g,苯200mL,浓硫酸10mL,搅拌下加热6870℃回流共沸脱水。
步骤2:待水基本蒸完后,分离出乙醇和苯。
步骤3:所得混合液冷却后依次用水、饱和碳酸氢钠溶液洗涤,再用无水硫酸钠干燥。
步骤4:常压蒸馏,收集182-184℃的馏分,得草酸二乙酯57g。
(1)步骤1中发生反应的化学方程式是 ,反应过程中冷凝水应从 (填“a”或“b”)端进入。
(2)步骤2操作为 。
(3)步骤3用饱和碳酸氢钠溶液洗涤的目的是 。
(4)步骤4除抽气减压装置外所用玻璃仪器有蒸馏烧瓶、冷凝管、接液管、锥形瓶和 。
(5)本实验中,草酸二乙酯的产率为 。
实验室用图示装置制取乙酸乙酯。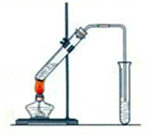
(1)浓H2SO4的作用是:①_____ _ __,②_____________。
(2)右边收集试管内装有 ,该溶液的作用是____________________。导气管不能插入液面以下,原因是 。加热前,大试管中加入几粒碎瓷片的作用是______________。
(3)制取乙酸乙酯的反应方程式是_______________________________________。
(4)实验室可用乙醇来制取乙烯,将生成的乙烯通入溴的四氯化碳溶液,反应后生成物的结构简式是_________________。
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,其目的是_____________。
(2)在烧瓶中配制一定比例的乙醇和浓硫酸的混合液的方法是:__________________。
(3)在该实验中,若用1 mol乙醇和1 mol乙酸在浓硫酸作用下加热,充分反应,能否生成1mol乙酸乙酯?______________,原因是____________________。
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。
试剂a是__________,试剂b是__________;分离方法①是__________,分离方法②是__________,分离方法③是____________。
(5)在得到的A中加入无水碳酸钠粉末,振荡,目的是_________________。
17.下图装置Ⅰ是实验室制乙酸乙酯的常用装置:

实验中所用的某些试剂及产物的相关数据如下:
| 物 质 |
熔点/℃ |
沸点/℃ |
||
| 乙 醇 |
-114 |
78 |
||
| 乙 酸 |
16.6 |
117.9 |
||
| 乙酸乙酯 |
-83.6 |
77.5 |
||
| 98%H2SO4 |
10 |
338 |
回答下列问题:
(1)如果用CH3CO18OH与CH3CH2OH反应,写出该反应的化学方程式 ,浓H2SO4的作用是 。
(2)要从装置Ⅰ中右侧小试管中分离出乙酸乙酯,应进行的操作是:撤出小试管,将混合液倒入 (填仪器名称),用力振荡,静置, (填现象),然后将产物从__ ___口(填“上”或“下”)倒出。
(3)采用装置Ⅱ可提高乙酸乙酯的产率,结合表格中的数据,说明该装置可提高乙酸乙酯产率的原因: 。
(10分)Ⅰ.实验室制得气体中常含有杂质,影响其性质检验。下图A为除杂装置,B为性质检验装置,完成下列表格: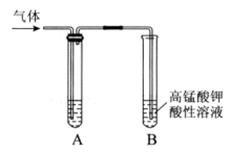
| 序号 |
气体 |
反应原理 |
A中试剂 |
| ① |
乙烯 |
溴乙烷和NaOH的醇溶液加热 |
|
| ② |
乙烯 |
无水乙醇在浓硫酸的作用下加热至170℃反应的化学方程式是 。 |
NaOH溶液 |
| ③ |
乙炔 |
电石与饱和食盐水反应 |
|
Ⅱ.为探究乙酸乙酯的水解情况,某同学取大小相同的3支试管,分别加入以下溶液,充分振荡,放在同一水浴加热相同时间,观察到如下现象。
| 试管编号 |
① |
② |
③ |
| 实验操作 |
 |
 |
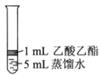 |
| 实验现象 |
酯层变薄 |
酯层消失 |
酯层基本不变 |
(1)试管①中反应的化学方程式是 ;
(2)对比试管①和试管③的实验现象,稀H2SO4的作用是 ;
(3)试用化学平衡移动原理解释试管②中酯层消失的原因 。
最常见的塑化剂邻苯二甲酸二丁酯可由邻苯二甲酸酐与正丁醇在浓硫酸共热下反应制得,反应的化学方程式及装置图(部分装置省略)如下:
已知:正丁醇沸点118℃,纯邻苯二甲酸二丁酯是无色透明、具有芳香气味的油状液体,沸点340℃,酸性条件下,温度超过180℃时易发生分解。
由邻苯二甲酸酐、正丁醇制备邻苯二甲酸二丁酯实验操作流程如下:
①向三颈烧瓶内加入30g(0.2mol)邻苯二甲酸酐,22g(0.3mol)正丁醇以及少量浓硫酸。
②搅拌,升温至105℃,持续搅拌反应2小时,保温至反应结束。
③冷却至室温,将反应混合物倒出.通过工艺流程中的操作X,得到粗产品。
④粗产品用无水硫酸镁处理至澄清→取清液(粗酯)→圆底烧瓶→减压蒸馏,经过处理得到产品20.85g。
请回答以下问题:
(1)步骤②中不断从分水器下部分离出产物水的目的是 。
判断反应已结束的方法是_______________________。
(2)上述实验可能生成的副产物的结构简式为 (填一种即可)
(3)操作X中,应先用5%Na2CO3溶液洗涤粗产品。纯碱溶液浓度不宜过高,更不能使用氢氧化钠;若使用氢氧化钠溶液,对产物有什么影响?(用化学方程式表示) 。
(4)操作X中,分离出产物的操作中必须使用的主要玻璃仪器有 。
(5)粗产品提纯流程中采用减压蒸馏的目的是___________________________。
(6)本实验中,邻苯二甲酸二丁酯(式量是278)的产率为 。
(I)已知:R-OH+HX→R-X+H2O。右图是实验室用乙醇与浓硫酸和溴化钠反应制备溴乙烷的装置,图中省去了加热装置。
有关数据见下表:乙醇、溴乙烷、溴有关参数
| |
乙醇 |
溴乙烷 |
溴 |
| 状态 |
无色液体 |
无色液体 |
深红棕色液体 |
| 密度/g•cm-3 |
0.79 |
1.44 |
3.1 |
| 沸点/℃ |
78.5 |
38.4 |
59 |
(1)制备操作中,加入的浓硫酸必需进行稀释,其目的是 。
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(2)加热的目的是 (从速率和限度两方面回答);应采取的加热方式是 。
(3)为除去产品中的一种主要杂质,最好选择下列_____溶液来洗涤产品。
A.氢氧化钠 B.碘化钠 C.亚硫酸钠
(4)第(3)步的实验所需要的主要玻璃仪器是 。
(Ⅱ)苯甲酸甲酯( )是一种重要的工业有机溶剂。请分析下列有机物的结构简式或性质特点,然后回答问题。
)是一种重要的工业有机溶剂。请分析下列有机物的结构简式或性质特点,然后回答问题。
(1)乙中含氧官能团的名称是 。
(2)甲、乙、丙三种有机物中与苯甲酸甲酯是同分异构体的是 。与NaOH溶液在加热条件下反应消耗NaOH最多的是 。
(3)符合丙条件的结构可能有________,种,写出其中两种 。