关于化学反应与能量的说法正确的是( )
| A.根据右图提供的信息,该反应是放热反应 |
| B.化学变化中的能量变化主要由化学键变化引起的 |
| C.化学反应中只伴随热量的变化 |
| D.CaCO3(s)==CaO(s)+CO2(g) ΔH="+178.5" KJ·mol-1的意义是表示1mol CaCO3完全分解生成1mol CaO和1mol CO2气体要放出178.5 KJ的热量 |
市场上经常见锂离子电池,它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导的高分子材料。这种锂离子电池的电池反应式为:

。下列说法不正确的是( )
| A. |
放电时,负极的电极反应式:
|
| B. | 该电池不能用水溶液作为电解质 |
| C. |
充电时,
|
| D. |
放电过程中
|
已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ。且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H—O键形成时放出热量463kJ,则氢气中1 mol H—H键断裂时吸收热量为 ( )
| A.920 kJ | B.557 kJ | C.436 kJ | D.188 kJ |
强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O(1) ⊿H=-57 .3kJ/mol。向1L0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时的热效应⊿H1、⊿H2、⊿H3的关系正确的是
.3kJ/mol。向1L0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时的热效应⊿H1、⊿H2、⊿H3的关系正确的是
| A.⊿H1>⊿H2>⊿H3 | B.⊿H1<⊿H3<⊿H2 | C.⊿H1<⊿H2<⊿H3 | D.⊿H1>⊿H3>⊿H2 |
下列说法正确的是:
A.在100 ℃、101 kPa条件下,1mol液态水气化时需要吸收40.69 kJ的热量,则H2O(g) H2O(l) 的ΔH = +40.69 kJ·mol-1 H2O(l) 的ΔH = +40.69 kJ·mol-1 |
| B.已知CH4 (g)+2O2(g)=CO2(g)+2H2O(l);△H=-802.33kJ/mol,则CH4的燃烧热为802.33 kJ |
C.H2(g)+Br2(g)=2HBr(g)△H=-72kJ·mol-1其它相关数据如下表: 则表中a为230 |
| D.已知S (g)+O2(g)=SO2(s);△H1,S (g)+O2(g)=SO2(g);△H2,则△H2<△H1 |
下列说法正确的是
| A.CO能继续和氧气反应生成稳定的CO2,所以CO的燃烧反应一定是吸热反应 |
| B.1 mol硫酸与1 mol Ba(OH)2完全中和所放出的热量为中和热 |
| C.相同条件下,2mol氢原子所具有的能量大于1mol氢分子所具有的能量 |
| D.101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热 |
已知热化学方程式(Q1、Q2均为正值):
C(s)+ O2(g) =CO(g) ΔH=-Q1 kJ·mol-1,C(s)+O2(g) =CO2(g) ΔH=-Q2 kJ·mol-1,
O2(g) =CO(g) ΔH=-Q1 kJ·mol-1,C(s)+O2(g) =CO2(g) ΔH=-Q2 kJ·mol-1,
有关上述反应的叙述错误的是
| A.Q1<Q2 |
| B.生成物总能量均高于反应物总能量 |
| C.由1 mol C反应生成1 mol CO气体时放出Q1 kJ的热量 |
| D.1 mol CO2气体具有的能量大于1 mol干冰具有的能量 |
下列说法或表示方法正确的( )
A.已知C(s)+O2(g)===CO2(g) ;C(s)+ ;C(s)+ O2(g)===CO (g) O2(g)===CO (g) ,则 ,则  |
B.在稀溶液中,H+(aq)+OH-(aq)===H2O(l)  kJ·mol-1,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热大于57.3 kJ kJ·mol-1,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热大于57.3 kJ |
C.由C(石墨)===C(金刚石); kJ·mol-1可知,金刚石比石墨稳定 kJ·mol-1可知,金刚石比石墨稳定 |
| D.已知氢气的标准燃烧热为-285.8 kJ·mol-1,相应的热化学方程式为2H2(g) + O2(g)=2H2O(l) ΔH = –285.8kJ·mol-1 |
硫单质有两种常见的同素异形体:单斜硫和正交硫。已知常温常压下: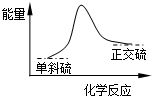
① S (s,单斜)+O2 (g)→SO2 (g)+297.16kJ;
② S (s,正交)+O2 (g)→SO2 (g)+296.83kJ
下列说法正确的是
| A.常温常压下单斜硫比正交硫稳定 |
| B.单斜硫转变为正交硫的能量变化可用右图表示 |
| C.S(g)+O2(g)→SO2(g)+Q3 Q3>296.83kJ |
| D.反应①中生成1 L SO2 (g)放出297.16kJ热量 |
下列关于反应能量变化的相关常识论断错误的是
| A.吸热反应不一定都要加热才反应 |
| B.化学键的断裂和形成是化学反应中能量变化的根源 |
| C.选择燃料只需考虑燃料热值大小 |
| D.若反应物的总键能大于生成物的总键能则反应为吸热反应 |
今有如下三个热化学方程式:
H2(g)+ O2(g)=H2O(g);△H=" a" kJ/mol
O2(g)=H2O(g);△H=" a" kJ/mol
H2(g)+ O2(g)=H2O(l);△H=" b" kJ/mol
O2(g)=H2O(l);△H=" b" kJ/mol
2H2(g)+ O2(g)=2H2O(l);△H=" c" kJ/mol
关于它们的下列表述,正确的是
| A.它们都是吸热反应 | B.a、b和c均为正值 |
| C.反应热的关系:a=b | D.反应热的关系:2b=c |
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1 mol产物的数据)。
根据上图回答下列问题:
(1)PCl3分解成P(s)和Cl2(g)的热化学方程式是__________________________________。
(2)P和Cl2分两步反应生成1 mol PCl5的△H1=_______________,与P和Cl2一步反应生成1 mol PCl5的△H2的关系是:△H2__________△H1(填“大于”、“小于”或“等于”)。
已知石墨在高温、高压及催化剂存在的条件下能转化为金刚石,该反应为吸热反应,由此可知
| A.石墨比金刚石稳定 | B.石墨总能量比等质量的金刚石高 |
| C.该变化属于物理变化 | D.该反应的焓变△H<0 |
碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示:
①H2(g) + I2(?) 2HI(g)+9.48kJ
2HI(g)+9.48kJ
②H2(g) + I2(?) 2HI(g)-26.48kJ
2HI(g)-26.48kJ
下列判断正确的是
| A.①中的I2为固态,②中的I2为气态 |
| B.②的反应物总能量比①的反应物总能量低 |
| C.①的产物比反应②的产物热稳定性更好 |
| D.1mol 固态碘升华时将吸热17kJ |