A、B、C、D、E、F六种中学化学中常见的物质,有转化关系(见图):
(1)若A、C、E皆为氧化物,且E为有毒气体,B、D、F皆为非金属单质,且D为气体。则A的结构式为 ,1molC中含有 个共价键。
(2)若A、C、E皆为氢化物,三者皆为极性分子,其中C的相对分子质量最小;D、E、F皆为氧化物,其中D、F为有毒气体。则:
①A、C、E沸点由高到低的顺序为 (填化学式);A、C、E三种气态氢化物稳定性最强的是 (填化学式)。
②B跟C反应生成E和F的化学方程式为 。③A跟D常温下反应可生成一种单质,化学方程式为  。
。
下图中的B~K分别代表有关反应的一种反应物或生成物,其中A、C、F、K是固体;E是常见的 气体单质而I是红棕色的气态氧化物。固态物质A加热后生成的气体混合物若通过碱石灰只剩余气体B,若通过浓硫酸则只剩余气体D。各物质间的转化关系如下图所示:
气体单质而I是红棕色的气态氧化物。固态物质A加热后生成的气体混合物若通过碱石灰只剩余气体B,若通过浓硫酸则只剩余气体D。各物质间的转化关系如下图所示:
请回答下列问题: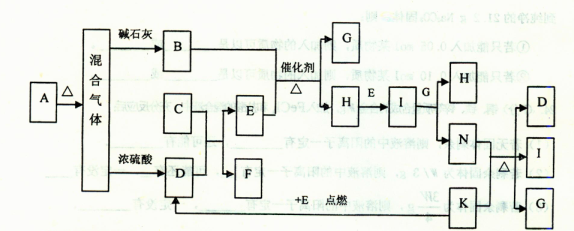
(1)写出实验室检验A物质中含有的阳离子的方法 。
(2)B与 E反应得到1mol H,则此时转移电子的物质的量为 mol。
E反应得到1mol H,则此时转移电子的物质的量为 mol。
(3)写出实验室制取B的化学方程式 。
(4)写出N的稀溶液与过量的铁粉反应的离子方程式 。
(5)若混合气体通过碱石灰得到的气体B与通过浓硫酸得到的气体D的物质的量之比是8:5,则用物质的量的关系表示此固体A的组成为 。
已知M是无色液体,C、H、D是有刺激性气味的气体,且D是单质,E为三原子非极性分子,②是工业上制取F的反应,J为漂白粉的有效成份。(部分反应条件未列出)
请回答下列问题:
(1)E、D、J的化学式分别是 、 、 ,G的电子式
(2)反应④的化学方程式
(3) 简述C的一种用途:
(4) A由三种元素组成,1 mol A与M反应可生成1 mol B和2 mol C,则A的化学式是
(5)漂白粉常用作消毒剂、杀菌剂、漂白剂等。漂白粉是一种混合物,漂白粉质量高低由"有效氯"(过量酸与漂白粉作用生成的氯气的质量与漂白粉的质量比)决定。漂白粉样品2.00克,加水研磨后,转入250毫升容量瓶内,用水稀释至刻度,摇匀后,取出25.0毫升,加入过量的KI溶液和过量的稀硫酸,静置。待漂白粉放出的氯气与KI完全反应后,用0.100摩/升的Na2S2O3标准溶液滴定反应中生成的碘。反应如下:2Na2S2O3+I2=Na2S4O6+2NaI滴定时用去Na2S2O3溶液20.0毫升。计算该漂白粉中有效氯的百分含量。
已知漂白粉与酸的反应为:Ca(ClO)2+CaCl2+2H2SO4=2CaSO4+2Cl2↑+2H2O
现有A、B、C、D、E、F六种物质的溶液,分别为NH3·H2O、NaHSO4、AlCl3、AgNO3、NaAlO2、NaOH中的一种,已知:
①将A溶液逐滴滴加到B溶液中至过量,先出现沉淀,后沉淀溶解;
②将C溶液逐滴滴加到D溶液中至过量,先出现沉淀,后沉淀溶解;
③将E溶液逐滴滴加到F溶液中至过量,先出现沉淀,后沉淀溶解;
④在①和③的反应中出现的沉淀是同一种物质;
⑤A、D、F三种溶液呈酸性。
请回答:
(1 )写出下列化学式:A ;D ;E 。
)写出下列化学式:A ;D ;E 。
(2)过量A溶液与B溶液反应的离子方程式为 ;
将C溶液逐滴滴加到F溶液中至过量,此过程中反应的离子方程式为
。
(3)若A、C的混合溶液呈中性,则该溶液中所有离子的浓度的 大小关系为
大小关系为
。
如下图所示的转化关系中,已知A是由短周期元素组成的酸式盐。通常状况下,D、E、F、Y、H为气体。G和K均为常见的强酸,D和X的分子中均含有10个电子。请回答下列问题: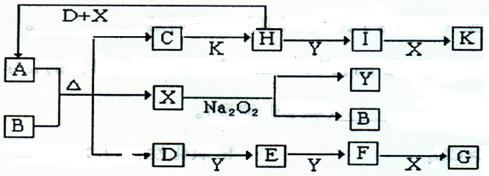
(1)B的电子式为 ,其中含有的化学键类型是 ;C的化学式是 。
(2)写出在加热条件下.A与足量的B溶液反应的离子方程式: 。
(3)写出D与Y在点燃条件下反应,生成X和一种单质的化学方程式: 。
(4)若G的稀溶液溶解了a mol Fe后(假设E是唯一的还原产物),溶液中两种金属阳离子的物质的量恰好相等,则被还原的G是 mol(用含a的代数式表示)。
(10分,每空2分)A、B、C、X均为中学化学常见的纯净物,它们之间有如下转化关系(副产物已略去)。 
(1)若X是空气中存在的强氧化性无色气体单质,则A可能是___________ (填序号)
(填序号)
a.C b.Al c.S d.Mg
(2)若X是日常生活中最常用的金 属单质,A是气体单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,X在气体A中燃烧产生棕黄色的烟。
属单质,A是气体单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,X在气体A中燃烧产生棕黄色的烟。
反应②的离子方程式为:
C溶液中加入NaOH溶液后产生的现象是
(3)若A在常温下为气态化合物,C是红棕色的气体,C与水反应后所得的浓溶液D与铜反应又生成C气体。则:反应①的化学方程式: ;
D的稀溶液与铜反应的离子方程式为:
X、Y、Z为三种常见 的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物。它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应)以下每空中填入一种即可)。
的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物。它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应)以下每空中填入一种即可)。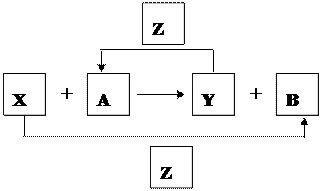
(1)当X、Y均为金属时,X的化学式为 ,Z为 (填名称)。
(2)当X为非金属且为气体,Y为金属且为紫红色时,X的化学式为 ____ ,
A的化学式为 。
(3)当X为金属、Y为非金属且为固体时,X与A反应的化学方程式 为
为
。
(4)当X、Y均为非金属 固体时,X与A反应的化学方程式为
固体时,X与A反应的化学方程式为
。
A、B、C、D均为中学常见物质,其中A为单质,B、C、D为化合物 ,并且存
,并且存 在如下转换关系:
在如下转换关系:
试回答下列问题:
(1)若B与C为氧化物,D为纯碱。
a.当A为非金属单质时,则反应③的化学方程式为 。
b.当A为金属单质时,则反应④中生成1mol纯碱转移电子数为 mol。
(2)若A为淡黄色非金属单质,B为气态氢化物,C为气态氧化物。 B与C反应中氧化剂与还 原剂的质量比为 。
原剂的质量比为 。
(3)若A为金属单质,B为氧化物,且反应①③均是与强碱溶液发生的反应,则反应①的离子方程式为 。
A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。
(1)若A为氯碱工业的产品,C为厨房中 的用品。
的用品。
①D的电子式是  。
。
②反应Ⅲ的离子方程式是 。
③氯碱工业制备A的化学方程式是 
 ,其中两种产物可与KI溶液反应制得一种化工原料,若消耗0.1 mol KI转移电子0.6 mol,则三种物质间反应的离子方程式是
,其中两种产物可与KI溶液反应制得一种化工原料,若消耗0.1 mol KI转移电子0.6 mol,则三种物质间反应的离子方程式是  。
。
(2)若A、D均为单质,且A为黄绿色气体 ,D元素的一种红棕色氧化物常用作颜料。
,D元素的一种红棕色氧化物常用作颜料。
①反应Ⅲ的离子方程式是 。
②B可作净水剂,其原理是  (用离子方程式表示)。在使用时发现B不能使酸性废水中的悬浮物沉降除去,其原因是 。
(用离子方程式表示)。在使用时发现B不能使酸性废水中的悬浮物沉降除去,其原因是 。
下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。已知:①反应C+G B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中E元素的质量分数为60%。
2F+D,F中E元素的质量分数为60%。
回答问题:
⑴①中反应的化学方程式为 ;
⑵化合物I的电子式为 ,它的空间结构是 ;
⑶1.6gG溶于盐酸,得到的溶液与铜粉完全反应,至少所需的铜粉的质量为 ,
⑷C与过量NaOH溶液反应的离子方程为 ,反应后的溶液与过量化合物I反应的离子方程式为 ;
⑸E在I中燃烧观察到的现象是 。
⑹G的化学式是 。
元素及其化合物的知识是“化学I”的重点内容。 A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如下图所示:

试写出符合下列条件的化学方程式:
(1)若物质A为氧化物: ;
(2)若A为金属单质,B为金属氧化物: ;
(3)若A为金属单质,B为非金属氧化物: ;
(4)若A和X均为非金属单质: ;
A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。
(1)Y元素在元素周期表中的位置 周期 族
(2)X的单质与A反应的化学方程式是 。
(3)若试剂1是NaOH溶液,X的单质与试剂1反应的离子方程式是 。
(4)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是 。
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示) 。
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成, 该反应的化学方程式是 。
该反应的化学方程式是 。
有A、B、C三种短周期元素在周期表中相对位置如下图:
| A |
|
|
|
| |
|
B |
C |
(1)A与C形成的液态化合物是常见的重要有机溶剂,则A、B、C三种元素最高价氧化物对应的水化物酸性由强到弱的顺序是: > > (用化学式表示)。
(2)X、Y为B、C两种元素形成的单质。标准状况下,X的密度为3.17g/L。Z是一种化合物,焰色反应呈紫色(透过钴玻璃),室温下0.1mol/LZ水溶液pH=13。X、Y、Z有如图转化关系:
①写出X与Z反应的离子 方程式: 。
方程式: 。
②已知丙能与稀硫酸反应生成使品红褪色的气体。丁的电子式 ,丁的水溶液pH 7(填“大于”“小于”或“等于”),其原因为
(用离子方程式表示)。
③将20mL0.5mol/L丙溶液逐滴加入20mL0.2mol/LKMnO4溶液(硫酸酸化)中,恰好褪色。写出反应的离子方程式 。
④写出X与水反应生成两种酸的电子式 , 。
有A、B、C、D、E、F、G、H等常见物质,已知有如下图转化关系,其中B、C 为常见非金属单质;F为常见金属单质;B在C中燃烧时,火焰呈苍白色;A和D的焰色反应为黄色。G和D溶液混和,产生红褐色沉淀。
(1)反应(1)中若生成0.1mol B,则转移的电子的物质的量为 。写出C与F反应的化学方程式 。(注明反应条件)
(2)图中所示的5个反应中属于氧化还原反应的有: 。(填写编号)
.下图每一方框中的字母代表一种反应物或生成物:
物质A跟B反应生成物质E、F和G;物质C跟D反应生成气体I,I中含有植物生长必须的元素之一,请填写下列空白:
(1)物质H的分子式是___________,气体I的分子式是____________
(2)写出电解饱和食盐水的化学方程式,并标出电子转移的方向和数目。
___________________________________________该反应中的 还原剂是___________
还原剂是___________
(3)反应①的化学方程式是_________________________________________。