有A、B、C、D、E、F、G、H等常见物质,已知有如下图转化关系,其中B、C 为常见非金属单质;F为常见金属单质;B在C中燃烧时,火焰呈苍白色;A和D的焰色反应为黄色。G和D溶液混和,产生红褐色沉淀。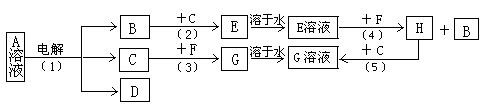
(1)反应(1)中若生成0.1mol B,则转移的电子的物质的量为 。写出C与F反应的化学方程式 。(注明反应条件)
(2)图中所示的5个反应中属于氧化还原反应的有: 。(填写编号)
有A、B、C、D、E、F、G、H等常见物质,已知有如下图转化关系,其中B、C 为常见非金属单质;F为常见金属单质;B在C中燃烧时,火焰呈苍白色;A和D的焰色反应为黄色。G和D溶液混和,产生红褐色沉淀。
(1)反应(1)中若生成0.1mol B,则转移的电子的物质的量为 。写出C与F反应的化学方程式 。(注明反应条件)
(2)图中所示的5个反应中属于氧化还原反应的有: 。(填写编号)