工业上制取铝的流程如下: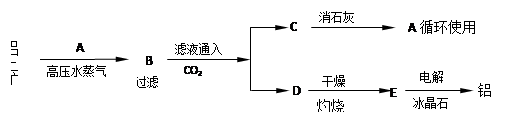
注:冰晶石的作用是使E在较低温度下熔化。
(1)试写出下列物质的化学式:
A ,B ,C ,D ,E 。
(2)在用此法制取铝时,分析铝土矿和赤泥(提取Al2O3之后的残渣)所得数据如下:
| |
Al2O3 |
Fe2O3 |
Na2O |
| 铝土矿 |
55% |
16% |
0% |
| 赤泥 |
15% |
48% |
8% |
试求制取1t Al2O3所需铝土矿和苛性钠的质量。(写过程)
(10分) 化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,这些废液必须经处理后才能排放。某化学实验室产生的废液中含有两种金属离子:Fe3+、Cu2+,化学小组设计了如下图所示的方案对废液进行处理,以回收金属,保护环境。
(1)废液经操作①得到的沉淀A中含有的金属单质是 ;
(2)写出操作①的反应离子方程式 ; 。
(3)在操作②中观察到的实验现象是 。
(4)操作③中发生主要反应的离子方程式为 。
NaCl是一种化工原料,可以制备一系列物质(见图)。下列说法正确的是( )
| A.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
| C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D.上图所示转化反应都是氧化还原反应 |
由短周期元素组成的甲、乙、丙、丁四种物质分别含有两种或两种以上元素,它们分子中质子总数均与氩原子的质子数相同,已知甲是气态氢化物,在水中分步电离出两种阴离子。下列推断合理的是( )
| A.某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应 |
| B.乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键 |
| C.丙中含有第2周期IV A族的元素,则丙一定是甲烷的同系物 |
| D.丁和甲含有某相同元素,且该元素在二者中的百分含量相同,则丁中一定含有-l价元素 |
NaCl是一种化工原料,可以制备一系列物质(如下右图所示)。下列说法正确的是
| A.石灰乳与Cl2的反应中Cl2既是氧化剂,又是还原剂 |
| B.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| C.常温下干燥Cl2能用钢瓶贮运,所以Cl2不与铁反应 |
| D.图中所示转化反应都是氧化还原反应 |
某新型无机非金属材料A,由两种非金属元素组成,其中所含元素的化合价为其最高正价或最低负价,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特征。A可由化合物B经下列反应制得:①B+NH3→C[C的化学式为Si(NH2)4];②C经隔绝空气高温分解得到A。为探究B的组成,进行了下图所示的转化实验,图中G、F、H均为难溶于水的物质,且为白色粉末,图中字母代表的均为中学化学常见的物质。
请回答下列问题:
(1)写出化合物B和化合物G的化学式________、________。
(2)A可能所属的晶体类型是________,在A晶体中,每个显正价原子周围结合的另一种原子的个数是________。
(3)写出反应②的离子方程式:_____________________________________________。
(4)写出C经隔绝空气高温分解得到A的化学方程式:_________________________________________________。
(5)分析反应③,你能得出的结论是________(合理即可)。
高锰酸钾是锰的重要化合物和常用的氧化剂,工业用软锰矿制备高锰酸钾的实验流程如下:
(1)上述流程中可以循环使用的物质有 (写化学式)
(2)从经济环保角度考虑,要完全反应b需要的试剂最好是 ,并写出相应的化学方程式 。
(3)高锰酸钾是氧化还原滴定分析时常用的一种试剂,在滴定操作时,应将高锰酸钾标准溶液盛放在 (填“酸式”或“碱式”)滴定管中,用酸性KMnO4溶液滴定硫酸亚铁晶体(FeSO4•7H2O)溶液, 写出滴定反应的离子方程式 。
(4)KMnO4、双氧水、活性炭常用于饮用水的处理,但三者在联合使用时必须有先后顺序。①氧化反应:H2O2 - 2e- → 2H+ + O2↑;还原反应:MnO4- + 5e- + 8H+ → Mn2+ + 4H2O
写出该氧化还原反应的化学方程式 。
②在处理饮用水时,活性炭应在高锰酸钾反应结束后投放,否则会发生KMnO4+ C+ H2O→MnO2 + X + K2CO3(未配平),其中X的化学式为 。
已知A是一种金属单质,B显淡黄色,其转化关系如图所示,则关于C的以下性质错误的是( )
| A.溶液呈碱性 |
| B.与澄清石灰水反应产生白色沉淀 |
| C.与足量盐酸反应放出气体 |
| D.受热易分解 |
中学常见物质A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去)。下列推断不正确的是( )
A.若D是一种强碱,则A、B、C均可与X反应生成D
B.若D为NaCl,且A可与C反应生成B,则E可能是CO2
C.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C
甲、乙、丙、丁分别是Al2(SO4)3、FeSO4、NaOH、BaCl2四种物质中的一种,若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加沉淀消失,丁滴入甲溶液时,无明显现象发生,据此可以推断丙物质是
| A.Al2(SO4)3 | B.NaOH |
| C.BaCl2 | D.FeSO4 |
下图中A~G均为中学化学中常见的物质,它们之间有如下转化关系。其中A是天然气的主要成分,B是一种能使带火星木条复燃的气体,C是一种能使澄清石灰石变浑浊的气体,E是一种淡黄色粉末状固体。(反应过程中某些产物已略去)
请回答问题:
(1)A的电子式为 。
(2)E的化学式为 。
(3)写出C转化为F的化学方程式 。
(4)写出G溶液中通入过量C的离子方程式 。
中学常见物质A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去)。下列推断不正确的是
A.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
B.若D是一种强碱,则A、B、C均可与X反应生成D
C.若D为NaCl,且A可与C反应生成B,则E可能是CO2
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C
A、B、C、X均为中学常见的纯净物,它们之间有如图转化关系(副产物已略去)。
回答下列问题:
(1)若X是强氧化性单质,则A不可能是________。
a.S b.N2 c.Na d.Mg e.Al
(2)若A、B、C为含金属元素的无机化合物,X为强电解质溶液,A溶液与C溶液反应生成B,则B的化学式为________,X的化学式可能为(写出不同类物质)________或________,反应①的离子方程式为________________________或________________________。
已知A、B、C是单质且C是绿色植物光合作用的产物之一,X、Y是化合物,它们之间的转化关系如图(反应条件略)。下列A、B间的对应关系,正确的是
A.A是铝,B是铁 B.A是碳,B是硅
C.A是氢气,B是铜 D.A是钠,B是氢气