足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4mol·mol-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
| A.60mL | B.45mL | C.30mL | D.75mL |
足量铜与一定量浓硝酸反应后过滤,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与3.36 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得溶液中加入1 mol/L NaOH溶液至Cu2+恰好完全沉淀,将沉淀过滤、洗涤、干燥、灼烧后得到黑色固体,则所得黑色固体的质量是( )
| A.12g | B.16g | C.24g | D.48g |
某固体混合物可能含有Al、(NH4)2SO4、MgCl2、AlCl3、FeCl2、NaCl中的一种或几种,现对该混合物做如下实验,所得现象和有关数据如图(气体体积已换算成标准状况下体积):下列说法不正确的是( )
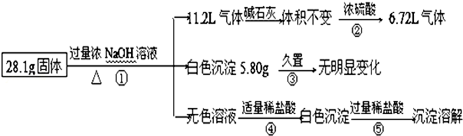
| A.混合物中一定不存在FeCl2和NaCl |
| B.反应④的离子方程式为:AlO2﹣+H++H2O=Al(OH)3↓ |
| C.混合物中一定含有Al、(NH4)2SO4、MgCl2三种物质,无法判断是否含有AlCl3 |
| D.白色沉淀5.80g是Mg(OH)2 |
m g铝镁合金与一定浓度的稀硝酸恰好完全反应(假定硝酸的还原产物只有NO),向反应后的混合溶液中滴加a mol/L NaOH溶液,当滴加到V mL时,得到沉淀质量恰好为最大值n g,则下列有关该实验的说法中错误的是
| A.沉淀中OH-的质量为(n-m)g |
| B.恰好溶解后溶液中的NO3-的物质的量为aVmol |
C.反应过程中转移的电子的物质的量为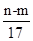 mol mol |
D.与合金反应的硝酸的物质的量为 mol mol |
已知反应:2NO2+2NaOH=NaNO3+NaNO2+H2O ;NO+NO2+2NaOH=2NaNO2+H2O。现有XmolNO2和YmolNO(X>Y)组成的混合气体,欲用m L含nmolNaOH的溶液吸收,使该混合气体全部转化成盐(NaNO3和NaNO2)进入溶液,则n的值至少是( )
| A.X/m mol | B.2X/3mol | C.(X+Y)mol | D.2(X+Y)/3mol |
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果不正确的是( )

| A.混合酸中NO3-物质的量为0.4mol |
| B.OA段产生的是NO,AB段的反应为: Fe+2Fe3+→3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.H2SO4浓度为5 mol·L-1 |
现取m克铝镁合金与一定浓度的稀硝酸恰好完全溶解(假定硝酸的还原产物只有NO),向反应后的混合溶液中滴加bmol/LNaOH溶液,当滴加到VmL时,得到沉淀质量恰好为最大值n克,则下列有关该实验的说法中正确的有( )
①沉淀中氢氧根的质量为(n-m)克
②恰好溶解后溶液中的NO3-离子的物质的量为 mol
mol
③反应过程中转移的电子数为 mol
mol
④生成标准状况下NO气体的体积为 L
L
⑤与合金反应反应的硝酸的物质的量为( +
+ )mol
)mol
| A.2项 | B.3项 | C.4项 | D.5项 |
将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO),向反应后的溶液中加入3mol/LNaOH溶液到沉淀完全,测得生成沉淀的质量比原合金的质量增加 5.1g.下列叙述不正确的是( )
| A.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol |
| B.参加反应的金属的总质量3.6g<m<9.6g |
| C.当生成的沉淀量达到最大时,消耗NaOH溶液的体积V=100mL |
| D.当金属全部溶解时收集到NO气体的体积在标况下为2.24L |
在1L浓度为0.2mol•L﹣1Fe(NO3)3和1.5mol•L﹣1H2SO4组成的混合溶液中加入39.2g铁粉使其充分反应.下列有关说法正确的是( )
| A.由于氧化性Fe3+>H+,故反应先不产生气体后产生气体 |
| B.反应后产生13.44LH2(标准状况) |
| C.反应后溶液中Fe2+和Fe3+物质的量之和为0.9mol |
| D.反应后溶液中Fe3+物质的量为0.8mol |
1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法中不正确的是( )
| A.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| B.该浓硝酸中HNO3的物质的量浓度是14.0mol/L |
| C.该合金中铜与镁的物质的量之比是2:1 |
| D.得到2.54g沉淀时,加入NaOH溶液的体积是600mL |
将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO)。向反应后的溶液中加人3 mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g。则下列叙述中不正确的是( )
| A.当生成的沉淀量达到最大时,消耗NaOH溶液的体积V≥100 mL |
| B.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol |
| C.参加反应的金属的总质量为9.6 g>m>3.6 g |
| D.当金属全部溶解时收集到NO气体的体积一定为2.24 L。 |
在一定浓度的浓硝酸中加入m克铜镁合金恰好完全溶解(假定硝酸的还原产物只有NO2),向反应后的混合溶液中滴加bmol/LNaOH溶液,当滴加到 v mL时,恰好完全反应,得到沉淀质量为n 克,则下列有关该实验的说法中正确的有( )
①沉淀中氢氧根的质量为(n-m)克 ②恰好溶解后溶液中的NO3-离子的物质的量为bv mol
③反应过程中转移的电子数为 mol ④生成NO2气体的体积为
mol ④生成NO2气体的体积为 L
L
⑤与合金反应反应的硝酸的物质的量为 mol
mol
| A.①②③④⑤ | B.①③④⑤ | C.①③⑤ | D.①②③⑤ |
含1 mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物与铁粉物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关判断正确的是
| A.曲线a表示Fe2+,曲线b表示Fe3+ |
| B.P点时总反应的离子方程式可表示为5Fe+16H++NO3-==3Fe2++2Fe3++4NO↑+8H2O |
| C.n2=0.25 |
| D.n3:n1=3:2 |
在标准状况下,将aLNH3完全溶于1L水得到VmL氨水,溶液的密度为ρg∙cm-3,溶质的质量分数为ω,溶质的物质的量浓度为cmol/L。下列叙述中正确的是
① ②
② ③
③ ④
④ ⑤上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω
⑤上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω
| A.①②④ | B.②③④ | C.②④ | D.②③⑤ |
足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入6 mol·L—1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
| A.60 mL | B.50 mL | C.30 mL | D.15 mL |