某金属单质跟一定浓度的硝酸反应,假定只产生单一的还原产物,当参加反应的单质与被还原HNO3的物质的量之比为2∶1时,还原产物可能是
| A.N2O | B.NO |
| C.NO2 | D.N2 |
下列有关计算的分析不正确的是
| A.在反应3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O中,当有1mol铜被氧化时,被还原的硝酸为2/3mol |
| B.将amolFeS放入含3amolH2SO4的浓硫酸中,充分反应后,氧化、还原产物分别是Fe3+、S和SO2,则放出的SO2气体少于1.5a mol |
| C.室温时,在容积为aml的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入bmlO2,则管内液面又继续上升,测得试管内最后剩余气体为cml,且该气体不能支持燃烧。则a、b、c的关系为a=4b+3c |
| D.某溶液100ml,其中含硫酸0.03mol,硝酸0.04mol,若在该溶液中投入1.92 g铜粉微热,反应后放出一氧化氮气体约为0.015mol |
在15.2g铁和铜组成的合金中加入过量的硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的NaOH溶液,生成25.4g沉淀,则下列表示气体X组成的选项中合理的是 ( )
| A.0.3mol NO、0.1mol NO2 | B.0.3mol NO2 |
| C.0.6mol NO | D.0.3mol NO2、0.1mol NO |
将4.48g Fe溶于1L 0.2mol·L-1的稀硫酸,再加入50mL 0.4mo1·L-1KNO3溶液后,其中的Fe2+全部转化成Fe3+,NO3-无剩余,生成一种氮氧化物NYOX。则该氮氧化物的化学式是
| A.N2O | B.NO | C.N2O3 | D.NO2 |
将铜和铁的混合粉末投入到稀硝酸中,待反应完全后铁有剩余,则溶液中一定有
| A.Fe(NO3)2 | B.Cu(NO3)2 | C.Fe(NO3)3 | D.HNO3 |
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68LO2(标况下)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
| A.60ml | B.45ml | C.30ml | D.15ml |
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
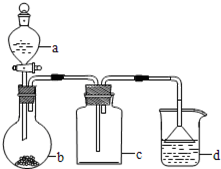
| 选项 |
a中的物质 |
b中的物质 |
c中的物质 |
d中的物质 |
| A |
浓氨水 |
CaO |
NH3 |
H2O |
| B |
浓硫酸 |
Na2SO3 |
SO2 |
NaOH溶液 |
| C |
稀硝酸 |
Cu |
NO2 |
H2O |
| D |
浓盐酸 |
MnO2 |
Cl2 |
NaOH溶液 |
将2.56 g Cu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体(NOx)的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12 L(标准状况),则反应中消耗HNO3的物质的量为
| A.0.05 mol | B.0.13 mol | C.1.05 mol | D.1 mol |
向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入150mL4mol/L的稀硝酸恰好使混合物完全溶解,放出2.24LNO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的H2在加热条件下还原相同质量的混合物,所得到的铁的物质的量为
| A.0.21mol | B.0.25mol | C.0.3mol | D.0.35mol |
某无色混合气体中可能含有Cl2、O2、HCl、SO2、NO2、NO、NH3中的两种或多种。将此无色混合气体通过品红溶液后,品红溶液褪色;把剩余气体排入空气中,气体很快变为红棕色,该无色混合气体遇浓盐酸未看到明显现象。下列关于原混合气体成分的判断正确的是
| A.一定有SO2、NH3和NO | B.一定有NO和HCl |
| C.可能有Cl2和O2 | D.一定没有Cl2、NO2、NH3和O2 |
将过量铁粉放入100mL3mol/L的HNO3溶液中,假设还原产物只有NO且HNO3完全反应,则参加反应的Fe的质量为
| A.2.8g | B.6.3g | C.5.6g | D.11.2g |
2007年诺贝尔化学奖授予善于做“表面文章”的德国科学家格哈德·埃特尔。他的成就之一是证实了气体在固体催化剂表面进行的反应,开创了表面化学的方法论。在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示。下列说法正确的是 
| A.NO2是该过程的最终产物 |
| B.NO和O2必须在催化剂表面才能反应 |
| C.汽车尾气的主要污染成分是CO2和NO |
D.该催化转化的总反应方程式为:2NO +O2 +4CO 4CO2+N2 4CO2+N2 |
往100mL pH=0的硫酸和硝酸混合液中投入3.84g铜粉,微热使反应充分完成后,生成一氧化氮气体448mL(标准状况)。则反应前的混合溶液中含硝酸的物质的量为
| A.0.02mol | B.0.08mol | C.0.10mol | D.0.16mol |
将O2和NH3的混合气体448mL通过加热的三氧化二铬(催化剂),充分反应后,再通过足量的水,最终收集到44.8mL氧气。原混合气体中O2的体积可能是(假设氨全部被氧化;体体积均已换算成标准状况)( ) 已知:NO在O2存在时与水可按4NO+3O2+2H2O=4HNO3反应进行
A.23l.5mL, B.268.8mL C.287.5mL D,313.6mL