已知25℃时,几种弱酸的电离常数如下,下列说法不正确的是( )
| 弱酸的化学式 |
CH3COOH |
HClO |
H2CO3 |
| 电离常数 |
1.8×10-5 |
2.9×10-8 |
K1= 4.3×10-7 K2=5.6×10-11 |
A.等物质的量浓度的各溶液①c(CH3COONa)②c(NaClO) ③c(NaHCO3)④c(Na2CO3)
pH关系为:④>②>③>①
B.少量CO2通入次氯酸钠溶液中:CO2+ClO-+H2O=HClO +HCO3-
C.新制氯水中Cl2+H2O HCl+HClO为适当增大HClO 的浓度,可加入少量固体NaHCO3
HCl+HClO为适当增大HClO 的浓度,可加入少量固体NaHCO3
D.某浓度的NaClO溶液的pH=d,则其中由水电离出的c(H+)=10-dmol/L
常温下,下列溶液中各微粒的物质的量浓度关系正确的是( )
| A.浓度为0.1 mol/L CH3COOH与0.1 mol/L CH3COONa混合后溶液呈弱酸性,则c(CH3COOH>c(Na+)>c(CH3COO-) |
| B.相同条件下,pH=5的①NH4Cl溶液、②CH3COOH溶液、③稀盐酸三种溶液中由水电离出的c(H+):①>②>③ |
| C.NaHCO3溶液:c(OH-)-c(H+)=c((HCO3-)+2c(H2CO3) |
| D.等物质的量浓度的NaClO、NaHCO3混合溶液中:c(HClO) + c(ClO-)= c(HCO3-) + c(H2CO3) + c(CO32-) |
现有物质的量浓度均为 0.1 mol·L - 1 的四种溶液各25mL:①氨水 ②NH4Cl 溶液
③Na2CO3溶液 ④NaHCO3溶液,下列说法正确的是:
| A.4种溶液pH的大小顺序:①>④>③>② |
| B.①、②混合后pH>7,则混合溶液中c(NH4+)<c(NH3·H2O) |
| C.①、②中分别加入25mL 0.1 mol·L – 1盐酸后,溶液中c(NH4+):①>② |
| D.③、④中分别加入12.5mL 0.1 mol·L – 1NaOH溶液后,两溶液中离子种类相同 |
某二元酸(化学式H2B)在水中的电离方程式为H2B=H++HB-;HB- H++B2-,则在0.1 mol/L 的Na2B溶液中,下列粒子浓度关系式正确的是( )
H++B2-,则在0.1 mol/L 的Na2B溶液中,下列粒子浓度关系式正确的是( )
A.c(B2-)+c(HB-)+c(H2B)=0.1 mol/L
B.c(Na+)+c(H+)=c(OH-)+c(HB-)+c(B2-)
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)=2c(B2-)+c(HB-)
下列叙述正确的是
| A.NaHCO3溶液中存在: c(OH-) =c(H+)+c(H2CO3) |
| B.某二元弱酸强碱盐NaHA溶液中存在:c(Na+)+c(H+)=c(A2-)+c(HA-)+c(OH-) |
| C.CH3COONa和NaCl混合溶液中存在:c(Na+)=c(CH3COO-)+c(Cl-) |
| D.常温下,10mL 0.02mol·L-1 HCl溶液与10mL 0.01mol·L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=7 |
物质的量浓度相同时,下列既能跟NaOH溶液反应,又能跟盐酸反应的溶液中,pH最大的是
| A.Na2CO3溶液 | B.NH4HCO3溶液 | C.NaHSO4溶液 | D.NaHSO3溶液 |
下列溶液中粒子的物质的量浓度关系正确的是:
| A.0.1 mol·L - 1 NaHC2O4溶液与0.1 mol·L – 1KOH溶液等体积混合,所得溶液中: c(Na+)>c(K+) >c(C2O42-) >c(OH-) >c(HC2O4-) |
| B.20mL 0.1 mol·L - 1NH4Cl溶液与10mL 0.1 mol·L - 1NaOH溶液混合后溶液呈碱性,所得溶液中:c(Cl-)>c(NH4+) >c(Na+)>c(OH-)>c(H+) |
| C.常温下,pH=2的HF溶液与pH=12的氢氧化钠溶液等体积混合,所得溶液中: c(Na+)+ c(OH-) >c(H+)+ c(F-) |
| D.0.1 mol·L – 1 NH3·H2O溶液与0.1 mol·L – 1 HNO3溶液等体积混合,所得溶液中: |
c(H+) >c(OH-) + c(NH3·H2O)
常温下,0.2 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合后(忽略混合前后溶液体积的变化),溶液的pH<7,则下列有关此溶液的叙述正确的是( )
| A.溶液中由水电离产生的H+浓度为1×10-7 mol/L |
| B.c(CH3COO-)+c(CH3COOH)-c(Na+)=0.05 mol/L |
| C.溶液中CH3COOH的电离程度小于CH3COONa的水解程度 |
| D.溶液中离子浓度的大小关系为:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A.0.1mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| B.0.1mol/L NH4Cl溶液:c(NH4+)=c(Cl-) |
| C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.在25℃时,将pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合后:c(H+)=c(CH3COO-)+c(OH-) |
下列叙述不正确的是
A.0.1 mol•L-1氨水中,c(OH-)>c(NH4+)
B.等体积等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
C.在0.1 mol•L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
D.0.1 mol•L-1某二元弱酸强碱盐Na2A溶液中,c(Na+)=2c(A2-)+2c(HA-)+2c(H2A)
已知0.1 mol•L-1的二元酸H2A溶液的pH=4,则下列说法中正确的是
A.在Na2A、NaHA两溶液中,离子种类不相同
B.物质的量浓度相等的Na2A、NaHA两溶液的pH相大小为前者小于后者
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-)
设某氨水的pH=X,某盐酸的pH=Y,已知X+Y=14,且X > 11将上述两溶液分别取等体积充分混合,混合液中各离子的浓度由大到小的顺序是( )
A.c(Cl-)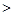 c(NH4+) c(NH4+)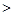 c(H+) c(H+)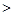 c(OH-) c(OH-) |
B.c(NH4+)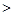 c(Cl-) c(Cl-)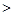 c(H+) c(H+)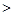 c(OH-) c(OH-) |
C.c(NH4+)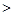 c(Cl-) c(Cl-) 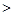 c(OH-) c(OH-)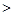 c(H+) c(H+) |
D.c(Cl-)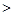 c(NH4+) c(NH4+)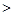 c(OH-) c(OH-)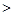 c(H+) c(H+) |
常温下,下列溶液的pH或微粒的物质的量浓度关系不正确的是 ( )
| A.pH=5.2的CH3COOH与CH3COONa混合溶液中,c(Na+)<c(CH3COO-) |
| B.在滴加酚酞溶液的氨水中,加入NH4Cl溶液恰好无色,则此时溶液的pH﹤7 |
| C.Na2CO3溶液中,c(OH-)-c(H+)= c(HCO3-)+2 c(H2CO3) |
| D.pH=2的一元酸溶液与pH=12的NaOH溶液等体积混合,则溶液的pH一定不大于7 |
下列有关说法正确的是( )
| A.常温下,0.1 mol/L Na2S溶液中存在:c(OH-) = c(H+) + c(HS-) + c(H2S) |
| B.常温下,pH为1的0.1 mol/L HA溶液与0.1 mol/L NaOH溶液恰好完全反应时,溶液中一定存在: c (Na+) = c(A-) > c(OH-) = c(H+) |
| C.常温下,pH=7的CH3COONa和CH3COOH混合溶液中c(Na+)="0.1" mol/L: c(Na+) = c(CH3COOH) > c(CH3COO-) > c(H+) = c(OH-) |
D.常温下,将0.1 mol/L CH3COOH溶液加水稀释,当溶液的pH从3.0升到4.0时,溶液中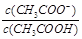 的值减小到原来的 的值减小到原来的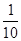 |