F2是氧化性最强的非金属单质,在加热条件下,物质的量相等的F2和烧碱完全反应,生成NaF、H2O和另一种气体,该气体是下列中的()
| A.H2 | B.HF | C.O2 | D.OF2 |
在FeCl3和CuCl2混合液中,加入过量的铁粉,充分反应后,溶液中的金属离子是( )
A Fe2+ B Fe3+ 和Fe2+ C Cu2+ 和Fe2+ D Cu2+
根据下列反应:(1)2Fe3++2I-=2Fe2++I2(2)Br2+2Fe2+=2Br-+2Fe3+判断离子的还原性由强到弱的顺序是( )
| A.Br->Fe2+>I- | B.I->Fe2+>Br-- |
| C.Br->I->Fe2+ | D.Fe2+>I->Br- |
已知下述三个实验均能发生化学反应
①将铁钉放入硫酸铜溶液中 ②向硫酸亚铁溶液中滴入几滴双氧水
③将铜丝放入氯化铁溶液中
下列判断正确的是( )
| A.实验①中铁钉做氧化剂 |
| B.实验②中Fe2+具有还原性 |
| C.实验③中发生的是置换反应 |
| D.上述实验证明氧化性Fe3+>Fe2+>Cu2+ |
下列反应中,水作氧化剂的是 ( )
| A.2Na2O2+2H2O===4NaOH+O2↑ | B.C+H2OCO+H2 |
| C.Cl2+H2O===HCl+HClO | D.2F2+2H2O===4HF+O2 |
实验室常利用以下反应制取少量氮气:NaNO2+NH4Cl=NaCl+N2↑+2H2O关于该反应的下列说法正确的是( )
| A.NaNO2是氧化剂 |
| B.N2既是氧化剂,又是还原剂 |
| C.NH4Cl中的氮元素被还原 |
| D.每生成1mol N2时,转移电子的物质的量为6mol |
氧化还原是常见的反应类型,根据信息回答以下问题: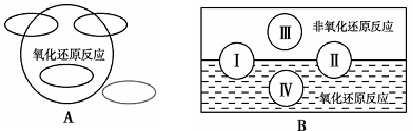
1、A图是“四种基本反应类型与氧化还原反应的关系”图,请在A图中用阴影部分表示反应:Cl2 + 2NaBr —→ 2NaCl + Br2 所属的区域。
2、“四种基本反应类型与氧化还原反应的关系”也可用B图表达。①其中Ⅰ为化合反应,则Ⅱ为 反应。②写出一个有水生成的符合反应类型Ⅲ的化学方程式: 。③写出一个有水参加的符合反应类型Ⅳ的化学方程式 ,
其中水作为 剂。(填氧化剂、还原剂等)
3、用“单线桥”分析下列氧化还原反应的电子转移方向及数目,并填空。
(1)2HClO —光→ 2HCl + O2↑ 氧化产物 被还原的元素
(2)2NaCl + 2H2O —电解→ 2NaOH + Cl2↑ + H2↑
4、有F-、Cl-、I-、Br2、I2五种粒子,其中氧化性最强的是 ,还原性最强的是 ,用离子方程式表示氧化性强弱的事实:
。
下列叙述中,正确的是( )
| A.含金属元素的离子不一定都是阳离子 |
| B.在氧化还原反应中,非金属单质一定做氧化剂 |
| C.元素从化合态变为游离态时,该元素一定被还原 |
| D.原子失电子数越多还原性越强 |
据以下判断Cu2+、Fe2+、Fe3+的氧化性,从强到弱的顺序为( )
① Fe + CuCl2 = FeCl2 + Cu
② 2FeCl3 + Cu = 2FeCl2 + CuCl2
| A.Fe3+>Fe2+>Cu2+ | B.Fe3+>Cu2+>Fe2+ |
| C.Fe2+>Cu2+>Fe3+ | D.Cu2+>Fe2+>Fe3+ |
已知:Ni +CuSO4=NiSO4+Cu Cu+2AgNO3=Cu(NO3)2+2Ag 则下列判断正确的是
| A.还原性:Ni>Cu>Ag | B.氧化性:Ni2+ > Cu2+ >Ag+ |
| C.还原性:Ni<Cu<Ag | D.氧化性:Ni2+ < Cu2+ <Ag+ |
已知下面反应可以发生: Br2 + 2NaI ="2" NaBr + I2
Cl2+ 2NaBr =" 2NaCl" + Br2则关于Cl2, Br2 ,I2氧化性强弱说法中,正确的是( )
| A.氧化性: I2>Br2 >Cl2 | B.氧化性: Br2 >I2>Cl2 |
| C.氧化性: Cl2 > Br2 > I2 | D.氧化性: I2>Cl2 >Br2 |
下列关于硫酸性质的描述中,正确的是
| A.浓H2SO4有氧化性,稀H2SO4无氧化性 |
| B.由于浓H2SO4具有吸水性,故可用来与蔗糖反应做“黑面包”实验 |
| C.稀H2SO4与铁、铝反应,浓H2SO4在常温下不与铁、铝反应 |
| D.浓硫酸与Cu的反应中有少量黑色固体生成,可能是CuO |
已知有如下反应:①2BrO3-+Cl2==Br2+2ClO3-,②2FeCl2+Cl2==2FeCl3 ③ClO3-+5Cl-+6H+==3Cl2+3H2O,④2FeCl3+2KI==2FeCl2+2KCl+I2,下列各微粒氧化能力由强到弱的顺序正确的是 ( )
| A.ClO3- > BrO3- > Cl2 > Fe3+ > I2 | B.BrO3- > Cl 2> ClO3- > I2 > Fe3+ |
| C.BrO3- > ClO3- > Cl2 > Fe3+ > I2 | D.BrO3- > ClO3- > Fe3+ > Cl2 >I2 |