 从铝土矿(主要成分是
从铝土矿(主要成分是 ,含
,含 、
、 等杂质)中提取
等杂质)中提取 的两种方法如下:
的两种方法如下:


 请回答下列问题:
请回答下列问题:
 (1)方法甲中,固体A的化学式____________
(1)方法甲中,固体A的化学式____________
 (2)方法乙加入烧碱后生成SiO32-的离子方程式为___________________
(2)方法乙加入烧碱后生成SiO32-的离子方程式为___________________
 (3)简述检验滤液B中含
(3)简述检验滤液B中含 的方法______________________________
的方法______________________________
 (4)滤液K中溶质的主要成份是 (填化学式),写出该物质的一种用途 。
(4)滤液K中溶质的主要成份是 (填化学式),写出该物质的一种用途 。
根据如图所示的化学反应框图解题。
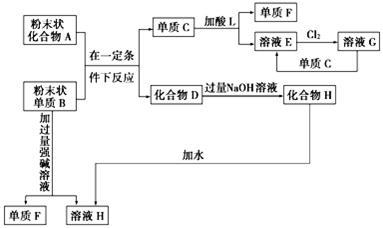
(1)单质F是 ,溶液H中所含的主要离子是 。
(2)写出下列反应的化学方程式:
C+L→F+E: ,
B→F+H: 。
(3)写出下列反应的离子方程式:
E+Cl2→G: ,
D→H: 。
下图中A~H均为中学化学中常见的物质,它们之间有如下转化关系。其中A、C均为金属单质,C与水反应生成D和最轻的气体,D、H的焰色反应均呈黄色,在通常状况下E(氢氧化物)跟NaOH或盐酸均可发生复分解反应。(反应过程中生成的水及其他产物已略去)

请回答以下问题:
(1)A是(填名称) ; H是(填化学式) 。
(2)请写出反应C→D的化学方程式,并用单线桥或双线桥法标明该反应中电子转移的方向和数 目: 。
(3)Na2O2也可以生成D,写出其反应的化学方式: 。
(4)写出E转化为G的离子方程式: 。
(5)写出D转化为F的化学方程式: 。
X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如下图所示(水及部分产物已略去)。

(1)若X为常见金属单质,W是某强酸的稀溶液。写出Y与X反应生成Z的化学方程式为________________。
(2)若X为非金属单质,W是空气的主要成分之一。实验室制取气体Y的离子方程式为__________________。
(3)若X、Y均为铝盐,X的水溶液显酸性。请写出Z转化为Y的离子方程式:_ _____。
(4)若X为一元强碱,常温下W为无色气味的气态氧化物。请写出Z转化为Y的化学方程式:__ _____。
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)

(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有有色气体生成,则C的电子式为 ,反应④的化学方程式为: 。
(2)若A为常见的金属单质,D、F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是 ,用电子式表示B分子的形成过程 。
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为 ,分子E的结构式为 。
某强酸性溶液X,可能含有Al3+、Ba2+、NH4+ 、Fe2+、Fe3+、CO32-、SO42-、SiO32-、NO3-中的一种或几种离子,取该溶液进行实验,其现象及转化如下图。反应过程中有一种气体是红棕色。请回答下列问题:

(1)由强酸性条件即可判断溶液X中一定不存在的离子有 。
(2)溶液X中,关于N03-的判断一定正确的是 。
a.一定有 b.一定没有 c.可能有
(3)产生气体A的离子方程式为 。
(4)转化⑥发生反应的现象为 。
(5)转化④中产生H的离子方程式为 。
(6)若转化③中,D、H20、02三种物质恰好发生化合反应生成E,则反应中D与02的物质的量之比为____________。
(7)对不能确定是否存在的离子,可以另取X溶液,加入下列溶液中的一种,根据现象即可判断,该试剂最好是 。
①NaOH溶液,②KSCN溶液,③石蕊试剂,④pH试纸,⑤KMn04溶液,⑥氯水和KSCN的混合溶液
下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,F是海水中含有盐的主要成分,J为D、G反应产物形成的水溶液。

请回答下列问题:
(1)B的化学式为 。
(2)反应②在工业上通常称之为 工业。
(3)写出反应③的离子方程式 。
(4)写出反应④的化学方程式 。
已知X为Fe2O3和CuO的混合物,且氧化性强弱顺序:Fe3+>Cu2+>H+>Fe2+。X 样品可发生如图所示的转化关系:
(1)写出步骤③可能发生反应的离子方程式(共有3个)__________。
(2)若溶液E中只有一种金属离子,则一定是_________________________;
若溶液E中含有两种金属离子,则一定是______________________。
(3)若D固体是纯净物,该固体是________(填化学式)。
(4)印刷电路板是由高分子材料和铜箔复合而成的,可用FeCl3溶液作“腐蚀剂”刻制印刷电路板,该过程发生反应的离子方程式_________________________。
已知有以下物质相互转化,已知,A是世界上用量最大的金属单质:

试回答:(1)写出E的化学式 ,F的化学式
(2)写出由E转变成F的化学方程式 。颜色变化_________________
(3)向G溶液加入A的有关离子反应方程式________________________________。
(4)写出G溶液中阳离子的鉴别方法(一种,要求写现象)____________________
(5)写出B溶液转变成G溶液的方程式_______________________________
有A、B、C、D、E、F六种化合物,它们之间的反应关系如下所示:
① A+B → C+E ② C+NaOH → 蓝色沉淀D + F
③ D A+E ④ F+Ba(NO3)2 → 白色沉淀 + NaNO3
回答下列问题:
(1)写出它们的化学式:A ,E 。
(2)写出①②③④反应的化学方程式,属于离子反应的只写离子方程式。
① ; ② ;
③ ; ④ 。
如下图所示下列反应皆为常见反应(部分反应条件省略),其中A、B、F均为单质,其余物质均为化合物且D常温下为液态,H是84消毒液的有效成分。

(1)写出G的化学式______________F化学式_______________
(2)写出C与D反应的化学方程式__________________________________
(3)写出CO2通入H溶液的离子方程式______________________________
(4)消耗7.8g C可以生产标准状况下的B________________L
有一包白色固体粉末,其中可能含有NaCl、Ba(NO3)2、CuSO4、Na2CO3中的一种或几种,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色:
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液加入足量AgNO3溶液,产生白色沉淀.
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是_________,一定不含有的物质是_________,可能含有的物质是_________.(写化学式)
(2)写出各步变化的离子方程式.
①__________________;
②__________________。
已知四种强电解质溶液,分别含有下列阴、阳离子中的各一种,并且互不重复:Ba2+、H+、K+、NH4+、CO32-、Cl-、OH-、SO42-.将这4种溶液分别标记为A、B、C、D,其相互关系如下:
①向A或D中滴入C,均生成白色沉淀;
②A和B混合加热产生的气体能被D吸收;
③A和D反应生成的气体能被B吸收。
请回答下列问题:
(1)A、B、C、D中电解质的化学式:
A________、B、________C、________D________。
(2)若将B和D混合,反应的离子方程式为______________________。
(3)若将③中生成的气体用过量的B吸收,则反应的离子方程式为___________________。
有一包白色粉末,其中可能含有Ba(NO3)2、CaCl2、K2CO3,现做以下实验:
(1)将部分粉末加水中,振荡,有白色沉淀生成;
(2)向(1)的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;
(3)取少量(2)的溶液滴入AgNO3溶液,有白色沉淀生成。
根据上述实验现象,判断原白色粉末中肯定含有什么物质,可能含有什么物质,写出各步反应的离子方程式。肯定有____________;可能含有____________
离子方程式:
(1)____________________________
(2)____________________________
(3)____________________________
实验室中有四种化合物A、B、C、D,分别可能由以下两组离子中的各一种所构成:(离子可以重复使用)
阳离子组:Na+、Mg2+、Cu2+、Ba2+
阴离子组:OH-、Cl-、SO42-、CO32-
(1)A不溶于水,也不溶于酸
(2)B溶于水后,若与阳离子组中的另一种离子反应,有A生成;若与阴离子组中的另两种离子反应,均产生白色浑浊现象
(3)C溶于水后,与阳离子组中的任一种离子都不反应;将一根铁棒置于C溶液中,一段时间后铁棒增重
(4)D的水溶液显碱性,与阴离子组中的另两种离子反应,分别生成A和一种白色沉淀
回答下列问题:
(1) 写出下列物质的化学式: B________, C________, D________,
(2) 检验A中阴离子的方法为_____________________________。
(3) 写出B与D反应的离子方程式:________________________。
(4) 将铁棒置于C溶液中一段时间后,铁棒增重0.8g,计算有_____mol Fe参与反应。(要求书写计算步骤)