下列有关结构和性质的说法中,正确的是 ( )
| A.Si、P、S、 Cl元素的单质与氢气化合越来越剧烈 |
| B.元素原子的最外层电子数越多,元素的金属性越强 |
| C.第三周期主族元素从左到右的最高价含氧酸酸性减弱 |
| D.元素中期表共有18列,第8列属于第ⅧB族、第17列属于第ⅫA族 |
现有H 、C、O、Na 四种元素,按要求完成下列各小题。
(1)写出Na+的结构示意图____________________。
(2)已知O元素的一种核素,其中子数比电子数多2,该核素可表示为:___________。
(3)A、B、C是由上述一种或几种元素组成的物质,且能实现A + B → C + H2O的转化,按要求写出化学反应方程式,并注明反应条件。
①酸性氧化物 → 盐:_________________________
②属于氧化还原反应:_________________________
(4)任写一种含上述三种元素 的非电解质________________;(填名称)上述四种元素组成的物质X可用于治疗胃酸(盐酸)过多,相应的化学方程式为_____________________________。
下列有关 、
、 、
、 说法错误的是
说法错误的是
| A.是碳元素的三种同位素 |
| B.是不同的原子 |
| C.化学性质完全不同 |
| D.其中的 14C和14N所含的质量数相等 |
已知aAm+与bBn-具有相同的核外电子排布,则下列关系正确的是
| A.a=b+m+n | B.a=b-m+n | C.a=b+m-n | D.a=b-m-n |
下列比较、归纳一定正确的是
| A.酸性:HClO4>H2CO3>H2SiO3 |
| B.稳定性:HF<H2O<NH3 |
| C.离子半径:Na+>F-> Al3+ |
| D.沸点:HI>HBr>HF |
下列微粒和基团中,碳原子不满足最外层为8电子结构的是
| A.一氯甲烷(CH3Cl) |
| B.甲基(-CH3) |
| C.碳负离子(CH3—) |
| D.乙烯(C2H4) |
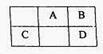
短周期元素A、B、C、D在周期表中的位置如图所示:B、D最外层电子数之和为12。回答下列问题:
(1)与元素B、D处于同一主族的第2-5周期元素单质分别与H2反应生成1 mol气态氢化物对应的热量变化如下,其中能表示该主族第4周期元素的单质生成1 mol气态氢化物所对应的热量变化是_______(选填字母编号)。
a.吸收99.7kJ b.吸收29.7kJ c.放出20.6kJ d.放出241.8 kJ
(2)DB2通过下列工艺流程可制化工业原料H2DB4和清洁能源H2。

①查得:
| 化学键 |
H-H |
Br-Br |
H-Br |
| 键能(kJ/mol) |
436 |
194 |
362 |
试写出通常条件下电解槽中发生总反应的热化学方程式: 。
②根据资料:
| 化学式 |
Ag2SO4 |
AgBr |
| 溶解度(g) |
0.796 |
8.4×10-6 |
为检验分离器的分离效果,取分离后的H2DB4溶液于试管,向其中逐滴加入AgNO3溶液至充分反应,若观察到 ,证明分离效果较好。
③在原电池中,负极发生的反应式为 。
④在电解过程中,电解槽阴极附近溶液pH (填“变大”、“变小”或“不变”)。
⑤将该工艺流程用总反应的化学方程式表示为: 。该生产工艺的优点有 (答一点即可)。
(3)溴及其化合物广泛应用于医药、农药、纤维、塑料阻燃剂等,回答下列问题:海水提溴过程中,向浓缩的海水中通入________,将其中的Br-氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为________________ 。
X、Y、Z、W、Q都是短周期元素,其中X原子的最外层电子数是内层电子数的3倍;X与Z同族,Y与Z同周期,Q原子的电子总数等于其电子层数的3倍,W与X、Y既不同族也不同周期且W不为稀有气体元素;X、Y、Z三种元素的族序数之和为16。下列说法正确的是( )
| A.Q与W能形成10电子, 不能形成14电子、18电子分子 |
| B.Y的最高价氧化物对应水化物的化学式只能表示为H4YO4 |
| C.Y、Z、Q分别与X化合,只能形成AB2型化合物 |
| D.X、Z、W三种元素形成的两种钠盐溶液发生化学反应生成的气体可使品红溶液褪色 |
I.元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3 :4,且M原子的质子数是Y原子的2倍;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,请回答下列问题:
(1)写出Y、Z、N按原子个数之比1 :1:1形成的化合物的电子式_______________。
(2)写出由X、Y、Z、M、N中某些原子形成的18电子分子和18电子离子发生氧化还原反应的离子方程式:_________________。
(3)上图表示由上述两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:________________。
Ⅱ.A、B、C、D是原子序数均小于20的四种元素。A与B同主族,且能形成BA2、BA3的型分子。B、C、D所形成的简单离子电子层结构相同,且B、C、D离子半径依次减小。请回答下列问题:
(4)D元素在元素周期表中的位置是_____。B与D所形成的化合物的化学键类型为______。
(5)将C单质的水溶液滴加到B与D所形成化合物的水溶液中,其反应的离子方程式为_。
元素X~Z是元素周期表中4种主族元素,其性质或结构信息如下表,有关下列元素的描述错误的是
| 元素 |
X |
Y |
W |
Z |
| 相关信息 |
用硫酸处理海藻灰时,可得通常状况下为紫黑色的固体,其制剂可用来消毒 |
工业上在冰晶石存在的条件下,用电解法制取其单质 |
最早是在用氯气处理提取食盐后的盐水母液中发现的,被称作“海洋元素” |
原子的电子总数是最外层电子数的6倍 |
A.实验室可在海藻灰的浸出液中滴加双氧水来制取元素X的单质
B.元素X、Y的单质充分混合后滴加少量水,可看到大量紫色蒸汽生成,说明该反应会放出大量的热
C.元素X的气态氢化物的沸点高于元素W的气态氢化物的沸点
D.元素Z是一种较活泼的金属元素,可用铝热法从Z的氧化物中制备Z的单质
X、Y、Z三种短周期元素,原子半径的大小关系为:r(y)>r(x)>r(z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生下图所示变化,其中B和C均为10电子分子。下列说法不正确的是
| A.X元素位于ⅥA |
| B.A不能溶解于B中 |
| C.B的沸点高于C的沸点 |
| D.A和C不可能发生氧化还原反应 |
主族元素X在周期表中位于第二周期,其原子最外层电子数大于4,元素Y在周期表中位于第三周期,其原子最外层电子数小于4,有关其说法正确的是( )
| A.X所形成的单质都是双原子分子 |
| B.原子半径X>Y |
| C.X、Y能形成的阴、阳离子数之比为1:2离子化合物,其一定为碱性氧化物 |
| D.由X、Y组成的某化合物与水反应能生成一种强碱和一种弱碱,其简单离子半径:X>Y |
下列有关说法正确的是
| A.原子最外层电子数为2的元素一定是ⅡA元素 |
| B.第三周期元素对应的离子半径从左往右依次减小 |
| C.第ⅦA族元素从上到下,其氢化物的酸性逐渐减弱 |
| D.第三周期的主族元素的最高正价一定等于其最外层电子数 |
有A、B、C、D、E、F六种短周期元素,其原子序数依次增大,A的单质分子内不含中子,B的某种同素异形体可以用于制作铅笔芯,C是形成氧化物种类最多的元素, D2—与E2+具有相同的电子层结构,F原子的最外层电子数与其电子层数相等。
(1)A单质的结构式 ;E2+的离子结构示意图 。
(2)C、D、E、F四种元素简单离子的离子半径由大到小的排列顺序为(用离子符号表示) 。
(3)由A和C两种元素可形成多种分子,其中有一种A、C原子个数比为3:1的分子,其电子式为 ;另一种分子中其原子个数比为2:1,已知在101kPa时,32.0g该液态化合物在氧气中燃烧,其中一种生成物为C元素形成的单质,放出热量624kJ (25℃时),写出该热化学方程式 。
(4)某抗酸药物只含A、B、D、E、F五种元素,取一定量该抗酸药进行如下实验:

过量试剂a是 ;通过计算可知该抗酸药的化学式为 。