甲、乙两物质的溶解度曲线如图所示.下列叙述中正确的是
| A.t1℃时,在100 g水中放入60 g甲,其溶质的质量分数为37.5% |
| B.t1℃时,甲和乙的饱和溶液的物质的量浓度一定相等 |
| C.t2℃时,甲和乙的饱和溶液中溶质的质量分数一定相等 |
| D.t2℃ 时,分别在100 g水中各溶解20 g甲、乙,同时降低温度,甲先达到饱和 |
用下列方法来制备胶体,能够得到胶体的是
| A.将等体积、等物质的量浓度的BaCl2溶液和硫酸相混合并振荡 |
| B.把1 mL饱和三氯化铁溶液逐滴加入到20 mL温水中,边加边振荡,并加热到沸腾 |
| C.把1 mL饱和三氯化铁溶液一次性加入到20 mL沸水中,并加以搅拌 |
| D.把1 mL饱和三氯化铁溶液逐滴加入到20 mL沸水中,边加边振荡 |
硫酸钠是一种重要的化工原料,其溶解度曲线如图所示.下列说法正确的是
| A.硫酸钠的溶解度随温度升高而增大 |
| B.30℃时硫酸钠饱和溶液的质量分数为40% |
| C.40℃时硫酸钠的溶解度约为50g |
| D.60℃时硫酸钠饱和溶液降温后一定饱和 |
下图为X物质的溶解度曲线。M、N两点分别表示X物质溶于100g水中所形成的两种溶液。下列做法不能实现M、N间的相互转化的是(X从溶液中析出时不带结晶水) 
| A.从M→N:先将M降温到t1过滤后再将其升温至t3 |
| B.从M→N:先将M恒温蒸发掉适量的水再升温到t3 |
| C.从N→M:先向N中加入适量固体X再降温到t2 |
| D.从N→M:先将N降温到t2再加入适量固体X |
下列推断合理的是
| A.明矾[KAl(SO4)2·12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
| B.向50mL 18mol/L 硫酸中加入足量铜片并加热,被还原硫酸的物质的量是0.45mol |
| C.浓硫酸溅到皮肤上,立即用碳酸钠稀溶液冲洗 |
| D.将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水色后加热也能恢复原色 |
实验是化学学习的基础。下列实验叙述正确的是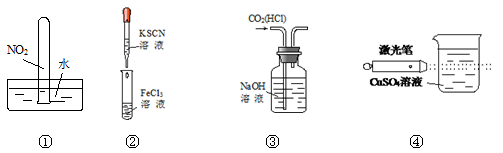
| A.实验①试管最终会充满水 |
| B.实验②试管中溶液变为血红色 |
| C.可用实验③装置除去CO2气体中含有的少量HCl杂质 |
| D.实验④检验硫酸铜溶液 |
下列有关化学用语的书写或表述正确的是
A.用铜做电极电解饱和食盐水:2NaCl+2H2O 2NaOH+H2↑+Cl2↓ 2NaOH+H2↑+Cl2↓ |
| B.稀醋酸与0.1 mol/LNaOH溶液反应:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol |
| C.切开的金属Na暴露在空气中,光亮表面逐渐变暗4Na+O2=2Na2O |
D.向沸腾的蒸馏水中逐滴加入1.0 mol/LFeCl3溶液,至液体呈透明的红褐色Fe3++3H2O Fe(OH)3↓+ 3 H+ Fe(OH)3↓+ 3 H+ |
储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,反应中的反应物和生成物有C、CO2、H2SO4、KCr2O7、Cr2(SO4)2、H2O七种物质。
(1)若将碳纳米颗粒分散到一定溶剂中,形成稳定的分散系,所具的性质有
①丁达尔效应;②加入饱和(NH4)2SO4溶液产生聚沉;③可通过半透膜。
(2)请用上述物质填空,配平化学方程式,并标出电子转移的方向和数目(
C+ + H2SO4→ K2SO4+ + Cr2(SO4)3+ H2O
(3)将标准状况下4.48 L产生的气体通入适量的NaOH溶液中充分反应后,溶液中生成盐的质量为19.0g。
(I)若要使生成的盐的质量变为25.2 g,则应继续向溶液中通入该气体 g。
(Ⅱ)向生成的19.0 g的盐溶液中加入一定量某物质,充分反应后,减压低温蒸发得到纯净的21.2 g Na2CO3固体。则:
①若只能加入0.05 mol某物质,则加入的物质可以是 或 。
②若只能加入0.10 mol某物质,则加入的物质可以是 或 。
在t ℃时,向x g KNO3不饱和溶液中加入a g KNO3或蒸发掉b g水,恢复到t ℃,溶液均达到饱和,据此,下列推论不正确的是( )
A.在t ℃时,KNO3的溶解度为 g g |
B.若原溶液中溶质的质量分数为 ,则x=2b ,则x=2b |
C.在t ℃时,所配的KNO3溶液中溶质的质量分数为w≤ % % |
| D.若将原溶液蒸发掉2b g水,恢复到原温度析出2a g KNO3 |