下列水溶液中的各组离子因为发生氧化还原反应而不能大量共存的是
| A.Na+、Ba2+、Cl、SO42- | B.Ca2+、HCO3、C1、K+ |
| C.MnO4、K+、I、H+ | D.H+、Cl、Na+、CO32 |
下列离子方程式中书写正确的是
| A.铝与盐酸反应 Al + H+ ==Al3++H2↑ |
| B.硫酸铜与Ba(OH)2溶液反应 Cu2++ 2OH-="=" Cu(OH)2↓ |
| C.铁与FeCl3溶液反应 Fe + Fe3+="=" 2Fe2+ |
| D.硝酸银溶液与氯化钠溶液反应 Ag+ + Cl-="=" AgCl↓ |
在含有Fe3+、Fe2+、Al3+、NH4+的稀溶液中加入足量的Na2O2固体,充分反应后,再加入过量的稀盐酸,反应完全后,离子数目几乎没有变化的是
| A.Fe3+ | B.Fe2+ | C.Al3+ | D.NH4+ |
下列反应的离子方程式书写正确的是
| A.钠和冷水反应 Na+2H2O=Na++2OH+H2↑ |
| B.金属铝溶于氢氧化钠溶液 Al+2OH=AlO2+H2 |
| C.金属铝溶于盐酸中:2Al+6H+=2Al3++3H2↑ |
| D.铁跟稀硫酸反应:Fe+2H+=Fe2++H2 |
下列离子方程式书写正确的是
| A.铝粉投入到NaOH溶液中:2Al+2OH-══ 2AlO2-+H2↑ |
| B.AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓ |
C.三氯化铁溶液中加入铁粉: |
| D.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl- |
将Fe、Cu、FeCl2、FeCl3、CuCl2盛于同一容器中充分反应,如Fe有剩余,则容器中只能有的金属或金属离子是
| A.Cu、Fe3+ | B.Fe2+、Fe3+ | C.Cu、Cu2+、Fe | D.Cu、Fe2+、Fe |
下列离子在溶液中能大量共存的是
A. |
B. |
| C.Fe2+ H+Na+NO3- | D. |
下列各组离子在溶液中可以大量共存,且加入氨水后也不产生沉淀的是
| A.Na+、Ba2+、Cl-、SO42- | B.K+、AlO2-、NO3-、OH- |
| C.K+、NH4+、Al3+、SO42- | D.H+、Cl-、CH3COO-、NO3- |
下列离子方程式书写错误的是:
| A.铝粉投入到NaOH溶液中:2Al+2OH-=2AlO2-+H2↑ |
| B.Al(OH)3溶于NaOH溶液中:Al(OH)3+OH-=AlO2-+2H2O |
| C.Ca(OH)2溶液中通入足量的CO2:CO2+OH—= HCO3— |
| D.Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-=2AlO2-+H2O |
下列离子方程式,错误的是
| A.钠投入水中:Na+H2O══ Na++OH-+H2↑ |
| B.碳酸钙与盐酸反应:CaCO3+2H+══ Ca2++CO2↑+H2O |
| C.钠投入硫酸铜溶液中:2Na+Cu2+══ Cu+2Na+ |
| D.Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++HCO3-+OH-══ CaCO3↓+H2O |
下列反应的离子方程式正确的是
| A.铝片跟氢氧化钠溶液反应:Al+2OH-=AlO2-+H2↑ |
| B.硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓ |
| C.碳酸钙跟醋酸反应:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |
| D.铜片跟稀硝酸反应:Cu+NO3-+4H+=Cu2++NO↑+2H2O |
某化合物有碳、氢、氧三种元素组成,其红外光谱图有C-H键、O-H键、C-O键的振动吸收,该有机物的相对分子质量是60,则该有机物的结构简式是 ( )
| A.CH3CH2OCH3 | B.CH3CH(OH)CH3 |
| C.CH3CH2CH2OH | D.CH3CH2CHO |
下列哪个选项属于碳链异构 ( )
| A.CH3CH2 CH2CH3和CH3CH(CH3)2 | B.CH2=C(CH3)2和CH3CH=CHCH3 |
| C.CH3CH2OH和CH3OCH3 | D.CH3CH2 CH2COOH 和CH3COOCH2 CH2 |
下列一定属于分离、提纯液态有机物的操作的是
| A.蒸馏 | B.蒸发 | C.重结晶 | D.萃取 |
同分异构体现象在有机化学中是非常普遍的,下列有机物互为同分异构体的是( )
①CH2=CHCH3 ②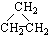 ③CH3CH2CH3 ④HC
③CH3CH2CH3 ④HC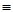 CCH3 ⑤
CCH3 ⑤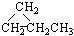 ⑥CH3CH=CHCH3
⑥CH3CH=CHCH3
| A.①和② | B.①和③ | C.①和④ | D.⑤和⑥ |