镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:
Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2由此可知,该电池充电时在阳极上发生反应的是( )
Cd(OH)2+2Ni(OH)2由此可知,该电池充电时在阳极上发生反应的是( )
| A.Ni(OH)2 | B.Cd(OH)2 | C.Cd | D.NiOOH |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O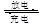 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
| A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
| B.充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O |
| C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化 |
| D.放电时正极附近溶液的碱性增强 |
锌银电池的负极是Zn,正极是Ag2O,以苛性钠溶液为电解质,电池放电时的总反应为Zn+Ag2O+H2O==Zn(OH)2 + 2Ag,下列判断正确的是( )
| A.放电时,OH-向负极方向移动 |
| B.放电时,正极反应式为Zn+2OH--2e-===ZnO+H2O |
| C.充电时,Zn发生氧化反应 |
| D.充电时, 阴极附近PH 减小 |
中国首个空间实验室——“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),它是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,a、b、c、d均为Pt电极。下列说法正确的是( )

A.B区的OH-通过隔膜向a电极移动,A区pH增大
B.图中右管中的OH-通过隔膜向c电极移动,d电极上发生还原反应
C.c是正极,电极上的电极反应为:2H++2e-=H2↑
D.当有1mol电子转移时,b电极产生气体Y的体积为11.2L
氨气是一种重要的化工产品,是生产铵盐、尿素等的原料.工业合成氨的反应如下:
N2(g)+3H2(g) 2NH3(g)△H=-92.4kJ/mol。
2NH3(g)△H=-92.4kJ/mol。
(1)实验室中常用来制备氨气的化学方程式为 。
(2)已知H2(g)的燃烧热为285.8kJ•mol-1,写出NH3(g)在纯氧中燃烧生成无毒、无害物质的热化学方程式 _。
(3)25℃时,将a mol (NH4)2SO4溶于水,向该溶液中滴加V L稀氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将__________________(填“正向”、“不”或“逆向”)移动,所滴加稀氨水的物质的量浓度为_____________mol•L-1(25℃时,NH3•H2O的电离平衡常数Kb≈2×10-5)。
(4)工业上常用CO2和NH3通过如下反应合成尿素[CO(NH2)2 ]:CO2(g)+2NH3(g) CO(NH2)2(l)+H2O(g)△H<0,t℃时,向容积恒定为2L的密闭容器中加入0.10mol CO2和0.40mol NH3,70min开始达到平衡。反应中CO2(g)的物质的量随时间变化如下表所示:
CO(NH2)2(l)+H2O(g)△H<0,t℃时,向容积恒定为2L的密闭容器中加入0.10mol CO2和0.40mol NH3,70min开始达到平衡。反应中CO2(g)的物质的量随时间变化如下表所示:
| 时间/min |
0 |
30 |
70 |
80 |
100 |
| n(CO2)/mol |
0.10 |
0.060 |
0.040 |
0.040 |
0.040 |
①20min时v正(CO2)_________80min时v逆(H2O)(填“>”、“=”或“<”)。在t℃时,该反应的平衡常数K= 。
②在100min时,保持其它条件不变,再向容器中充入0.050mol CO2和0.20mol NH3,重新建立平衡后CO2的转化率与原平衡相比将_________(填“增大”、“不变”或“减小”)。
③根据表中数据在图甲中绘制出在t℃下NH3的转化率随时间变化的图象;保持其它条件不变,则(t+10)℃下正确的图象可能是 (填图甲中的“A”或“B”)。
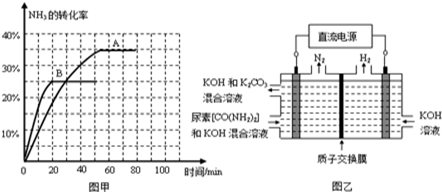
④图乙所示装置(阴、阳极均为惰性电极)可用于电解尿素[CO(NH2)2]的碱性溶液制取氢气。该装置中阳极的电极反应式为______ ,若两极共收集到气体22.4L(标况),则消耗的尿素为______g(忽略气体的溶解)。
以葡萄糖为燃料的微生物燃料电池示意图如图所示。
关于该电池的叙述正确的是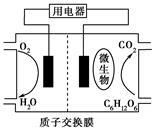
| A.该电池能够在高温下工作 |
| B.电池的负极反应为: C6H12O6+6H2O-24e-=6CO2↑+24H+ |
| C.放电过程中,H+从正极区向负极区迁移 |
D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体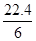 L L |
CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标。
(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H="-890.3" kJ·mol-1
CO(g)+H2O (g)=CO2(g)+H2 (g) △H="2.8" kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H="-566.0" kJ·mol-1
反应CO2(g)+CH4(g) 2CO(g)+2H2(g) 的△H= 。
2CO(g)+2H2(g) 的△H= 。
(2)为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验: 在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g)△H=" -" 49.0kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g)△H=" -" 49.0kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。

①从反应开始到平衡,氢气的平均反应速率
v(H2)= mol/(L·min)
②该反应的平衡常数表达式为 ,升高温度,平衡常数的数值将 (填“增大”、“减小”或“不变”)。
③下列措施中能使n(CH3OH)/n(CO2)增大的是 。
| A.升高温度 |
| B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离 |
| D.再充入1molCO2和3molH2 |
④在25℃、101kPa下,1g液态甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为________________________。
⑤我们常用的一种甲醇燃料电池,是以甲醇与氧气的反应为原理设计的,其电解质溶液是KOH溶液。写出该电池负极的电极反应式__________________________。
2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200oC左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2=2CO2 +3H2O,电池示意如图,下列说法不正确的是
| A.电池工作时,1mol乙醇被氧化时就有6mol电子转移 |
| B.a极为电池的负极 |
| C.电池工作时电流由b极沿导线经灯泡再到a极 |
| D.电池正极的电极反应为:4H+ + O2 + 4e—=2H2O |
氢气是一种清洁能源,氢气的制取是氢能源利用领域的研究热点;氢气也是重要的化工原料。
(1)纳米级的Cu2O可作为太阳光分解水的催化剂.一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气发生反应:
2H2O(g) 2H2(g)+O2(g)△H=+484kJ•mol﹣1,不同时段产生O2的量见下表:
2H2(g)+O2(g)△H=+484kJ•mol﹣1,不同时段产生O2的量见下表:
| 时间/min |
20 |
40 |
60 |
80 |
| n(O2)/mol |
0.0010 |
0.0016 |
0.0020 |
0.0020 |
上述反应过程中能量转化形式为光能转化为 能,达平衡过程中至少需要吸收光能为 kJ(保留三位小数)。
(2)氢气是合成氨工业的原料,合成塔中每产生2mol NH3,放出92.2kJ热量.已知:

则1mol N﹣H键断裂吸收的能量约等于 。
(3)已知:2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJ/mol
N2(g)+2O2(g)═2NO2(g)△H=+67.7kJ/mol
则H2还原NO2生成水蒸气和氮气反应的热化学方程式是 。
(4)氢镍电池是近年开发出来的可充电电池,它可以取代会产生污染的铜镍电池。氢镍电池的总反应式是 H2+2NiO(OH)  2Ni(OH)2。请由总反应式回答:
2Ni(OH)2。请由总反应式回答:
1.电解质溶液应该是 (选填酸溶液、碱溶液),
②.电池放电时,负极反应式为 ,
3.外电路中每通过0.2NA个电子时,H2的质量理论上减小 g,
4.电池工作时,电子由 极通过外电路流向 极(选填正、负)。
下列叙述不正确的是
| A.太阳能蓄电池只是将太阳能直接转化为电能的装置 |
| B.燃料电池是将化学能直接转化为电能的装置,所以能量利用率高 |
| C.碱性Zn-Mn干电池比酸性Zn-Mn干电池耐用,且不易漏液 |
| D.手机上用的锂离子电池属于二次电池 |
纸电池是一种有广泛应用的“软电池”,右图这种碱性纸电池采用薄层纸片作为载体和传导体,纸的两面分别附着锌和二氧化锰。下列有关该纸电池说法不合理的是
| A.Zn为负极,进行氧化反应 |
| B.电池工作时,电子由MnO2流向Zn |
| C.正极反应:MnO2+e-+H2O=MnO(OH)+OH- |
| D.电池总反应:Zn+2MnO2+2H2O=Zn(OH)2+2MnO(OH) |
科学家开发出一种新型锂—氧电池,其能量密度极高,效率达90%以上。电池中添加碘化锂(LiI)和微量水,工作原理如图所示,总反应为:O2+4LiI+2H2O 2I2+4LiOH
2I2+4LiOH
对于该电池的下列说法不正确的是
| A.放电时负极上I-被氧化 |
| B.充电时Li+从阳极区移向阴极区 |
| C.充电时阴极反应为LiOH+e-==Li+OH- |
| D.放电时正极反应为O2+2H2O+4Li++4e-==4LiOH |
由NO2、O2、熔融盐NaNO3组成的燃料电池如图所示,在使在过程中石墨I电极反应生成一种氧化物Y,下列有关说法正确的是( )

| A.石墨I极为正极,石墨II极为负极 |
| B.Y的化学式可能为NO |
| C.石墨I极的电极反应式为NO2+NO3――e-═N2O5 |
| D.石墨II极上发生氧化反应 |
已知电池的比能量是参与电极反应的单位质量的电极材料放出电能的大小。有关下述两种电池说法正确的是( )

锂离子电池的总反应为:LixC+Li1-xCoO2 C+LiCoO2
C+LiCoO2
锂硫电池的总反应为:2Li+S Li2S
Li2S
| A.锂离子电池放电时,Li+向负极迁移 |
| B.锂硫电池充电时,锂电极发生还原反应 |
| C.理论上两种电池的比能量相同 |
| D.右图表示用锂离子电池给锂硫电池充电 |