下列做法不利于保护金属资源的是
| A.采取各种有效防锈措施避免金属锈蚀 |
| B.国家加大开采矿物的力度,并鼓励私人到处开采 |
| C.用塑料代替钢和其他合金制造管道和机器部件 |
| D.回收利用铝制饮料罐 |
保护金属资源的有效途径是
①防止金属腐蚀
②回收利用废旧金属
③禁止生产易造成金属腐蚀的化工产品
④合理有效地开采矿物
⑤寻找金属的代用品
| A.①②③ | B.①②③④⑤ | C.②④⑤ | D.①②④⑤ |
金属资源是不可再生的资源,保护金属资源是我们刻不容缓的职责,下列有关叙述不正确的是
| A.大力开采矿物以保障金属材料的供用 |
| B.提高废旧金属的回收利用率 |
| C.在金属制品上刷漆、涂油等防止金属腐蚀 |
| D.用特种塑料代替金属制造机器的零部件 |
为保护金属资源下列做法不可行的是
| A.在金属表面涂油漆防止金属锈蚀 |
| B.回收利用废旧金属 |
| C.利用优质塑料制品代替金属 |
| D.禁止开采金属矿藏 |
在日常生活中,下列做法科学的是( )
| A.为了防止海产品腐烂变质,用甲醛水溶液浸泡海产品 |
| B.用蒸馏的方法降低水的硬度 |
| C.用炉具清洁剂除去热水瓶内的水垢 |
| D.为防止被雨水淋湿的自行车生锈,先用干布擦净,再用带油的布擦 |
下列对课本中相关实验的分析不正确的是
| A.电解水实验能说明水由氢、氧两种元素组成 |
| B.探究铁在空气中生锈的条件实验说明铁生锈时一定要有氧气和水参加 |
| C.黄豆与芝麻混合的实验能说明分子之间有空隙 |
| D.二氧化碳灭火实验能说明二氧化碳不助燃、不可燃、密度大于空气 |
钢铁产业是我国的支柱产业之一,选择优质炼铁原料十分重要。甲、乙两组同学对某钢铁厂所购进的赤铁矿粉中主要成分Fe2O3的含量进行测定。(假设每步反应均能完全进行,赤铁矿粉中的杂质性质稳定,既不溶于水也不参与反应)
(1)甲组同学称取一定质量的赤铁矿粉,采用如图装置进行实验。
①装置A中发生反应的化学方程式是 。
②为充分吸收反应生成的CO2,装置B中应盛放的试剂是浓 溶液。
③可以通过下面不同的方法计算赤铁矿粉中Fe2O3的含量。
方法一:称量反应前后装置A的总质量,计算出Fe2O3的含量。
方法二:称量 ,得出反应生成的CO2的质量,计算出Fe2O3的含量。
(2)乙组同学称取等质量的赤铁矿粉放入烧杯中,向烧杯中加入过量的稀硫酸充分反应, (填一个操作名称)后立即称量。根据称量的数据计算出Fe2O3的含量。
(3)甲、乙两组同学通过相互比较后对各自的实验方案进行评价。
世界每年因锈蚀而损失的金属数量巨大,防止金属锈蚀已成为科学研究中的重大问题。下列有关金属锈蚀与保护措施中不正确的是( )
| A.铁锈蚀的实质是铁与空气中的氧气、水蒸气等发生了化学变化 |
| B.同样的铁制品在海南比在兰州更易锈蚀 |
| C.在铁制品表面刷油漆可以防止铁锈蚀 |
| D.铝的抗腐蚀性能比铁强,生活中用钢丝球洗刷铝锅 |
下列说法不符合事实的是( )
| A.钢铁生锈是缓慢氧化 |
| B.铁在氧气中燃烧生成四氧化三铁 |
| C.铁锈的主要成分是四氧化三铁 |
| D.及时擦干被雨水淋湿的自行车可防止自行车生锈 |
如图是探究铁锈蚀条件的装置。调节L端与R端的液面使其高度一致,塞紧木塞,一周后观察。下列推断错误的是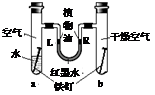
| A.b管中铁钉无明显锈蚀 |
| B.L端与R端液面高度仍然保持一致 |
| C.该实验说明铁锈蚀与空气、水有关 |
| D.若将a管中的水改为食盐水能加快铁的锈蚀 |
请回答下列有关金属的问题。
(1)铝是活泼金属,为什么通常铝锅却很耐腐蚀?
(2)铁在空气中生锈的原因是铁跟 发生了反应。
(3)A、B、C三种金属固体,将A和B浸入稀硫酸中,B溶解并产生氢气,A无变化;将A和C浸入硝酸银溶液中,A表面有银析出而C无变化。
①判断A、B、C和银四种金属的活动性由强到弱的顺序 。
②具体确定一种A后,写出A与硝酸银溶液反应的化学方程式。
在日常生活中,下列做法不正确的是( )
| A.装食品用的聚乙烯塑料袋可用加热的方法封口 |
| B.用食盐水去除铁锅内的铁锈 |
| C.乡村井水浑浊时,向其中加明矾可以净水 |
| D.被蚊虫叮咬后涂肥皂水可以止痒 |
下列有关实验现象描述正确的是
| A.打开浓盐酸瓶塞,可看到大量白烟 |
| B.硫在空气中燃烧,产生明亮的蓝紫色火焰 |
| C.氨水中滴入紫色石蕊试液后,溶液变红色 |
| D.铁钉长时间暴露在潮湿的空气中,表面会生成铁锈 |
铁制品在通常情况下很易生锈,制造时往往在铁制品表面电镀一层铜起防锈作用。下列说法正确的是( )
| A.镀铜铁制品不可以在弱酸性条件下使用 |
| B.镀铜铁制容器可盛硝酸银溶液 |
| C.镀铜铁制品不易生锈的原因之一是使铁隔绝了空气 |
| D.镀铜铁制品是一种合金 |