下图是六种物质的相互转化关系,已知E是固体单质,六种物质均含有E元素。
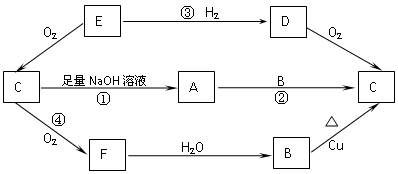
(1)写出各物质的化学式: B ;E ;F ;
(2)写出反应①的离子方程式________________________________________
(3)写出反应④的化学方程式_________________________________________
(4)写出B→C反应的化学方程式
下图是六种物质的相互转化关系,已知E是固体单质,六种物质均含有E元素。

(1)写出各物质的化学式: B ;E ;F ;
(2)写出反应①的离子方程式________________________________________
(3)写出反应④的化学方程式_________________________________________
(4)写出B→C反应的化学方程式