已知某实验室用水煤气合成甘(乙)氨酸的流程如下: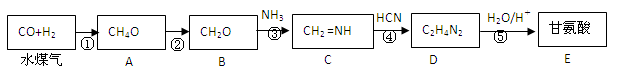
已知: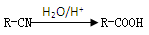 反应④属于加成反应。回答:
反应④属于加成反应。回答:
(1)写出A → B的化学方程式: 。指出其反应类型 。
(2)比较沸点高低:A B 主要原因是: 。
(3)写出C → D的化学方程式: 。
(4)任写一种甘氨酸的同分异构体的结构简式: 。
2分子甘氨酸形成一种二肽的结构简式: 。
已知某实验室用水煤气合成甘(乙)氨酸的流程如下:
已知: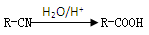 反应④属于加成反应。回答:
反应④属于加成反应。回答:
(1)写出A → B的化学方程式: 。指出其反应类型 。
(2)比较沸点高低:A B 主要原因是: 。
(3)写出C → D的化学方程式: 。
(4)任写一种甘氨酸的同分异构体的结构简式: 。
2分子甘氨酸形成一种二肽的结构简式: 。