化学来源于生活,又服务于生活。请用所学的化学知识回答下列问题:
(1)食醋是生活中常用的调味品,食醋中醋酸的化学式为 。
(2)臭氧主要分布在距地面10~50千米的高空,它能吸收大部分紫外线,保护地球生物,臭氧的化学式为 。
(3)铁在潮湿的空气中易生锈,铁生锈过程中生成了FeO(OH),该化合物中铁的化合价为 价。
(4)在新冠疫情期间,采用喷洒次氯酸钠(NaClO)对环境进行消毒,其原因是次氯酸钠与空气中的CO2和H2O反应生成了有强氧化性的次氯酸,则次氯酸的化学式为 。
(5)发生森林火灾时,在大火蔓延路线前砍掉一片树木,形成隔离带,其灭火原理是 。
学习小组同学用如图装置进行实验。打开分液漏斗的活塞,将NaOH浓溶液加入锥形瓶A中,关闭活塞,打开弹簧夹,观察到A中产生白色沉淀,烧杯B中液面降低。
(1)写出CO2与NaOH溶液发生反应的化学方程式: 。
(2)若X是一种碱,其化学式可能是 (只写一种)。
(3)学习小组同学用的X是CaCl2,实验结束后,同学们又分别做了以下三组实验:
①取少量A中溶液,测其pH,pH>7
②取少量A中溶液,向其中加入CaCl2溶液,无明显现象,再测其pH,pH>7
③取少量A中溶液,测其pH,pH>7,再向其中加入K2CO3溶液,产生白色沉淀
查阅资料可知CaCl2溶液呈中性。
以上三组实验事实中,能说明A中溶液一定含有NaOH的是 (填序号)。

根据下面NaNO3在不同温度时的溶解度表回答问题。(忽略溶解时的热量变化)
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
溶解度/g |
80.8 |
87.6 |
94.9 |
103 |
113 |
124 |
136 |
149 |
(1)20℃时,将90g NaNO3固体加入盛有100g水的烧杯中,充分搅拌后,得到溶液的质量为 g。给烧杯加热,使溶液温度升至40℃时,溶液中溶质与溶剂的质量比为 。
(2)80℃时,将249g NaNO3饱和溶液降温至 时,溶液质量变为224g。
(3)50℃时,将200g溶质质量分数为50%的NaNO3溶液改为该温度下的饱和溶液,至少应向溶液中再加入 g NaNO3固体。
金属的发现与使用历史体现了人们对其性质的认识和科技发展的水平。
(1)2021年3月,三星堆遗址再次出土的文物中,黄金面具残片最为引人瞩目,其历经三千年依旧金光灿灿,这是因为金的化学性质非常 。
(2)唐宋时期流行的“湿法炼铜”的原理是铁和硫酸铜溶液的反应,该反应的化学方程式为 。
(3)《周礼•考工记》中有关于将铜、锡以不同比例熔合制成功能各异的青铜器的记载。将铜片和锡片分别伸入稀盐酸中,锡片表面有气泡生成而铜片没有,说明金属活动性锡
(填“>”或“<”)铜。
我国嫦娥五号月球探测器成功将月球上的岩石和土壤带回地球。
(1)发射探测器使用的推进剂是液氢和液氧,液氢燃烧的化学方程式为 。
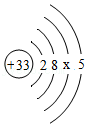
(2)嫦娥五号的登月着陆器使用的是砷化镓太阳能电池,砷的原子结构示意图如图,则x为 。
(3)月球岩石中富含钛铁矿,其主要成分是FeTiO3,其中钛(Ti)元素的化合价为+4,则铁元素的化合价为 。
第十四届全国运动会将于2021年9月15日在陕西西安盛大开幕。
(1)“石榴花”形的西安奥体中心主会场,建造时使用了大量钢铁。钢的硬度比纯铁
(填“大”或“小”)。
(2)以“秦岭四宝”为创意原型的全运会吉祥物灵动可爱、充满活力。吉祥物的制作原料之一是聚酯纤维,聚酯纤维属于 (填“合成”或“天然”)纤维。
(3)热情好客的陕西人民将会为运动员提供丰富的陕西美食。肉夹馍是美食之一,馍提供的有机营养素主要是 。
(4)全运村的绿植养护需要用到营养液,下列营养液的成分中属于复合肥的是 (填序号)。
①(NH4)2SO4
②KNO3
③Ca(H2PO4)2

气候变化中的海洋
海洋覆盖了地球70%以上的面积,是世界上最大的生物栖息地,有超过25万种生物生活在其中,为人类提供了食物、能源和交通,是应对气候变化的忠实“朋友”。
20世纪50年代以来,人类活动产生的温室气体导致地球系统热量不断增加。海洋吸收了绝大部分全球变暖的热量,还“消化”了2~3倍人为排放的二氧化碳,减缓了气候变化速度及影响。
20世纪90年代初以来,海洋变暖的速度增加了1倍。在过去的20年里,所有大洋盆地都观测到了持续数天到数月的极端海洋高温天气,即“海洋高温热浪”,它可以延伸数千公里的范围,深达数百米。热浪频发,易引起更强烈的热带气旋、厄尔尼诺现象等。2006~2015年,全球平均海平面每年上升约3.6mm,为1901~1990年期间上升速度的2.5倍。海洋在溶解了二氧化碳后,酸性增强,会影响牡蛎、蛤蜊等贝类的外壳或骨骼的形成。
阅读文本,回答问题:
(1)海洋为人类提供的食物有 (举1例,下同),能源有 。
(2)海洋吸收热量发生的变化属于 (“物理变化”或“化学变化”)。
(3)海洋“消化二氧化碳”的过程中发生反应的化学方程式为 。
(4)“海洋高温热浪”对海洋生物的危害是 。为保护海洋生态系统,人类应采取的有效措施是 。

【关注生产实际】
造纸术是中国古代四大发明之一。一直以来,传统工艺不断改进。现阶段,利用方解石(主要成分为CaCO3,还含有少量MgO、Fe2O3、SiO2等杂质)造纸已较为普遍,它取代传统的植物纤维造纸,全程无需用水,原料造价仅为传统造纸的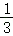 。(已知:SiO2、聚乙烯塑料、粘合剂均难溶于水,且不与盐酸反应。)分析生产过程,回答下列问题:
。(已知:SiO2、聚乙烯塑料、粘合剂均难溶于水,且不与盐酸反应。)分析生产过程,回答下列问题:
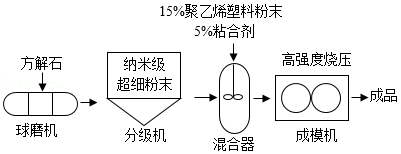
(1)将方解石粉碎成纳米级超细粉末的目的是 。
(2)混合器内需要进行的操作是 。
(3)利用方解石作原料生产纸张的优点是 。
(4)从绿色环保的角度分析,对使用的原料需要改进的地方是 。
(5)成品纸张在保存过程中应避免与酸接触,若遇到稀盐酸,则可能发生反应的化学方程式为 (写1个)。
【关注生活现象】
山西省大力实施文化强省战略,着力推进文旅融合,通过转型跨越,实现经济高质量发展。下面展示了几个旅游景点,请运用所学化学知识,就相关问题表达观点,完成下题。

(1)图Ⅰ:西侯度遗址是中国最早的人类用火证据,曾为全国二青会圣火采集留下了举国关注的佳话。圣火采集,选用主要成分为 的天然气作为清洁燃料,圣火燃烧发生反应的化学方程式为 。
(2)图Ⅱ:壶口瀑布以排山倒海的雄姿著称于世,彰显中华母亲河的博大恢宏。黄河已成为造福百姓的幸福河,生活诸多方面都离不开她,黄河水在发展经济方面可用于 。浑浊的河水给牲畜饮用时,事先应进行的简单处理是 。
(3)图Ⅲ:“万年冰洞”诞生于新生代第四纪冰川时期。冰洞内冰的物质成分用化学式表示为 ,与同质量的水相比,其体积变 ,分子间的间隔变 。
(4)为保护我省地面旅游资源,西侯度遗址上的木制建筑应严禁烟火,理由是 。为保障壶口瀑布等景点的环境卫生,应做到 。
电子工业上制造铜电路板,常用30%的FeCl3溶液腐蚀镀铜电路板上的铜箔(Cu),如图是某兴趣小组设计的处理该生产过程中产生废液的流程图,据如图回答下列问题:
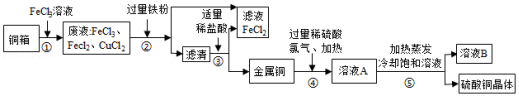
查阅资料:2Cu+2H2SO4+O2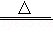 2CuSO4+2H2O;2FeCl3+Fe═3FeCl2
2CuSO4+2H2O;2FeCl3+Fe═3FeCl2
(1)步骤①所得的废液中只含有FeCl3、CuCl2、FeCl2三种溶质,据此可判断步骤①中铜与FeCl3反应生成的两种产物是 (写化学式)。
(2)步骤②中加入的铁粉与氯化铜发生反应的化学方程式是 ,步骤②还需要进行的实验操作是 。
(3)步骤③加入适量稀盐酸充分反应。当观察到 现象时,说明滤液中只剩下铜。
(4)步骤②③所得FeCl2可与一种气体单质发生化合反应生成FeCl3,实现循环使用,根据质量守恒定律可推测该单质是 。
(5)溶液B中含有的溶质是 。
2021年6月8日是第13个“世界海洋日”。烟台有漫长的海岸线,蕴藏着丰富的海洋资源。某兴趣小组设计的综合利用海水的部分流程图如图。据如图回答:
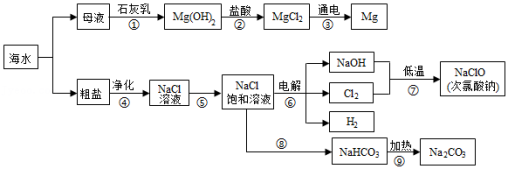
(1)海水制镁,步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式是 。步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是 。
(2)海水晒盐。通常采用 (填“降温”或“蒸发”)结晶的方法使海水中的氯化钠析出。通过步骤④除去粗盐溶液中含有的MgCl2、Na2SO4、CaCl2等可溶性杂质,需要依次加入过量的BaCl2溶液、过量的Na2CO3溶液、过量的NaOH溶液,然后过滤,在滤液中加入适量的稀盐酸。其中加入过量的Na2CO3溶液的目的是 。
(3)海水制碱。步骤⑧⑨是氨碱法制纯碱的流程,步骤⑧中需要向NaCl饱和溶液中先后加入的两种物质是 (写化学式)。步骤⑨中发生反应的化学方程式是 。
(4)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是 。
(5)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH═X+NaClO+H2O,则X的化学式是 。
2020年9月中国宣布:力争CO 2的排放在2030年前实现"碳达峰",2060年前实现"碳中和",新能源的开发、CO 2的"捕集"与利用成为当前研究的热点。
(1)氢能源开发,2021年4月科技部与山东省签署"氢进万家"科技示范工程。
①氢气作为新能源的优点是 (答一条)。
②光伏发电可为电解水制气提供电能,光伏发电用到的高纯硅可用SiO 2和碳在高温条件下反应制取,同时生成一种可燃性气体,该反应的化学方程式是 。
③某种镁铝合金是一种储氢材料,制取该合金通常在真空中熔炼而非空气中熔炼的原因是 。
(2)CO 2的"捕集",如图是一种利用NaOH溶液"捕集"CO 2的主要技术流程。
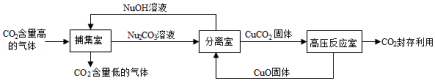
①"捕集室"中发生反应的化学方程式是 。"捕集室"中采用喷淋方式加入NaOH溶液,其优点是 。
②整个设计流程中,可以循环利用的物质是 (写化学式)。
(3)CO 2的利用。
①在高温高压下,CO 2和NH 3可以合成尿素[CO(NH 2) 2],同时生成水,该反应中参加反应的CO 2与NH 3的分子个数比是 。
②超临界CO 2是指温度与压强达到一定值时,CO 2形成气态与液态交融在一起的流体,研究发现超临界CO 2流体和水相似,溶解能力强,被誉为"绿色环保溶剂"。下列关于超临界CO 2流体的说法正确的是 (填序号)。
| A. |
它是混合物 |
| B. |
它的化学性质与普通二氧化碳相同 |
| C. |
它的分子不再运动 |
| D. |
它可代替许多有害、有毒、易燃的溶剂 |
化学与生活息息相关,请回答下列问题:
(1)人体缺 元素能导致佝偻病或骨质疏松。
(2)某同学的午餐:炖排骨、炒芹菜、米饭,其中富含糖类的食物是 。
(3)某品牌加碘盐中添加的是碘酸钾(KIO3),KIO3中碘元素的化合价是 。
(4)为防止铁锅、菜刀等铁质厨具生锈,日常生活中常用的方法是 (答一条)。
(5)铝合金材料常用来作汽车的轮毂,铝合金材料的主要优点是 (答一条)。
氮化硼(BN)陶瓷基复合材料在航天领域应用广泛。硼单质是制备氮化硼(BN)的原料之一,某工厂利用硼砂(主要成分为Na2B4O7•10H2O,杂质中含少量Fe3+)制备硼(B)单质的部分流程如图所示:
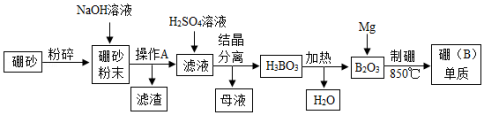
请完成下列问题:
(1)粉碎硼砂的目的是 。
(2)操作A的名称是 。
(3)滤渣的成分为 (填化学式)。
(4)写出H3BO3加热分解的化学方程式 。
(5)“制硼”反应的化学方程式为 。
构建知识网络模型是化学学习中重要的学习方法。如图1是小明同学利用左手构建的酸的化学性质知识网络。
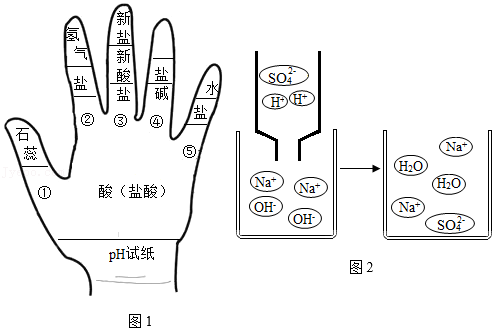
请完成下列问题:
(1)如用湿润的pH试纸测定盐酸的pH,则结果会 (填“偏大”“偏小”或“无影响”)。
(2)图1中①的现象是 。
(3)世界卫生组织推广使用中国铁锅,使用铁锅炒菜时,放点食醋可以补充人体中构成血红素的 (填“Fe2+”或“Fe3+”),该反应的原理是利用了酸的 (填序号“②”“③”“④”或“⑤”)化学性质。
(4)小明用图2来说明稀硫酸与氢氧化钠溶液反应的过程,该过程不发生变化的微粒是
(用符号表示),该反应的微观实质可表示为H++OH﹣═H2O。依此类推当图1中③是向稀盐酸中滴加硝酸银溶液时,反应的微观实质用同样的方法可表示为 。
(5)图1中⑤的性质可用于除铁锈,反应的化学方程式为 。
(6)盐酸、硫酸、食醋具有相似化学性质是因为它们水溶液中都含有 (用符号表示)。