用化学用语回答下列问题:
(1)氧元素的符号_____;
(2) 个氧原子_____;
(3)水的化学式_____。
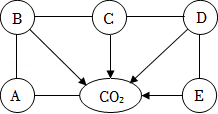
构建知识网络是一种重要的学习方法。如图是初中化学常见的单质、氧化物、酸、碱、盐五种不同类别的物质与 的知识网络图,其中D为红棕色固体,盐为钠盐。图中“一”表示反应关系,“→”表示转化关系,请回答下列问题:
(1)写出C和D的化学式:
C ;D 。
(2)A属于上述五种类别中的 。
(3)D和E反应的化学方程式为 。
(4)图中的反应没有涉及的基本反应类型是 。
五氧化二钒( )广泛用于化工行业。工业钒废催化剂中主要含硫酸氧钒( )和少量的 、 等杂质,现要除去钒废催化剂中的杂质并得到五氧化二钒固体,其流程如图所示。请回答下列问题:
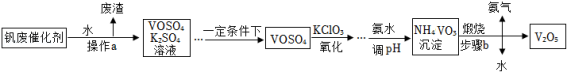
(1) 中硫元素的化合价为 。
(2)操作a的名称是 ,废渣的主要成分为 。
(3)步骤b反应的化学方程式为 。
(4)该流程中可循环利用的物质是 。
利用工业废液(主要含NaHS以及少量Na2S和Mg、Ca、Fe的化合物)制备重要化工原料硫酸钠的流程图如下。
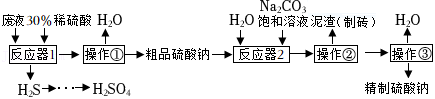
已知:Ⅰ.粗品硫酸钠含少量H2SO4、MgSO4、CaSO4、FeSO4等杂质。
Ⅱ.在溶液里,微溶物发生复分解反应可转化为不溶物。
Ⅲ.部分物质的溶解性见如表。
部分物质的溶解性表(室温)
阴离子 阳离子 |
SO42﹣ |
CO32﹣ |
Na+ |
溶 |
溶 |
Ca2+ |
微溶 |
不溶 |
Mg2+ |
溶 |
微溶 |
Fe2+ |
溶 |
不溶 |
(1)操作①名称是 。
(2)“反应器1、2”内均需要进行的操作是 。
(3)泥渣的成分有MgCO3、 等。
(4)流程中可循环使用的物质是 和 。
(5)“反应器1”中NaHS发生复分解反应生成H2S气体的化学方程式是 。
近年来我国航天事业迅速发展,彰显了我国科技力量的日益强大。
(1)某种火箭推进剂发生化学反应的微观示意图如下,该反应的产物有N2和 。
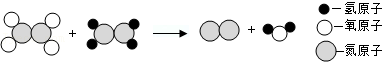
(2)“天宫课堂”广西地面分课堂上,某同学提问“空间站的氧气是怎么来的?”,太空教师叶光富解答是通过电解水得到,该反应的化学方程式是 。太空教师王亚平将泡腾片塞入蓝色水球中,产生很多小气泡,还闻到阵阵香气。“闻到香气”说明分子具有 的性质。航天员用过的水净化后可循环使用,其中利用活性炭的 性可除去水中的异味和色素等。
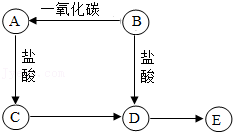
A、B、C、D、E均含同一种金属元素,它们之间的转化关系如图所示(“→”表示反应可一步实现,部分物质和反应条件略去)。已知:B为金属氧化物,其中金属元素显 价,且其质量分数为 ;A为单质;E为难溶性碱;B→A是工业制取A的主要反应原理。
(1)写出工业上由B制取A的化学方程式:__________。
(2)写出A与盐酸发生反应的现象:_______________。
(3)写出D→E的化学方程式:__________,其基本反应类型为_____。
(4)C与氯气( )可发生化合反应生成D,该反应的化学方程式为__________。
影片《闪闪的红星》中潘冬子面对敌人对食盐的疯狂封锁,机智勇敢,不畏艰险,用河水将竹筒里的食盐全部溶成盐水,再用棉袄吸收,最终将食盐送给了红军。结合下表中氯化钠的溶解度回答有关问题。
温度/ |
|
|
|
|
|
|
溶解度/ |
|
|
|
|
|
|
(1)氯化钠属于_____(填“易溶”“可溶”“微溶”“难溶”)物质。
(2)从表中数据发现氯化钠溶解度的主要特点是__________。
(3)从食盐水中得到食盐固体,一般采用的方法是_____。
(4)假设潘冬子的竹筒中有 氯化钠, 时最少需用_____ 水才能完全溶解。
(5) 时,将 食盐放入 水中,搅拌溶解,所得溶液中溶质的质量分数为_____(结果保留至 )。
海水是宝贵的自然资源,从海水中提取食盐的主要过程如图。
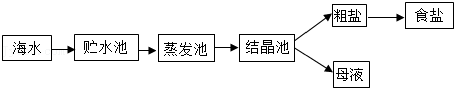
(1)食盐的主要成分是_______。
(2)蒸发池中,水蒸发属于_______(填“物理”或“化学”)变化。
(3)下列是去除粗盐中难溶性杂质的操作,正确的顺序是_______(填序号)。
| A. | 过滤 |
| B. | 溶解 |
| C. | 蒸发 |
阅读下面科普短文。
广袤无际的自然界是一个碳的世界。碳在自然界中的循环变化,对于生态环境有极为重要的意义。
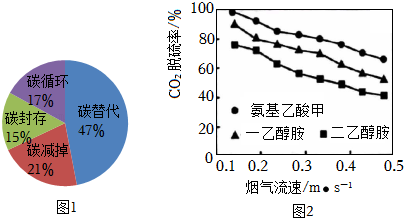
随着工业生产的高速发展和人们生活水平的提高,排入大气中的 越来越多,导致温室效应增强。减少 排放,实现碳中和,已成为全球共识。碳替代、碳减排、碳封存、碳循环是实现碳中和的4种主要途径。科学家预测,到2050年,4种途径对全球碳中和的贡献率如图1。
的吸收是碳封存的首要环节,常选用 、氨水、一乙醇胺等作吸收剂。在研究膜吸收法吸收 时,研究人员通过实验比较了一乙醇胺、二乙醇胺、氨基乙酸钾3种吸收剂对烟气中 的脱除效果,其结果如图2。
我国提出2060年前实现碳中和,彰显了负责任大国的作为与担当。实现碳中和人人有责,让我们从衣食住行点滴做起,节约能源,低碳生活。
(原文作者邹才能、林忠华等,有删改)
依据文章内容回答下列问题。
(1)自然界碳的循环中,化石燃料燃烧_______(填“吸收”或“释放”) 。
(2)由图1可知,到2050年,对全球碳中和贡献率最大的途径是_______。
(3)用 溶液吸收 ,发生反应的化学方程式为______________。
(4)判断下列说法是否正确(填“对”或“错”)。
①由图2可知,随烟气流速增大, 脱除效果增强。_______
②节约用电,绿色出行,有助于实现碳中和。_______
(5)对比图2中三条曲线,得出的结论是:在实验研究的烟气流速范围内,当烟气流速相同时,____________________________。
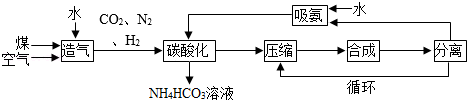
要实现“装满‘米袋子’,充实‘菜篮子’”的目标,化肥起到非常重要的作用。工业以煤、空气和水为原料生产碳酸氢铵的一种流程如图所示:
(1) 属于_____(填“氮”、“磷”、“钾”或“复合”)肥。
(2)“造气”是利用煤、空气和水在一定条件下反应获取 和 ,加快“造气”反应速率的具体措施有 _______________(写一点)。
(3)“合成”是指 和 在一定条件下反应生成氨气,反应的化学方程式为 ____________________。
(4)“循环”是指 __________(填物质名称)的循环利用。
北京冬奥会成为迄今为止第一个“碳中和”的冬奥会。碲化镉可用于制作薄膜太阳能电池,国家速滑馆“冰丝带”外墙使用了大量碲化镉发电玻璃。
(1)如图是元素周期表中元素镉、碲的相关信息,回答下列问题:
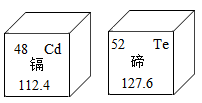
①镉的相对原子质量为_______。
②碲有多种化合价, 读作_______。
(2)碲化镉可由 洛液和 溶液通过复分解反应制得,化学方程式为_______。
(3)建筑物上的碲化镉发电玻璃工作时将太阳能转化为_______能。
金属材料与人类生活息息相关,请回答下列问题。
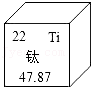
(1)钛元素在元素周期表中的信息如图所示,则钛的相对原子质量是 。
(2)家用台灯通常采用铜质插头,是利用金属铜的 性。
(3)我国是最早采用湿法炼铜的国家,铁与硫酸铜溶液反应的化学方程式是 。
(4)将一定质量的Zn片加入AgNO3、Cu(NO3)2的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是 ;若滤液蓝色,则滤液中溶质一定有 。
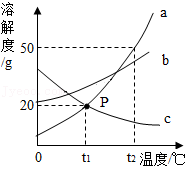
如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,根据如图回答下列问题。
(1)P点的含义是 。
(2)t2℃时,a、b、c三种物质的溶解度由大到小的顺序是 。
(3)t1℃时,将25g a物质加入到100g水中,充分搅拌溶解后恢复到原温度,所得溶液中溶质与溶剂的质量比是 (最简整数比)。
(4)t2℃时,将a、b、c三种物质的等质量的饱和溶液降温至t1℃,下列说法正确的是 。
A.都是饱和溶液
B.溶质质量分数大小关系是:b>a>c
C.析出晶体质量最多的是a
(1)如图1中A、B、C、D是四种粒子的结构示意图。
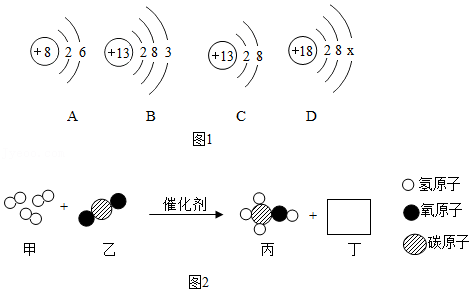
①C粒子的符号为 。
②图A、B、C、D共表示 种元素,由A、C两种元素组成的化合物的化学式为 。
③D中x= 。
(2)二氧化碳会引起温室效应。某纳米纤维化剂可将二氧化碳转化为液体燃料甲醇(CH3OH),其微观示意图如图2(图中的微粒恰好完全反应)。
①该反应中涉及到的单质的化学式为 。
②写出该化学反应方程式: 。
厉害了,我的国!5月15日,“天问一号”巡视器成功着陆于火星乌托邦平原,我国首次火星探测器任务着陆火星取得圆满成功。运载“天问一号”探测器的“长征五号遥四”常用氢氧燃料提供动力。结合以下装置探究氢气、氧气的相关实验,回答下列问题。

(1)如图的仪器甲的名称为 。
(2)在实验室用高锰酸钾做原料制取氧气,发生装置应选择 (填标号),选用装置F采用排空气法收集,氧气应从 (填“h”或“i”)通入。
(3)采用锌与稀盐酸反应制取氢气,反应原理为(用化学方程式表达) ,选择上述恰当的装置,组装一套制取、除杂、并收集一瓶氢气的装置,所选装置的接口连接顺序为a→ → →h(填接口标号)。