如图是初中化学教科书中的一些实验装置示意图。回答下列问题:
(1)A实验中,一段时间后可根据观察到 的现象,得出铁生锈需要与氧气接触的结论;
(2)B实验中,观察到薄铜片上的乒乓球碎片先燃烧,滤纸碎片后燃烧,可以说明燃烧条件之一是 ;
(3)C实验可得到的结论是 ;
(4)D实验中,向水中加少量硫酸钠或氢氧化钠的目的是 。
掌握仪器的使用并严格按照操作要求进行实验,是保证化学实验成功和安全的关键,根据所学化学知识,回答下列问题:
(1)将pH试纸用蒸馏水润湿后,测定某酸溶液的pH,测定的结果 (选填“偏大”或“偏小”或“无影响”)
(2)做细铁丝在氧气中燃烧实验时,在集气瓶中预先放一些水的目的是 ;
(3)用氯化钠固体和水配制50g溶质质量分数为6%的氯化钠溶液,在用量筒量取水时仰视读数,其它实验操作均正确,所配制好的溶液溶质质量分数会 (选填“偏大”或“偏小”或“无影响”);
(4)粗盐中难溶性杂质的去除实验步骤是:溶解、过滤、 、计算产率,各实验步骤都要用到的仪器是 。过滤操作中速度慢的原因可能是 。
如图是实验室制取气体的常用装置,请回答下列问题.
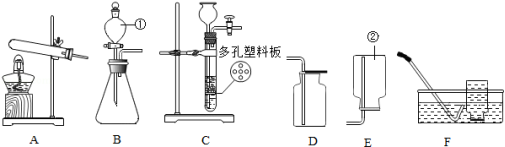
(1)写出图中标号仪器的名称是:① ,② .
(2)实验室可加热KMnO 4固体制取O 2,请写出该反应的化学方程式 ,应选用的气体发生装置是 (填字母),气体收集装置是 (填字母,写出一种即可).
(3)实验室可用Zn粒与稀硫酸反应制取H 2,若选用C装置,其优点是便于控制反应的发生和停止,此时Zn粒应放置于 .
(4)实验室可用石灰石(或大理石)与稀盐酸反应制取CO 2,请写出该反应的化学方程式: .若选用C装置,能否体现其优点并说明具体理由: .
李老师在《燃烧的条件》教学中,改进了教材中的实验,如图所示,在铜片上罩上烧杯,请回答:
(1)罩上烧杯的作用是 ;
(2)能说明燃烧条件之一是温度达到可燃物着火点的实验现象是 。
(3)热水的作用是 。

请你根据所学知识并结合如图所示装置回答有关问题:
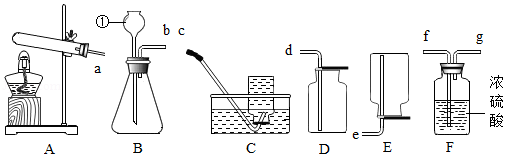
(1)指出标号仪器的名称:① .
(2)用氯酸钾和二氧化锰共热制氧气的化学方程式是 ,用C装置收集氧气不纯的原因是 (写一点即可).
(3)制取并收集一瓶干燥的二氧化碳气体,所选装置接口的连接顺序是 (填字母),判断二氧化碳是否收集满的方法是 .
某化学小组欲配制49g溶质质量分数为20%的稀硫酸来进行实验,老师为他们提供了溶质质量分数为98%的浓硫酸(密度为1.84g/cm 3).
(1)通过计算,需要用到溶质质量分数为98%的浓硫酸的质量是 g.
(2)量取浓硫酸时仰视读数(其他操作正确),则配制的稀硫酸的溶质质量分数 (填"大于"、"小于"或"等于")20%.
(3)A和B是两个同学稀释浓硫酸操作的示意图,正确的是 (填"A"或"B").
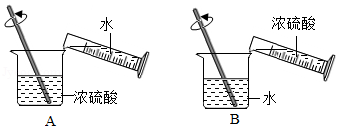
(4)玻璃棒搅拌的作用是 .
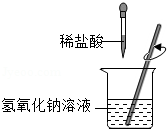
小红同学进行酸碱中和反应的实验(如图所示)。她向氢氧化钠溶液中滴加一定量稀盐酸后,想起氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到试管中溶液颜色没有变化。于是她对烧杯中的溶液进行了以下探究:
(1)小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠恰好完全反应;②氢氧化钠有剩余;③盐酸过量。
小明同学却断定不可能"氢氧化钠有剩余",他的理由是: ;
(2)他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证。请根据相关内容填写如表:
| 试验方法 |
可能观察到的现象 |
结论 |
| 将少量锌粒放入试管中,然后从烧杯中取适量溶液至试管中。 |
如果 |
则盐酸过量 |
| 如果 |
则盐酸与氢氧化钠恰好完全反应 |
(3)经过讨论,他们认为利用下列几种物质代替锌粒,也可以达到验证目的。你认为其中不正确的是 (填序号)。
A.生锈的铁钉 B.碳酸钠粉末 C.硫酸钠粉末 D.氢氧化铜
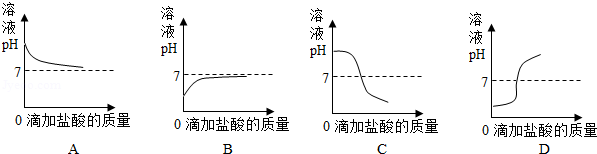
(4)如图曲线能够表示小红所做试验中溶液pH变化趋势的是 (填序号)。
有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行实验。

请回答下列问题:
(1)过滤操作中用到的玻璃仪器有烧杯、玻璃棒和 ,其中玻璃棒的作用是 。
(2)滤渣a的成分是 ,滤液中溶质的成分除氯化钠还有 ,白色沉淀b的成份是 。
(3)若现象①"滤渣全部溶解"变为"滤渣部分溶解",其他现象不变,则原样品中不能确定是否存在的物质是 。
某班学生分三组分别做了二氧化碳制取和性质验证实验,如图所示。实验结束后,老师取两份等质量的丙废液,分别与甲、乙废液混合,将甲废液与丙废液倒入烧杯A中,有白色沉淀生成;将乙废液与丙废液倒入烧杯B中,有气泡产生。请填空:

(1)甲废液与乙废液所含溶质的成分可能不同的是 (用化学式填空,下同)
(2)烧杯A中沉淀的成分一定有 。
(3)另取少量丙废液样品,加入足量的氯化钡溶液,有白色沉淀生成,过滤,向滤液中滴加氯化铁溶液,观察到有红褐色沉淀生成,未发现其他明显现象。由此推测出,丙废液溶质的成分是 ,丙废液与氯化钡溶液反应的化学方程式为 ,烧杯A的上层清液中溶质的成分一定有 。
实验是进行科学探究的重要方式,某同学设计如图所示实验,探究二氧化碳的有关性质。请填空:

(1)实验1采用科学探究中的控制变量法,该实验控制的变量是 。
(2)实验1中干石蕊纸花喷水后放入二氧化碳中,观察到的现象是 ,该反应的化学方程式是 。
(3)实验2是在实验1的基础上设计的创新改进实验,将二氧化碳缓慢通入竖直放置的玻璃管中,能观察到第 (填序号)号棉球先变色,通过此现象可获得关于二氧化碳的另外一条性质是 。
t 1℃时,将a、b两种固体各18g,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图甲所示,升温到t 2℃时,现象如图乙所示,a、b两种固体在水中的溶解度曲线如图丙所示。

请填空:
(1)从t 1℃到t 2℃的变化过程中,一直处于饱和状态的是 (填"a"或"b")的溶液。
(2)图丙中曲线M表示的是 (填"a"或"b")的溶解度曲线。
(3)若a中混有少量的b,可采用 结晶的方法提纯a。
酸奶是日常生活中常见的一种食品,如表是某酸奶外包装上标识的营养成分表.
| 项目 |
能量 |
蛋白质 |
脂肪 |
糖类 |
钠 |
| 每100g |
329kJ |
2.6g |
3.1g |
10.0g |
60mg |
请填写下列空格:
(1)酸奶中的 在消化道内会逐渐被分解成可被人体吸收的多种氨基酸.
(2)脂肪在人体内分解、氧化释放出能量的过程,是将 能转化为热能.
(3)蔗糖(C 12H 22O 11)是酸奶中的一种糖类物质,蔗糖的组成中碳、氢元素的质量比为(最简整数比) .
(4)在选择制作酸奶包装盒的材料时,从化学性质的角度分析该材料应具备 的特点(填写一条即可)
根据下列装置,回答问题:
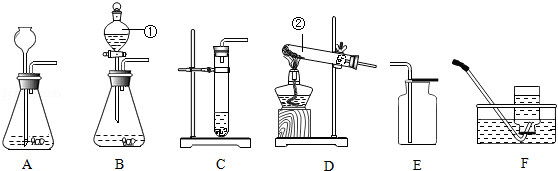
(1)写出图中标号仪器的名称:① ;② .
(2)实验室用过氧化氢溶液和二氧化锰制取氧气时,发生反应的化学方程式为 ,从控制反应速率和节约药品的角度考虑,发生装置最好选用 (填装置序号).
(3)因为氧气不易溶于水,所以可以利用装置 (填装置序号)收集,如果要做铁丝在氧气中燃烧的实验,用这种装置收集氧气时应注意 .
氢气是中学化学的重要试剂,可以与Fe 2O 3、CuO等多种金属氧化物反应得到金属单质.某化学兴趣小组利用白铁(表面镀锌的铁)加工业的下脚料制取氢气,生成的氢气与CuO反应,其反应装置如图:(部分夹持装置省略)
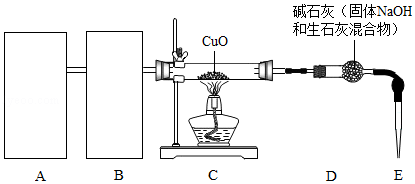
(1)从下图a、b、c中选择一套制取氢气的最佳装置 置于A处.
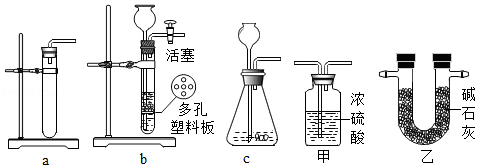
(2)该小组若选用盐酸和白铁片反应制取氢气,请为B处从上图甲和乙中选择一套合适的除杂装置 .
(3)检验装置气密性之后,点燃C处酒精灯之前必须进行的步骤是 .
(4)若称取CuO的质量为m 1g,反应一段时间后C处药品完全变为紫红色,此时停止加热,继续通入氢气至药品冷却,称量D装置,质量增加了m 2g,则m 1和m 2应满足的关系是 .(忽略其他因素带来的误差)
硫酸是化学实验室里的常见试剂.现利用质量分数为98%、密度为1.84g/cm 3的浓硫酸配制100mL质量分数为10%、密度为1.07g/cm 3的稀硫酸.(已知:水的密度近似为1g/cm 3,不同质量分数的溶液混合后总体积不是两种溶液体积之和)
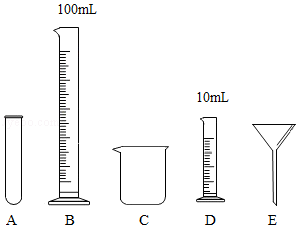
(1)量取浓硫酸时需要的仪器是 .
(2)配制该稀硫酸溶液时,下列方法最合理的是 (假设需要浓硫酸的体积是V mL).
a、分别用量筒量取V mL浓硫酸和(100﹣V)mL水,在烧杯中混合均匀
b、先量取V mL浓硫酸倒入烧杯中,再称量(107﹣1.84V)g水,慢慢倒入盛有浓硫酸的烧杯中混合均匀
c、先量取(107﹣1.84V)mL水倒入烧杯中,再将量取的V mL浓硫酸慢慢倒入盛水的烧杯中混合均匀
d、先在100mL量筒中加入V mL浓硫酸,然后向其中加水恰好至100mL刻度处混合均匀
(3)在量取浓硫酸时若俯视量筒的刻度线,则所配制的硫酸溶液的质量分数 10%(填"大
于"、"等于"或"小于").
(4)用pH试纸测定所配制的硫酸溶液的pH,正确的操作是 .