为测定某BaCl 2溶液的溶质质量分数,进行如下实验:取104g该溶液于烧杯中,加入1g稀硝酸溶液酸化,无任何现象,然后将30g一定溶质质量分数的硫酸溶液分三次加入,每次充分反应后过滤、称量(实验中物质的质量损失忽略不计),数据如表:
| |
第1次 |
第2次 |
第3次 |
| 加入硫酸溶液的质量/g |
10 |
10 |
10 |
| 过滤后溶液的质量/g |
105 |
105 |
111.7 |
根据以上数据计算:(BaCl 2+H 2SO 4═BaSO 4↓+2HCl)
(1)该实验过程中产生沉淀的总质量为 g.
(2)该BaCl 2溶液中溶质的质量分数(写出计算过程)
2015年,我国科学家屠呦呦因为发现疟疾药物青蒿素而获得诺贝尔奖,请根据青蒿素的化学式C 15H 22O 5计算:
(1)一个青蒿素分子由 个原子构成.
(2)青蒿素中碳元素和氧元素的质量比为 (填最简整数比)
某石油化工厂化验室的实验员用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,测得实验数据如表:
| 实验序号 |
消耗NaOH溶液的质量 |
洗涤后溶液的pH |
| ① |
30g |
pH<7 |
| ② |
40g |
pH=7 |
| ③ |
50g |
pH>7 |
请回答下列问题:
(1)欲计算出一定量石油产品中所含H 2SO 4的质量,你觉得应该选择实验序号 的数据.
(2)若一定量石油产品中残余硫酸的质量为100g,请计算该残余硫酸的溶质质量分数(写出详细的计算过程)
如图所示是某中学化学兴趣小组对二氧化碳与氢氧化钠溶液反应进行的创新实验.
已知:20℃时,氢氧化钠在乙醇中的溶解度为17.3g,而碳酸钠在乙醇中几乎不溶解.
请回答下列问题:
(1)写出仪器a的名称 .
(2)按图组装好二氧化碳的发生装置,实验前要检查装置的 .
(3)反应装置中长颈漏斗的作用是 (填序号)
A.添加稀盐酸 B.添加石灰水 C.添加稀盐酸和石灰石
(4)制取二氧化碳气体的化学反应方程式为 .
(5)将二氧化碳气体通入饱和氢氧化钠乙醇溶液中,马上有沉淀出现,出现这一现象的原因是 (请用文字表述)

某化学小组将稀盐酸滴入一定量的碳酸钙样品(杂质不与盐酸反应)中制取CO 2.产生CO 2的质量与滴入稀盐酸的质量关系如图所示,请回答:
(可能用到的相对原子质量:H﹣1 C﹣12 O﹣16 Cl﹣35.5)
(1)该试验最多制得CO 2得质量为 g.
(2)计算所滴加的盐酸中溶质的质量分数.(要求有计算过程)

某工厂化验室用稀硫酸处理造纸厂产生含有氢氧化钠的废水.现称取废水样品80g倒入烧杯中,逐滴加入10%的稀硫酸至恰好完全反应,消耗稀硫酸98g.(反应的化学方程式:H 2SO 4+2NaOH═Na 2SO 4+2H 2O)
(1)氢氧化钠中氧元素的质量分数是 ;
(2)求废水中氢氧化钠的质量分数(要写出计算过程).
某化学兴趣小组参观了一个石灰厂时,带回了一些石灰石样品,同学们利用这些石灰石样品做了如下实验:取样品10g放入烧杯中,将50g稀盐酸分5次加入,实验过程所得的数据如表所示(已知石灰石样品中的杂质不参与反应,也不溶于水)。根据实验数据计算:
| 实验次数 |
加入稀盐酸的质量/g |
剩余固体的质量/g |
| 1 |
10 |
8 |
| 2 |
10 |
6 |
| 3 |
10 |
4 |
| 4 |
10 |
2 |
| 5 |
10 |
2 |
(1)第 次加入稀盐酸充分反应,CaCO 3恰好完全反应;
(2)石灰石样品中CaCO 3的质量分数= ;
(3)所用稀盐酸中溶质的质量分数。(写出计算过程,结果精确到0.1%)。
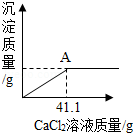
某化学课外活动兴趣小组的同学,对某化工产生产的纯碱样品(已知杂质只含氯化钠)的纯度产生了兴趣,设计实验并探究如下:①取一定质量的该样品,加55.65g水配成溶液;②向溶液中逐渐加入一定质量分数的CaCl 2溶液(实验中产生的沉淀与加入CaCl 2溶液的质量关系如图所示),当反应至A点时恰好完全反应;③过滤,测得所得滤液为100g14.35%的氯化钠溶液(实验过程中水的损失忽略不计)。试求:
(1)完全反应后,所得滤液中水的质量为 g。
(2)该纯碱样品中碳酸钠的质量分数为多少? 。(无计算过程不给分)
(1)某学习小组为测定M硫酸厂排放的废水中的硫酸含量进行如下实验:取50g废水于烧杯中,滴入质量分数为10%的氢氧化钠溶液(假定废水中其他成分不与氢氧化钠反应),当废水pH 时(填">7"、"=7"、"<7")反应恰好完全,测得消耗该氢氧化钠溶液8g,据此计算该废水中硫酸的质量分数.
(2)M硫酸厂常用熟石灰对废水进行处理并产生硫酸钙,已知M厂每天用这种方法处理废水50吨,计算M厂每天理论上能产生多少吨硫酸钙.
实验室要配制100克5%的Na 2SO 4溶液。试计算:
(1)需要Na 2SO 4固体 g。
(2)Na 2SO 4中硫元素与氧元素的质量比为 。
工业上煅烧石灰石(CaCO 3)可制得生石灰(CaO)和二氧化碳,如果要制取2.8t氧化钙,计算需要碳酸钙的质量.
某化学兴趣小组在实验室用碳酸钠溶液和熟石灰制取少量氢氧化钠溶液。他们的实验过程和相关数据如图所示。请计算:
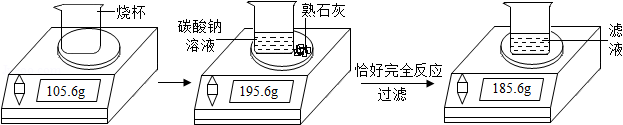
(1)实验中生成沉淀的质量为 g;
(2)所得氢氧化钠溶液中溶质的质量分数。
实验室用50g溶质质量分数为7.3%的稀盐酸与足量的石灰石反应制取二氧化碳,理论上可制得二氧化碳多少克?
我市锰矿资源丰富,MnO 2是一种无机功能材料,主要用于制造干电池。某校课外活动小组同学得到当地某粗MnO 2样品(主要含有杂质MnCO 3,其它杂质忽略不计),为了测定此样品中MnO 2的含量,把100g粗MnO 2样品放入烧杯中,将40g稀硫酸分4次加入与之充分反应,测得的数据如下表。
| 次数 |
1 |
2 |
3 |
4 |
| 加入稀硫酸的质量(g) |
10 |
10 |
10 |
10 |
| 剩余固体质量(g) |
94.25 |
88.5 |
82.75 |
78.2 |
(已知烧杯中发生的反应为:MnCO 3+H 2SO 4═MnSO 4+H 2O+CO 2↑)
请根据图表数据回答下列问题:
(1)样品中杂质的质量是多少?
(2)该样品中MnO 2的质量分数是多少?
(3)稀硫酸中溶质的质量分数是多少?