碳酸钠与盐酸的反应是分两步进行的,第一步反应的化学方程式为:
.为验证该反应分两步进行.如图所示进行实验(装置气密性良好).

步骤
:用注射器1向小药瓶中緩慢注入一定量的稀盐酸,边注入边振蕩,细玻璃管中液柱略微升高;換注射器
从瓶中缓慢抽取气体,澄清石灰水不浑浊.
步骤
:…
(1)补充步骤
的实验操作和预期现象.
(2)说明细玻璃管在实验中的作用.
(3)实验后,将小药瓶、注时器
、注射器
中的所有物质依次倒入一个洁净的烧杯中,只得到无色溶液,向其中滴加酚酞溶液不变色.写出溶液中溶质成分存在的几种情况(酚酞省略不写).
、
是生活中常见的盐,某实验小组通过以下实验来研究者离子物质的性质(已知:
、
的水溶液呈碱性;
受热易分解生成
、
和
).
(1)称取两种固体各1g分别放入两支试管中,再加入5mL水,振荡.固体充分溶解,并恢复至室温;
①发现
完全溶解,而
有剩余.由此得出结论:在相同温度下,;
②向所得溶液中各滴入1~2滴酚酞溶液后,溶液均呈 色。
(2)①取少量
按如图装置进行实验,可观察带的现象是:大试管口有水珠生成,;
②用的方法除去混在
粉末中少量的
。

(3)测定
样品(含
杂质)中
的质量分数:
①称取mg样品放入烧杯中加水溶解;
②加入过量的
溶液充分反应,反应的化学方程式为;证明反应后
有剩余的方法是;
③过滤、洗涤、干燥,称量测定的质量为ng.则样品中
的质量分数为.
向一定质量AgNO3。和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示。
(1)请写出a点所发生反应的化学方程式。
(2)e点所示的溶液中含有哪些溶质?
(3)d点表示的固体中含有哪些物质?
构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:

(1)如用湿润的pH试纸测定盐酸的pH,则结果会(填"偏大"、"偏小"、"无影响")。
(2)图中①的现象是:。
(3)写出一个符合图中③的化学方程式。
(4)图中性质④属于反应(填基本反应类型)。
(5)图中⑤的性质在工业上可用于(填用途)。
为了达到收旧利废节能减排的目的,从含有金属镁、铁、铜的粉末中,分离和提取出重要化工原料MgSO4和有关金属,实验过程如下:
请回答:
(1)操作①中被磁铁吸引的金属A是__________;
(2)在蒸发过程中需要使用玻璃棒,其作用是______________________________;
(3)写出步骤②所涉及的化学反应方程式:___________________________________;
(4)实验步骤②中除了加入稀硫酸外,还可选用下列试剂__________(填标号)。
a.硫酸铜溶液 b.氯化钠溶液 c.硝酸银溶液
写出下列反应的化学方程式,并在括号内注明基本反应类型:
(1)氢气在氧气中燃烧 ( )反应。
(2)铁和硫酸铜溶液反应
(3)碳酸钠溶液与石灰水混合
向硝酸银、硝酸铜和硝酸镁的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中滴加稀盐酸,无明显现象,则滤液中一定含有的金属离子是什么?写出上述过程中一定发生反应的化学方程式。
请用所学化学知识解释下列问题。
(1)可燃物是否充分燃烧与哪些因素有关?(填写一个即可)并举一例加以证明。
(2)向盛有氢氧化钠溶液的试管中滴加硫酸铜,产生沉淀,对其加热,产生黑色固体,请推断黑固体是什么物质?再向其中加入稀硫酸,黑色物质消失,溶液变为蓝色,请用化学方程式解释黑色固体消失的原因。
化学就在我们身边。请用化学方程式表示下列事实中的化学反应:
(1)收藏家收藏清朝末年的铝制品至今仍保存完好,其原因是:
;
(2)用自来水配制的硝酸银溶液变浑浊(提示:自来水经氯气消毒后会含有少量盐酸):
。
某化学兴趣小组欲除去固体氯化钠中混有少量可溶性氯化镁和难溶性泥沙,设计下图所示实验方案,请参与实验并回答问题。
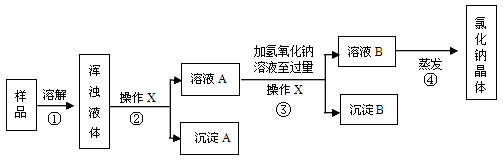
(1)步骤①中玻璃棒搅拌的作用是。
(2)步骤②、③中,操作X的名称是。
(3)步骤③中,加入过量氢氧化钠溶液的目的是;沉淀
的化学式是。
(4)有同学认为原实验方案不完善,做出这种评价的依据是。
有人用经过粉碎的含有较多有机物杂质的粗铜,通过下列步骤制取硫酸铜晶体
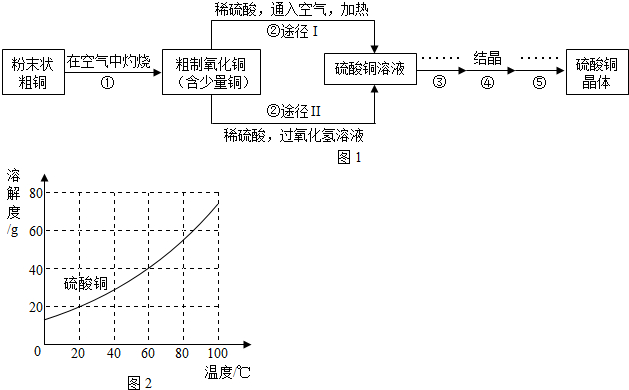
(1)若步骤①中灼烧温度过高会产生副产物氧化亚铜(铜的化合价为+1价),其化学式为。
(2)写出步骤②中氧化铜与稀硫酸反应的化学方程式:。
(3)步骤②中,铜和稀硫酸不能直接发生置换反应的原因是。
(4)反应途径Ⅰ和Ⅱ,分别发生如下反应:
途径Ⅰ:
途径Ⅱ:
请选择你认为更适合于实际应用的途径,并说明理 由:。
(5) 根据图2,步骤④的结晶方法为。
(6)若800
粗制氧化铜(其中单质铜的质量分数为4%),通过途径Ⅱ转化为硫酸铜,计算参加反映的过氧化氢的质量。写出计算过程。
下图中的甲、乙、丙表示初中化学常见的物质,且甲、乙、丙为不同类别的化合物,乙属于氧化物。胃液中含有适量的甲,可帮助消化。图中"-"表示两端的物质问能发生化学反应;"→"表示物质间存在转化关系;部分反应物、生成物已略去。

(1)写出甲的化学式。
(2)①若乙在常温下为液体,丙可用来改良酸性土壤,则乙的化学式为,丙的化学式为。
②若乙在常温下为气体,且可由甲与大理石反应得到,则乙的化学式为,丙能与①中的丙发生复分解反应,其化学方程式为(写出一个即可)。
③写出①中的乙和②中的乙发生化合反应的化学方程式 为。
碳酸钡与碳酸钙具有相似的化学性质,高温下能分解成两种氧化物;氧化钡与氧化钙都能与水反应生成对应的碱。以含有碳酸钡的毒重晶石生产氢氧化钡的流程如下:
(1)操作I的名称是 ;操作II的名称是 ,其目的是 ;
(2)写出水浸池中发生反应的化学方程式 ;
(3)下列相关说法正确的是 。
A.毒重晶石进行预处理“研磨成粉状”有利于充分焙烧
B.焙烧炉中添加焦炭粉和热空气可以维持炉内的高温状态
C.焙烧炉内只涉及到分解反应