小明同学对木炭和木片进行了如下的探究:
分别点燃木炭和木片,在火焰的上方分别罩一个冷而干燥的烧杯,发现红热的木炭上方罩的烧杯内壁上没有水雾,将烧杯调转过来,迅速向烧杯内倒入少量澄清石灰水振荡,石灰水变浑浊,说明木炭燃烧没有生成 ,生成了 。
而罩在木片火焰上方的烧杯内有水雾产生,倒转过来,向烧杯中倒入少量澄清石灰水振荡,石灰水变浑浊,,说明木片燃烧既生成了 ,又生成了 。由此得出的结论是木片和木炭的成分是 (填相同或不同)。
在碳、一氧化碳、二氧化碳、氧气四种物质中,每一种物质都有不同于其他三种物质的特点,例如:碳:常温常压下是固体,其他三种物质是气体。请根据示例,填空:
(1)一氧化碳:________________________________;
(2)二氧化碳:________________________________;
(3)氧气:____________________________________.
某兴趣小组利用下图装置进行二氧化碳的制取和部分性质实验,请回答下列问题:
(1)关闭E打开C,从长颈漏斗A中加入液体与锥形瓶B中固体接触,即有二氧化碳气体产生。观察到D中的蜡烛慢慢熄灭,说明二氧化碳具有____________的性质。写出实验室制取二氧化碳的化学方程___________。
(2)关闭C打开E,则观察到G中的蜡烛燃烧得更旺,说明有氧气生成。
[查阅资料]二氧化碳能与过氧化钠( )反应生成碳酸钠和氧气。
)反应生成碳酸钠和氧气。
[实验探究]要检验反应后F中的固体物质含有碳酸钠,可取少量反应后F中固体物质于试管中,滴入盐酸,观察到有气泡产生;用蘸有澄清石灰水的玻璃片放在试管口,观察到澄清石灰水变浑浊,写出该反应的化学方程式_________________。
[实验结论]二氧化碳与过氧化钠反应的化学方程式为____________________。
[拓展联系]某同学用一团棉花包裹过氧化钠并滴入几滴水,发现棉花团燃烧,说明过氧化钠也能和水反应生成氧气且反应一定___________(选填放热或吸热)。
(12分)在氧气、一氧化碳、二氧化碳、氢气四种物质中,
能使带火星的木条复燃的是________(用化学式填空,下同);有剧毒的是________;
可以使紫色石蕊溶液变红的是________;可以做制冷剂的是________;
可用来填充气球的是________;具有可燃性的是________。
某燃料X在7.2g氧气中燃烧,得到9.2g混合气体(可能含有一氧化碳、二氧化碳、水蒸气)。化学兴趣小组的同学利用下图所示装置验证混合气体的成分。
资料:①浓硫酸具有吸水性。②浓氢氧化钠溶液能吸收二氧化碳。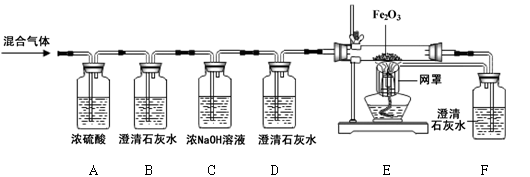
(1)通过混合气体后,A装置增重4.5g,说明混合气体中含有________________________。
(2)B装置中澄清石灰水变浑浊,发生反应的化学方程式为 。D装置的作用是 。
(3)当观察到 ,证明混合气体中有CO。
(4)实验结束后,同学们称量B、C装置共增重3.3g,根据以上数据可确定燃料X中所含元素及元素质量比为_________________。
二氧化碳是重要的资源,具有广泛的用途。
(1)二氧化碳可用于生产碳酸饮料,其中发生反应的化学方程式为_________________。
(2)液态二氧化碳可用于扑救档案室发生的火灾,下列说法正确的是________。
A.液态二氧化碳气化后不会污染档案
B.二氧化碳可覆盖在可燃物表面,隔绝空气
C.液态二氧化碳气化时吸热,降低可燃物的着火点
(3)为减少温室气体二氧化碳的排放,可以将二氧化碳进行转化。下图为该反应的微观示意图,根据图示回答下列问题。
① 物质C是由_____________构成(填“分子”、“原子”或“离子”)。
② 以上4种物质中属于氧化物的是_____(填字母序号)。
③ 该反应中C、D两种物质的质量比是 。
下列物质的用途与性质不对应的是
| A.食品包装中充氮气以防腐——常温下氮气的化学性质不活泼 |
| B.一氧化碳用于冶炼金属——一氧化碳具有可燃性 |
| C.稀有气体能制成多种用途的电光源——稀有气体在通电时发出不同颜色的光 |
| D.干冰可用做制冷剂——干冰升华吸热 |
科技节活动中,化学实验小组做了如下实验,请回答以下问题。
(1)图A所示实验可观察到“铁树”上浸有无色酚酞试液的棉团由白色变为 色,该实验中没有涉及的性质是 (填字母)。
A.氨分子是不断运动的 B.氨分子有一定质量 C.浓氨水具有挥发性
(2)图C所示实验发生反应的化学方程式为 。
(3)图C所示实验中,当通过导管向热水中通入氧气时,白磷在水下燃烧,该实验说明燃烧需要的条件为:①可燃物;②达到燃烧所需要的 ;③ 。
(4)图D所示实验观察到紫色小花变为红色,小花变红的原因是
(用化学方程式表示)。
化学小组的同学利用干冰做兴趣实验。
(1)在降温加压时二氧化碳会变成无色液体,温度进一步降低,液态二氧化碳可变成雪花状固体—干冰。上述过程发生了(填“物理”或“化学”)变化,说明分子具有的性质是________。
(2)如图1所示向盛有干冰的玻璃容器中加入热水,立即产生大量浓厚的白雾,在容器口涂一层洗涤灵膜,很快观察到膜鼓起(如图2),此时容器中的主要气体是 。
(3)向图3装置的小试管中加入适量干冰,看到U形管中左侧液面上升、右侧液面下降,产生此现象的原因是 。
(4)另取一盛有适量澄清石灰水的玻璃容器,向其中加入少量干冰,观察到的主要现象是,发生反应的化学方程式为__________。
(4分)小明为了验证CO的化学性质,他设计了如图所示的实验装置,请你结合装置图回答下列问题:
(1)写出下列装置中发生的化学反应方程式
装置A ,
装置D ,
(2)装置B的作用是 ;
(3)装置有一个明显不足,请指出具体的改进措施
(4分)科学家把工业上排出的二氧化碳气体采用“组分转化”技术,将CO2和H2以一定比例混合,在一定条件下反应生成一种重要的化工原料和水,反应的化学方程式为:2CO2+6H2  X十4H2O,
X十4H2O,
(1)请写出X的化学式 ,判断依据是 。
(2)为了减缓大气CO2含量的增加,下列建议中,目前可行的是 (填序号)
①严格遵守国际相关“低碳”公约
②禁止使用煤、石油等矿物能源
③更多地利用太阳能、风能等清洁能源
④少开私家车
(3分)用下列所给物质的番号按要求填空:
①二氧化碳 ②石墨 ③金刚石 ④活性炭 ⑤氢气 ⑥氖气
(1)可用于霓虹灯的是 (2)可用于切割玻璃的是
(3)可制碳酸饮料的是 (4)可作燃料的气体单质是
(5)可用于制铅笔芯的是 (6)可用于冰箱除味的是
在碳、一氧化碳、二氧化碳、氧气四种物质中,每一种物质都有不同于其他三种物质的特点,例如:碳:常温常压下是固体,其他三种物质是气体。请根据示例,填空:
(1)一氧化碳:____________________________________________;
(2)二氧化碳:____________________________________________;
(3)氧气:________________________________________________。
Ⅰ.某研究性学习小组的同学学习了二氧化碳的性质后,对二氧化碳溶于水的过程,有没有发生化学变化?提出实验改进:用如图所示装置进行实验,验证二氧化碳能与水反应(已知氮气的密度小于空气的密度),
操作为:
①从a端通入二氧化碳 ②从分液漏斗中滴加适量水
③从b端通入氮气 ④将石蕊溶液染成紫色的干燥纸花放入广口瓶中
实验操作顺序最合理的是__ _,发生变化的化学方程式为: 。
Ⅱ.另一小组在课外活动时对“二氧化硫能否与水反应生成酸”进行了实验探究。请你参与他们的探究活动,并回答有关问题。
[查阅资料]常温下二氧化硫是一种无色气体,易溶于水。
[假 设]二氧化硫能与水反应生成酸。
[设计实验]
(1)小雨同学将二氧化硫气体通入紫色石蕊试液中,观察溶液颜色的变化。他认为,若紫色石蕊试液变 色,则证明假设成立。
(2)小涛同学认为小雨同学的实验方案不严密。小涛同学用紫色石蕊试液将白色滤纸染成紫色,干燥后做成三朵紫色的小花,然后按下列图示进行实验,在(I)、(Ⅱ)、(Ⅲ)中分别观察到变色和不变色的两种现象。
小涛同学认为,若 (填序号)中的紫色小花变色,则证明假设成立。
[交流反思]小明同学对小涛同学的实验方案提出了质疑,他认为上述实验还不足以证明“二氧化硫和水反应生成了酸”,其理由是 。三位同学讨论后补充了一个实验,使探究活动获得了成功,你认为这个实验应该是 (简述实验步骤和现象)。
[结 论]通过上述实验得出:二氧化硫能与水反应生成酸。
氧气和二氧化碳都是人类赖以生存的气体,因此研究其制法极为重要。
①工业上用分离液态空气的方法制取氧气,主要是利用了氧气和氮气的 不同。二氧化碳的工业制法与实验室制法不约而同地选择了碳酸钙(大理石或石灰石),不仅因为这种原料含有 (填“钙元素”或“碳酸根”),而且来源非常广泛。
②某小组根据实验室制取氧气的方法和思路研究二氧化碳的实验室制法。
【确定反应原理】
Ⅰ.实验室制取二氧化碳的反应原理是(写化学方程式) 。
Ⅱ.甲同学认为:应该选择反应C+O2 CO2制取二氧化碳,乙同学不同意甲的观点,乙同学的理由是(写一条) 。
CO2制取二氧化碳,乙同学不同意甲的观点,乙同学的理由是(写一条) 。
【确定实验装置】
Ⅰ.写出下列编号仪器的名称:③ ;④ 。
Ⅱ.若要制取一瓶二氧化碳气体所需仪器的编号为 。
Ⅲ.实验室制取气体发生装置的选择依据是 ,收集装置的选择依据是 。
| A.反应物状态 | B.气体的密度 | C.反应的条件 | D.气体溶解性 |
【进行制取实验】
Ⅰ.验满二氧化碳气体的方法是 。
Ⅱ.写出检验二氧化碳气体的反应的化学方程式 。
③某同学利用双氧水分解的反应测定双氧水的浓度。他用如图装置进行实验。
Ⅰ.若该反应产生0.01mol氧气,则参加反应的过氧化氢的物质的量为 (列式计算)。
Ⅱ.气体从溶液中逸出时会带出水蒸气,该因素将导致上述实验测定的双氧水的溶质质量分数 (填“偏大”或“偏小”)。