构建知识网络是一种重要的学习方法。右图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为红色固体单质。请回答下列问题: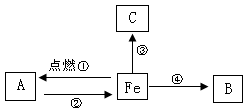
(1)A物质的化学式为 。
(2)B物质的一种用途是 。
(3)反应②还需要的一种反应物是 (填化学式)。
(4)写出反应③的方程式,并注明基本反应类型:
( )。
“孔雀石”的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它是一种重要的铜矿石原料。小明欲从孔雀石中提炼出单质铜。
【查阅资料】(1) 碱式碳酸铜加热易分解,其方程式为:Cu2(OH)2CO3加热2CuO+CO2↑+H20。
(2) 向Cu2(OH)2CO3中加入足量的盐酸,固体完全溶解,有无色气体生成,写出此反应的化学方程式: 。
【设计方案】在实验室中以碱式碳酸铜、铁粉、稀盐酸为原料来制取单质铜。请你仿照下图画出方案二制取铜的流程图,要求:步骤最少。
方案一:
方案二:你设计的方案为
【进行实验】方案一中最后一步:在溶液中加入过量的Fe的实验现象为
【反思】铜锈的主要成分也是碱式碳酸铜,从碱式碳酸铜的化学式[Cu2(OH)2CO3]推知,铜生锈可能与空气中的氧气、水、________________________有关。
以电解食盐水为基础制取氯气、氢氧化钠等产品的工业称为"氯碱工业",它是目前化学工业的重要支柱之一。由于粗盐中含有少量
、
、
等杂质,不符合电解要求,因此必须经过精制。以粗盐为原料的"氯碱工业"流程如下:

回答下列问题:
(1)氯气、氢氧化钠在工业上有广泛的用途。下列关于氢氧化钠的描述中,错误的是。
| A. | 能去除油污,可做厨房清洁剂 | B. | 易溶于水,溶解时放出大量的热 |
| C. | 水溶液能使石蕊溶液变红 | D. | 可用作某些气体的干燥剂 |
(2)操作②的名称是,操作④的名称是。
(3)操作①②间除杂质时所加的三种试剂是
溶液、
溶液、
溶液(均过量),其顺序要求是:
溶液必须在
溶液之(填"前"或"后")加入。有同学提出用溶液代替
溶液可达到同样的目的。
(4)电解饱和
溶液的化学方程式是。
(5)该流程中可以循环利用的物质是。
阅读下面科普短文。
肼(N2H4)又称联氨,有类似于氨的刺鼻气味,贮存时用氮气保护并密封,用途广泛。肼燃烧放热量大且燃烧产物对环境无污染,常用作火箭燃料,点燃时与助燃物质液态N2O4发生反应,生成N2和H2O。高压锅炉水处理时用于脱除氧气以防止锅炉的腐蚀,也可以把锅炉内表面锈蚀后的氧化铁还原为结构紧密的四氧化三铁保护层,减缓锅炉锈蚀。用于烟草、土豆、玉米的贮藏,用于食用盐酸的制造等。熔点1.4℃,沸点113.5℃;有强烈的吸水性,形成水合肼(N2H4·H2O),可以用固体烧碱进行脱水;能吸收空气中的二氧化碳;易溶于水;与液氧接触能自燃;长期暴露在空气中或短时间受热时易发生分解。对眼睛有刺激作用,能引起延迟性发炎,对皮肤和粘膜也有强烈的腐蚀作用。
依据短文内容,回答下列问题:
(1)肼的下列性质中,属于化学性质的是 (填字母序号,下同)。
A.与氧化铁作用 B.易溶于水
C.易分解 D.有刺鼻的气味
(2)肼在常温下为______(填“固态”“液态”或“气态”)。
(3)肼作为火箭燃料燃烧时反应的化学方程式为 。
(4)肼有强烈的吸水性,能吸收空气中的CO2,下列物质中的 也具有这些性质。
A.NaCl B.Ca(OH)2 C.NaOH D.NaHCO3
(5)肼需要密封保存的原因是______。
A、B、C、D、E、F、G是初中化学常见的物质,A在常温下是一种无色液体,D是天然气的主要成分,G是一种重要建筑材料的主要成分,E是一种金属氧化物,与A反应能生成一种常见的碱。它们之间的转换关系如下图所示:

(1)写出下列物质的化学式:A_、D。
(2)写出反应④的化学方程式。
(3)E在日常生活中用途广泛请写出其中一点。
(4)点燃B、D之前一定要。
(5)B是最清洁的燃料,与其它燃料相比其优点有,但是作为燃料暂时还不能广泛使用你认为的原因是:。
一辆有约30吨硝酸的罐车在某厂道路发生侧翻,硝酸泄露,散发出黄色烟雾,流到石灰石地面,发出嘶嘶声,产生大量气泡,泄露出来的硝酸不断流进路边的排水沟,气味十分刺鼻.
(1)由题给信息可知,硝酸的物理性质是 _________ (任写一条)
(2)硝酸见光后,除分解生成二氧化氮气体外,还生成水及占空气体积分数约21%的气体,实验室保存硝酸应密封,遮光保存在棕色瓶内,放在低温阴凉处,硝酸见光分解的化学方程式为 _________
(3)为消除硝酸对环境的污染,对泄露的酸必须处理,经济上合理、对环境污染小的化学处理方法是 ________ .
氯化钙是多用途的干燥剂和建筑防冻剂。实验室里用石灰石和盐酸制备二氧化碳的含酸废液(含有MgCl2、FeCl3等)通过以下途径制得无水氯化钙。
(1)操作I的名称为 ,操作II的名称为 。滤渣 的化学成分有
的化学成分有
。
(2)石灰乳的作用是① ,② ,写出其中1个反应的化学方程式 。
下图是燃气热水器示意图。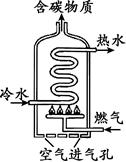
(1)某热水器以天然气为燃气。
①写出天然气完全燃烧的化学方程式_________________________。
②当“空气进气孔”被部分堵塞,燃烧将产生有毒气体M,M的化学式为_______。
(2)1kg不同燃料燃烧产生 和
和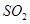 的质量如下表所示。
的质量如下表所示。
①其中较清洁的燃料是______________。使用_________作燃料时最易形成酸雨。
②酸雨形成过程中某一步反应的微观示意图如下:
则该反应的化学方程式为 ,反应中“ ”和“
”和“ ”的质量比为 。
”的质量比为 。
医用氯化钙常用于合成药物。以工业碳酸钙(含少量Fe3+等杂质)为原料生产二水和氯化钙(CaCl2·2H2O)的流程如下图所示。
|
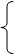
|
滤液…→CaCl2·2H2O
①加盐酸 ② 加Ca(OH)2 ③操作a

 滤渣
滤渣
2012年4月15日,央视《每周质量报告》对“非法厂商用皮革下脚料造药用胶囊”曝光,其制成的胶囊往往重金属铬超标。
(1)重金属的毒性主要是由于它与人体内酶的—SH基结合而产生。误食重金属盐后,可尽快喝适量牛奶或鸡蛋清解毒。牛奶和鸡蛋清富含的营养素是______________。
(2)下图是铬元素在周期表中的一格,你能从该图的数字得到的信息有:_____________(写一条)。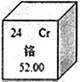
(3)铬是银白色有光泽且硬而脆的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。人们通常在自行车车圈、水龙头等表面镀一层铬,是为了_________。
(4)铬的化合物可用于检测是否酒后驾车,其原理为遇到酒精红色的CrO3转变为绿色的Cr2(SO4)3,在Cr2(SO4)3中铬元素的化合价为___________________。
海水淡化可采用膜分离技术。如图一所示,对淡化摸右侧的海水加压,在其左侧得到淡水。其原理是海水中的水分子可以透过淡化摸,而其他各种离子不能透过。请回答:

(1)采用膜分离技术淡化海水的原理,与化学实验中常见的操作相似。
(2)对淡化膜右侧的海水加压后,海水中溶质的质量分数会(填"增大"、"减小"或"不变")
(3)海水中含有大量的氯化钠,图二是氯化钠的溶解度曲线,据此可知盐场从海水中得到食盐晶体利用的方法是结晶(填"降温"或"蒸发")。
氢氧化钴[Co(OH)2]受热易分解,能与酸性溶液反应,可作涂料和清漆的干燥剂,制备方法为:①Co+2HCl=CoCl2+H2↑,②CoCl2+2NaOH=Co(OH)2↓+2NaCl。下列判断正确的是
| A.钴的金属活动性比铜的弱 | B.①为置换反应,②为复分解反应 |
| C.氢氧化钴的化学性质稳定 | D.氢氧化钴可以干燥氯化氢气体 |
某学校兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究。
【查阅资料】两者的热稳定性:
(1)食用纯碱受热不分解。
(2)食用小苏打270 ℃时完全分解为碳酸钠、二氧化碳、水
【实验探究】
(1)验证两种粉末的稳定性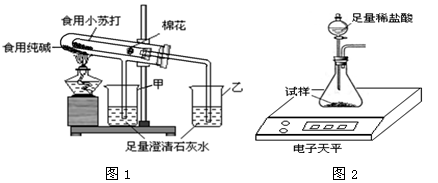
在老师的指导下,该小组按图1所示装置进行实验操作,观察到 (填“甲”或“乙”)烧杯中澄清石灰水变浑浊,小试管中发生反应的化学方程式为 __________ ,装置中棉花的作用是 。写出食用小苏打的一点用途_______________________。
(2)测定食用纯碱粉末的纯度
取食用纯碱粉末试样(假设只含少量氯化钠)22g放入烧杯中,向烧杯中加入200g足量的稀盐酸,充分反应后气体全部逸出,烧杯中剩余物的总质量为213.2g。
①反应生成CO2的质量为 g。
②通过计算确定食用纯碱粉末中Na2CO3的质量分数 (结果保留一位小数,下同)。
③如果测得的结果比实际纯度高,可能的原因是 (答一种即可)。
④求反应后所得溶液中溶质的质量分数(请写出计算过程)。
某化学兴趣小组的同学参照教科书内容,在学校实验室里完成了以下两个实验:
实验一:配制溶质质量分数为6%的NaCl溶液50 g,按如下步骤进行操作:
实验二:称取5.0 g粗盐进行提纯。粗盐除含有NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质。为了有效将粗盐提纯,实验的各步操作流程如下图所示:
请你根据以上信息回答下述问题:
(1)配制50 g溶质质量分数为6%的NaCl溶液,需NaCl______g,水______mL。
(2)NaCl溶解过程中用到了玻璃棒,它的作用是________________。
(3)粗盐提纯时,操作Ⅰ的名称为__________________。
(4)某同学所得精盐比其他同学明显要少,原因可能是____________________。
A.溶解时将5.0 g粗盐一次全部倒入水中,立即过滤
B.蒸发时有一些液体、固体溅出
C.提纯后所得精盐尚未完全干燥
在元旦联欢晚会上,被誉为化学魔术师的晓慧同学为同学们表演了一组化学魔术,在三支盛有液体的玻璃杯中,分别倒入用酒瓶装的一种液体,同学们看到下列奇特现象:A杯中变成了“红葡萄酒”(变为红色);B杯变成了“汽水”(产生大量的气泡);C杯中变成了“牛奶”(有白色沉淀)。请你来揭开魔术秘密:
(1)酒瓶中的液体可能是 。
(2)B杯中产生的气体是 。
(3)写出C杯中发生的化学方程式 。