生活离不开水。净化水的知识在日常生活中有着广泛的应用。
(1)茶杯内的纱网,可将茶叶与茶水分离,便于饮用,该设计利用的原理是相当于 。
(2)自制净水器中常加入 ,用于除去水中的异味和色素。
(3)自来水生产过程中,可用___________方法除去水中不溶性杂质,同时还必须进行消毒. 是一种新型的自来水消毒剂,其中氯元素的化合价为___________。
是一种新型的自来水消毒剂,其中氯元素的化合价为___________。
(4)保护环境、珍爱水资源,是每个公民应尽的责任和义务。下列做法有利于保护水资源的是_____________(填序号)
| A.大量使用化肥农药 | B.工业废水处理达标后排放 |
| C.使用含磷洗衣粉 | D.生活污水直接排放 |
(5)目前部分农村的饮用水主要还是地下水。饮用遭到污染或硬度大的地下水不利于人体健康。为了降低水的硬度,要建议村民在饮用前要___________。
有S2--和S两种粒子,回答:S2--中的“2”表示_____ ________;
S2--和S的质子数______ ___(填相同或不同);已知S2--有16个质子,则其核外共有______个电子;如果硫单质中有一种相对分子质量为128的硫分子,则该单质的化学式为___________。
化学用语是化学学科的专用语言,请用化学用语回答问题:
(1)空气中含量为21%的气体 ; (2)地壳中含量最多的金属元素 ;
(3)氩气 ; (4)两个钠离子
(5)三个铵根离子 。(6)氧化钡中钡元素的化合价 。
(7)根据结构示意图 写出的微粒符号 。
写出的微粒符号 。
(1)含磷洗衣粉中含有Na5PxO10,其洗涤废水的任意排放会污染环境,已知在上述化合物中磷的化合价为+5,则X应为 。
(2)由地壳中含量最多的金属元素和地壳中含量最多的非金属元素组成的化合物的化学式是__________________
(3)已知铁的氧化物中铁与氧元素的质量比为7:3,则其化学式为 ______ 。
下图为一氧化碳还原氧化铜的装置图:
(1)实验过程中,先进行的是 。(填①或②)
①加热 ②.通一氧化碳
(2)A中可看到的现象是: ;反应的反学方 程式为:
B中可看到的现象是: ;反应的反学方程式为:
(3)该装置的不足之处是: 。
俄国化学家门捷列夫在总结前人经验的基础上,通过艰辛的努力,终于提出了现代元素周期表的雏形。下表为元素周期表的部分元素的相关信息,利用下表回答相关问题
(1)请画出16号元素原子结构示意图 化学反应中该原子比较容易 (填“得到”或“失去”)电子变成 (填离子符号)
(2) 表示的是 (填离子符号);
表示的是 (填离子符号);
(3)空气中含量最多的元素和地壳中含量最多的元素和地壳中含量最多的金属元素组成的化合物
(填化学式);
(4)上表中第二、三周期元素最外层电子数的变化规律是 。
为减少污染、提高煤的利用率,可将煤转化为可燃性气体,此过程可认为是碳与水的反应,其微观示意图如下所示:
请写出由图中获取的两点信息:(1) ;(2) 。
下图是氧元素、铝元素在周期表中的部分信息,以及四种粒子的结构示意图。 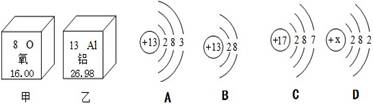
根据图示回答下列问题:
(1)氧原子的原子核内质子数是 ,铝的相对原子质量是 ;
(2)写出甲和乙形成化合物的化学式 ;
(3)粒子B的符号为 ;
(4)D粒子中X= 。
生活离不开水,净化、软化水的知识在日常生活中有着广泛的应用。
(1)茶杯内的纱网,可将茶叶与茶水分离,便于饮用,该设计利用的化学原理是 。
(2)有些村民取浑浊的河水作生活用水,将浑浊的河水用下图所示的简易净水器进行净化。用此装置净化后得到的水属于 (填“纯净物”或“混合物”)。
(3)井水硬度较大,为降低硬度,生活中常用的方法是 。
(4)为了防止水的污染,①抑制水中所有动、植物的生长;②不任意排放工业废水;③禁止使用农药和化肥;④生活污水经过净化处理后再排放。其中可以采用的方法是 (填序号)。
NaOH俗名 、 、 ,其固体暴露在空气中,容易 而使表面潮湿并逐渐溶解,这种现象叫做 ;同时吸收空气中的 而变质,生成 。因此NaOH固体必须 保存。
在碳、一氧化碳、二氧化碳、氧气四种物质中,每一种物质都有不同于其他三种物质的特点,例如:碳:常温常压下是固体,其他三种物质是气体。请根据示例,填空:
(1)一氧化碳:________________________________;
(2)二氧化碳:________________________________;
(3)氧气:____________________________________。
(1)在“水、氮气、稀有气体、明矾”中选择适当的物质填空:
①食品包装袋中防腐的气体是 ;②净化水时用作絮凝剂的是_ ;
③相对分子质量最小的氧化物是 ;④通电时发出不同颜色光的是_____ 。
(2)矿物质水中元素及国标含量如下表所示,请用化学符号填空
①矿物质水中含有的镁元素 ;
②久置的水中溶有一定量的氧气,请表示出2个氧分子 ;
③下表中的一种阴离子 ;
④硫酸钙中钙元素的化合价为+2价 ;
根据如图所示装置回答有关问题:
(1)写出下列仪器名称M ;N
(2)若用装置B排水收集氧气,气体从 (填“a”或“b”)导管通入瓶内;瓶底留少量水进行装置C中的实验,水的作用是 .
(3)对比装置D和C,可以得出关于可燃物燃烧的条件是 .
(4)某同学连接A、E、F进行实验,A中所加药品不同,F中所加药品相同.
①若实验时E中蜡烛熄灭,F中溶液变浑浊,说明A中产生的气体所具有的性质为 .
②若实验时E中蜡烛燃烧更旺,F中溶液变浑浊,则A中反应的化学方程式为 .
③F中溶液变浑浊的化学方程式为 .
(5)某同学用碳酸钠粉末和稀盐酸反应来制取二氧化碳,为了较好地控制反应速率,
可选用的发生装置是 (填字母A或G)。
用 Y 形试管或 Y 形导管完成以下实验。 
(1)图A 中 Y 形试管左侧管中加入无色酚酞试液,右侧管中加入浓氨水,一段时间后,可观察到的现象:______________,用分子的观点解释这一现象:_______________________。
(2)图B 中 Y 形导管平放于桌面,实验中可观察到的现象:________________________,用化学方程式解释以上现象:________________________;若把 Y 形导管固定在铁架台上(如图 C ) , a 管位于上方, b 管位于下方,两石蕊试纸均湿润,可观察到 b 管中试纸变色比 a 管明显,原因是:___________________。
实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色粉末。某兴趣小组的同学对该样品的成分及含量进行了探究。
【提出问题】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含Na2CO3;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3。
则NaOH变质反应的化学方程式为________________________________;
【查阅资料】
碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
【实验探究】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告。
| 实验操作 |
实验现象 |
实验结论 |
| (1)取少量样品溶于水,加入 ; |
白色沉淀产生 |
该反应的化学方程式为 |
| (2)将上述反应后的混合液过滤,取滤液加入 ; |
|
证明猜想Ⅱ成立。 |