鉴别失去标签的五瓶溶液:稀盐酸、稀硫酸、
溶液、
溶液和
溶液。
(1)根据溶液颜色即可确定
溶液。取少量四种无色溶液分别放入四支试管中,再分别滴加
溶液,可鉴别出
溶液和
溶液。鉴别出
溶液的现象是;
(2)另取少量剩余的两种溶液分别放入两支试管中,再分别滴加
溶液,其中一支试管内产生白色沉淀,该反应可用化学方程式表示为,至此,五瓶溶液已全部鉴别出来;
(3)实验结束后,将所有试管中的物质充分混合,过滤除去沉淀,得到无色滤液;取少量无色滤液滴加
溶液,无明显现象,另取少量无色滤液分别与下列物质混合时,一定无明显现象的是。
| A. | 酚酞溶液 |
| B. | |
| C. | |
| D. | 溶液 |
E. 溶液
结合
、
的相关知识,回答下列问题
(1)可用来改变酸性土壤的固体是;
(2)从微观角度看,它们的溶液具有相似化学性质的原因是;
(3)除去
溶液中混有的少量
,可选用的试剂是。
实验设计是化学实验的重要环节。请根据下列实验要求回答相关问题: 【活动与探究一】用对比实验方法探究二氧化碳的性质。

(1)实验一中振荡
个矿泉本塑料瓶,观察到塑料瓶变瘪的程度为
,其中变浑浊的瓶内发生反应的化学方程式为;对比
瓶与(填"
"或"
")瓶的实验现象,可证明
能与
发生反应。
(2)实验二观察到
装置中发生的现象是结论是(用化学方程式表示)。
【活动与探究二】用变量控制方法探究影响物质溶解性的因素。
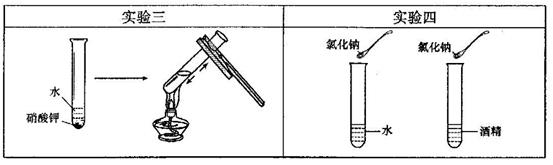
(3)实验三目的是探究对硝酸钾溶解性的影响;实验四是探究溶剂种类对物质溶解性的影响,该实验中需要控制的变量是温度和.
【活动与探究三】定量测定空气中氧气的含量。

(4)实验五中,反应的原理为(用化学方程式表示);装置一比装置二更合理,理由是;
根据下表提供的实验数据,完成下表:
| 硬质玻璃管 的容积 |
反应前注射器中 气体体积 |
反应后注射器中 气体体积 |
实验测得空气中氧气 的体积分数 |
| 30mL |
20mL |
12 mL |
定量实验操作中易产生误差,如果反应前气球中存在气体(其量小于注射器内的空气),而实验后冷却至室温,将气球内的气体全部挤出读数,导致实验测得结果(填"偏小、'偏大"或"无影响")。
化学是一门研究物质的科学,我们一般从物质的存在、性质、制备、用途等方面研究一种物质或一类物质。以金属为例,请你参与其中回答相关问题:
(1)认识金属元素存在:自然界中大多数金属都以化合物的形式存在。
下列矿石的主要成分属于氧化物的是(填字母序号,下同);
A.铝土矿 (主要成分
)
B.钾长石(主要成分
)
C.赤铁矿 (主要成分
)
D.磁铁矿 (主要成分
)
(2)探究金属性质:金属原子容易失去最外层电子,化学性质活泼。图1为探究金属化学 性质的实验,图2是金属化学性质网络图。
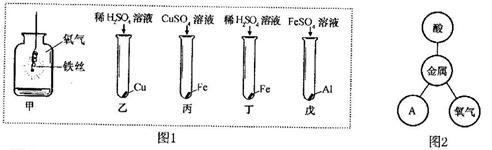
①图1甲中反应现象是丙中反应的化学方程式为;
②图1只有乙中不反应,能得出三种金属活动性及它们和氢元素的位置关系,由强到弱的顺序是(填元素符号);
③依据图1完成金属性质网络,图2中的A属于(填物质类别);
(3)认识金属的制备:工业上常采用还原法、置换法、电解法制备金属。
用一氧化碳还原赤铁矿冶铁反应的化学方程式为
(4)金属在生产生活中应用广泛。
①下列金属制品的用途,利用其导电性的是
| A. |
铁锅 |
B. |
铜导线 |
C. |
铝箔 |
D. |
黄金饰品 |
②合金性能优于单一金属,因而被广泛应用。焊锡(主要含锡、铅)与其组成金属相比
具有的特性,可用于焊接电子元件;
③ 金属是一种有限资源,需要保护和回收利用。
黄铜(铜锌合金)用作弹壳的制造。现有一批使用过的,锈迹斑斑的弹壳,处理这批弹壳可以制得硫酸锌和铜,其主要流程如下所示。
【收集资料】弹壳上的锈主要为
,能与稀硫酸反应得到硫酸铜溶液;弹壳中其他杂质不溶于水、也不参加反应。
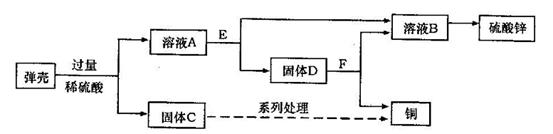
a.写出弹壳上的锈与稀硫酸反应的化学方程式。
b.固体D为。
神奇的化学变化﹣﹣光合作用与燃烧反应如图为光合作用和木柴燃烧过程中,部分物质参与循环的示意图.

请据图并结合你学过的知识,回答下列问题:
(1)从物质组成的角度看,葡萄糖和纤维素均属于(填"无机物"或"有机物").
(2)从物质转化的角度看,光合作用及葡萄糖转化为纤维素属于(填"物理"或"化学")的变化.光合作用的化学方程式为碳不完全燃烧的化学方程式为.
(3)从能量转化的角度看,绿色植物光合作用时能量转化的方式是,而木炭燃烧时能量转化的方程式是.
(4)在图中光合作用与燃烧反应过程中参与循环的元素有.
小丽同学建立了微型化学实验室,她收集的物质有:①镁条 ②氧化镁 ③氢氧化钠 ④小苏打 ⑤ 醋酸 ⑥葡萄糖等,其中属于碱的物质是(填化学式),属于有机化合物的是(填序号),在食品工业中作为发酵粉主要成分的物质是(填序号)。
不同类别物质间存在一定关系。镁、氧化镁和醋酸之间的变化关系如下图所示("-"表示相连的两种物质能发生反应,"→"表示某种物质可转化为另一种物质)。回答下列问题:

(1)甲物质是(填完整名称);
(2)写出"乙→丙"反应的化学方程式。
请分析、比较以下几组化学反应,得出结论。
| 组别 |
化学方程式 |
结论 |
| I |
|
反应物相同,生成物不同, 原因。 |
| II |
|
反应物相同,生成物不同, 原因。 |
| III |
|
反应物相同,生成物不同, 原因。 |
| IV |
(反应缓慢) (反应迅速) |
反应物相同,反应速率不同, 原因。 |
| 实践与应用 |
科学探究正努力实现对化学反应的控制,很多化学家致力于研究二氧化碳的"组合转化"技术,把过多二氧化碳转化为有益于人类的物质。若让二氧化碳和氢气在一定条件下反应,可生成一种重要的化工原料,反应的化学方程式如下: ,推断X的化学式是。 |
图中A、B、C、D、E是初中化学常见的五种不同类别的物质. E是导致溫室效应的一种气体,图中"﹣"表示相连物质能发生化学反应,"→"表示两种物质间的转化关系(部分反应物、生成物及反应条件省略).

(1)写出物质E的一种用途;
(2)物质C与E反应的化学方程式是;
(3)写出图中一个属于中和反应的化学方程式。
(4)A与B反应的微观实质是。
下列实验设计能达到实验目的是( )
| 选项 |
实验目的 |
实验方案 |
| A |
检验某气体是否为二氧化碳 |
用燃着的木条 |
| B |
稀释浓硫酸 |
将水缓慢加入浓硫酸中,并搅拌 |
| C |
区分氧化钙与碳酸钙 |
取样品,加入适量水 |
| D |
除去K2S04溶液中的K0H |
加入适量稀盐酸 |
物质的结构决定性质,下列有关说法错误的是()
| A. | 过氧化氢与水化学性质不同的原因是由于分子构成不同 |
| B. | 盐酸与硫酸化学性质相似的原因是在水溶液中都含有 |
| C. | 氢氧化钠与氢氧化钙化学性质相似的原因是在水溶液中都含有 |
| D. | 金刚石与石墨物理性质差异较大的原因是由于碳原子的结构不同 |
达州市钢铁厂用于炼铁的石灰石主要成分是
,课外小组同学取来该石灰石样品
,粉碎后,将
一定溶质质量分数的稀盐酸分5次加入到该样品中,所测数据如下(杂质不与稀盐酸反应,也不溶于水):
| 次数 |
一 |
二 |
三 |
四 |
五 |
| 加入稀盐酸的质量/g |
25 |
25 |
25 |
25 |
25 |
| 剩余固体的质量/g |
19 |
14 |
9 |
4 |
4 |
(1)石灰石样品中
的质量为;
(2)第次恰好完全反应;
(3)求最后所得溶液中
的质量分数(写出计算过程,结果保留到0.1%)。
(某研究性学习小组同学将钠置于充满
的集气瓶中进行燃烧,反应后集气瓶内有黑色固体和白色固体生成。
该小组经分析得知,白色固体中不可能有
,原因是。他们对白色固体成分进一步探究。
【提出问题】白色固体是什么?
【查阅资料】①
②钠能与水反应生成
和
【猜想与假设】Ⅰ.白色固体是
Ⅱ.白色固体是
Ⅲ.白色固体还可能是
【设计实验】
| 实验步骤 |
实验现象 |
实验结论 |
|
| 取少量白色固体于试管中,加入适量水振荡。 |
固体全部溶解 |
||
| 向上述所得溶液中加入过量
溶液,静置。 |
产生白色沉淀 |
||
| 取静置后的上层清液于试管中,滴加无色酚酞试液。 |
试液不变色 |
白色固体是 。 |
【得出结论】①通过上述实验,三个猜想中猜想成立。
②钠在
中燃烧的化学方程式为。
【反思与交流】钠着火,可以选用的灭火物质是。
A.水 B.干沙土 C.二氧化碳
(4分)甲、乙、丙、丁四种物质在一定条件下能发生如下反应:甲+乙→丙+丁。
(1)若甲、丙为单质,乙、丁为化合物,则上述反应的基本反应类型为。
(2)若甲、乙、丙、丁均为化合物,丙为不溶于稀
的白色沉淀,写出一个符合要求的化学方程式:。
(3)若甲、乙、丙均为化合物,丁为单质,则丁可能为。
利用化学变化可以制备新物质.
是一种无色、无臭的气体,密度比空气略小,难溶于水,易于血红蛋白结合,具有可燃性.请结合所学知识和CO的相关信息回答下列问题:
(1)下列两个反应都能生成
,从实验室制备气体的思路分析,实验室制备
选择反应②而不用①的理由是(任选一个角度回答)
①炽热的焦炭和水蒸气反应:
②草酸晶体和浓硫酸供热:
(2)某同学设计下列装置制备、提纯
,并用
来还原氧化铜.请根据如图回答:

①写出一氧化碳还原氧化铁的化学反应方程式。
②该同学的设计存在的一处明显缺陷是.用改进后装置进行实验,在点燃E处酒精灯之前,必须进行的一项操作是(从实验安全角度考虑)。
③装置
的作用是,
中发生反应的化学方程式为。
④证明一氧化碳能还原氧化铁的实验现象是:装置
中固体颜色的变化为,
中,
中。