用久的热水瓶内胆有一层水垢【主要成分是CaCO3和Mg(OH)2】。兴趣小组为了解具体成分进行了实验。他们取样品25克放入质量为100克的锥形瓶中,置于电子天平上,往瓶内加入150克稀盐酸时,恰好完全反应(样品中的杂质不与稀盐酸反应),此时天平示数如图。对所得混合物进行过滤、洗涤、干燥、称量,得到固体4.2克。请回答下列问题:
(1)恰好完全反应时,溶液中的溶质为 (填化学式)。
(2)样品中CaCO 3的质量分数是多少?
(3)反应结束时溶液中MgCl 2的质量分数是多少?(精确到0.1%)。

尿素[CO(NH 2) 2]是一种常见的氮肥,工业上制备反应如下:
CO 2+2NH 3 CO(NH 2) 2+H 2O,请计算:
(1)尿素中氮元素的质量分数。
(2)生产6t尿素,理论上需要氨气的质量是多少?
科学研究中,常通过对实验数据的分析计算,得出某未知物质的相对分子质量,从而推测该物质的分子式。某科研小组经反复实验,发现2A+3B=2C+4D中,3.2gA恰好和4.8gB完全反应,生成4.4gC.请问:
(1)同时生成D的质量为 g。
(2)若D的相对分子质量为18,求A的相对分子质量(写出计算过程)。
早在西汉时期的《淮南万毕术》中就记载"曾青得铁则化为铜",成为现代湿法冶金的先驱。现有含1.6kg硫酸铜的工业废液,加入铁粉回收铜,请计算:
(1)硫酸铜中铜元素的质量分数。
(2)理论上与硫酸铜反应消耗铁粉的质量。
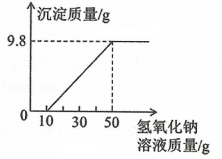
向盛有100g稀硫酸和硫酸铜混合溶液的烧杯中滴加氢氧化钠溶液至过量,过滤、烘干并称量沉淀的质量。该反应过程如图所示。请按要求回答问题:
(1)滤液中的溶质是 (填化学式)。
(2)计算原混合溶液中硫酸铜的质量。
(3)氢氧化钠溶液的溶质质量分数。
科学家尝试通过多种途径减少CO 2的排放,或将CO 2转化为有用的物质。其中一种途径是利用NaOH溶液来"捕捉"CO 2,并将CO 2储存或利用,反应流程如图所示。

(1)反应分离室中分离物质的操作是 。
(2)上述反应流程中,可循环利用的物质是 。
(3)若反应分离室中有溶质质量分数为10.6%的Na 2CO 3溶液100千克,求完全反应后,理论上可生成CaCO 3的质量(要求根据化学方程式计算)。
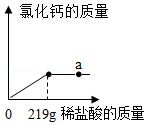
实验室模拟高温煅烧石灰石的方法制取二氧化碳,取35g石灰石样品(假设杂质受热不分解且不与酸反应),煅烧一段时间恢复到室温,测得生成11g二氧化碳。向剩余固体中逐滴加入某盐酸至不再反应为止,又生成2.2g二氧化碳,加入盐酸的质量与生成的氯化钙质量关系如图:
(1)石灰石样品的质量分数是 (结果保留一位小数,下同);
(2)a点溶液的pH 7(填“<”“>”或“=”);
(3)求所加盐酸的溶质质量分数(写出计算过程)。
小嘉发现:向碳酸钠溶液中倾倒稀盐酸,很快就产生了气泡:向碳酸钠溶液中逐滴加入稀盐酸,滴加一定量后才有气泡产生。查阅资料:向碳酸钠溶液中逐滴加入稀盐酸,先发生的反应是Na2CO3+HCl═NaCl+NaHCO3;当Na2CO3全部转化成NaHCO3后,再发生反应NaHCO3+HCl═NaCl+H2O+CO2↑。为此他用如图所示装置进行了如下实验:
步骤一:在广口瓶中加入10克溶质质量分数为10.6%的碳酸钠溶液,用注射器向瓶中缓慢注入一定量的溶质质量分数为7.3%的稀盐酸,观察到瓶内无明显现象; 步骤二:继续用注射器向瓶中注入稀盐酸,一段时间后观察到瓶内连续产生气泡,烧杯中澄清石灰水?。 |
(1)步骤二中,观察到烧杯中澄清石灰水 。
(2)上述实验中,加入稀盐酸多少克后,才开始产生二氧化碳? 。
(3)向一定量碳酸钠溶液中无论是倾倒还是逐滴加入足量的稀盐酸,完全反应后产生二氧化碳质量是相同的,其本质原因是什么? 。

某兴趣小组在实验室发现盛有固体氢氧化钠的试剂瓶破裂瓶盖处有"白毛"状物质(如图),根据所学知识,他们推断"白毛"状固体物质中含有碳酸钠,依据是 。他们取5g白色固体,加水配成20g溶液倒入烧杯中,将40g氯化钡溶液分成四等份,分4次加入烧杯中,充分反应后测得数据如下表:
| 实验次数 |
1 |
2 |
3 |
4 |
| 加入氯化钡溶液的质量/g |
10 |
10 |
10 |
10 |
| 烧杯中所得溶液的质量/g |
28.03 |
36.06 |
44.09 |
54.09 |
(1)第 次实验,加入的氯化钡与碳酸钠恰好完全反应。
(2)求5g白色固体中碳酸钠的质量。(写出计算过程,结果保留两位小数)

实验室用含杂质的锌(也称粗锌)与盐酸反应制取氢气,取8.0g含杂质的锌粒于烧杯中(所含杂质不溶于水,也不与酸反应),向其中加入73.0g稀盐酸,恰好完全反应后烧杯内剩余物质的质量为80.8g。计算:
(1)生成氢气的质量 g。
(2)求稀盐酸的溶质质量分数(请写出计算过程)。
某炼钢厂每天需消耗5000t含Fe2O376%的赤铁矿,该厂理论上可日产含Fe 98%的生铁的质量是多少?
化学兴趣小组要测定制作叶脉书签所用氢氧化钠溶液的浓度。取40g该氢氧化钠溶液于锥形瓶中,加入数滴酚酞溶液后再滴加质量分数为10%的稀硫酸,当锥形瓶中液体由红色恰好变成无色时,消耗稀硫酸的质量为49g。试计算该氢氧化钠溶液中溶质的质量分数。
为测定某赤铁矿中Fe2O3的含量,取10g该赤铁矿样品于烧杯中,向其中加入100g稀盐酸,恰好完全反应,测得剩余固体的质量为2g。(杂质不溶于水也不与酸反应)
请完成下列分析及计算:
(1)10g样品中杂质的质量为 g。
(2)计算稀盐酸中溶质的质量分数。
钼是一种重要的金属,用它制成的合金有良好的机械性能,在工农业生产和国防上都有广泛的用途。如图是利用钼矿石(主要成分为MoS 2)制备金属钼的流程图:
信息:MoO 3+3H 2 Mo+3H 2O

请回答下列问题:
(1)反应①常将钼矿石粉碎,目的是 ;MoO 3中钼元素的化合价为 。
(2)操作Ⅰ的名称是 ;常用NaOH溶液吸收反应①的尾气,化学方程式为 。
(3)制得19.2吨金属钼,理论上至少需含MoO 380%的粗产品多少吨?请写出计算过程。
注:粗产品杂质中不含钼元素
某课外兴趣小组的同学取14g大理石样品(主要成分是CaCO3)于烧杯中,将50克稀盐酸分成5次加入到烧杯中充分反应(已知大理石样品中其余成分不溶于水,也不与稀盐酸反应),得到如下数据:
次数 |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
加入稀盐酸的质量/g |
10 |
10 |
10 |
10 |
10 |
烧杯中剩余物的总质量/g |
22.8 |
31.6 |
40.4 |
49.6 |
59.6 |
试计算:
(1)实验过程中生成气体的总质量 g;
(2)实验最终所得溶液中CaCl2的质量分数(写出计算过程);
(3)第4次加入10g稀盐酸所产生气体的质量 g。