在催化剂的作用下,用O 2将HCl转化为Cl 2,可提高效益,减少污染.
(1)写出反应Ⅰ的化学方程式 ;
(2)反应Ⅱ所属基本反应类型为 ;
(3)钠在氯气中燃烧生成氯化钠,若4.6g钠完全转化为氯化钠,至少需要氯气的质量是多少?

将12.5g混有二氧化锰的氯酸钾固体加热至质量不再减少,冷却后称量固体的质量为7.7g。
(1)反应时生成氧气的质量为 g。
(2)计算反应前固体中二氧化锰的质量分数(要求写出计算过程)。
掌握科学的研究方法,探索化学世界的奥秘.
(1)分类是学习化学的重要方法之一.
①生活中,常会接触到下列物质:
A.铜丝 B.甲烷 C.过氧化氢 D.碘酒
其中属于混合物的是(填字母,下同) ,属于氧化物的是 .
②根据物质在转化过程中的特点,可将化学反应分为化合反应,分解反应、置换反应和复分解反应四种基本反应类型,下列转化不属于这四种基本反应类型的是 .
A.生石灰与水反应 B.一氧化碳还原氧化铁 C.中和反应
(2)实验是学习化学的一条重要途径,实验室中可用KClO 3在MnO 2催化下受热分解制取氧气,并将反应后的混合物进行分离回收,实验操作如图所示(MnO 2难溶于水)

①图A中试管口略向下倾斜的原因是 ,图B操作中玻璃棒的作用是 .
②图C操作中的一处明显错误是 ,图D操作中,当看到 ,停止加热.
(3)质量守恒定律是帮助我们学习的认识化学反应实质的重要理论.
①下列表述正确的是
A.蜡烛燃烧后质量减小,说明质量守恒定律不是普遍规律
B.每32g S和32g O 2完全反应后,生成64g SO 2
C.在化学反应aA+bB=cC+dD中一定有:a+b=c+d
②有机化合物R与足量氧气置于密闭容器中充分反应生成CO 2和H 2O,实验测得反应前后物质的质量如下表:
| |
R |
O 2 |
CO 2 |
H 2O |
| 反应前质量/g |
46 |
128 |
0 |
0 |
| 反应后质量/g |
0 |
32 |
x |
54 |
则x= ,已知参加反应的物质R与氧气的分子个数之比为1:3,则R的相对分子质量是 .
碳及其氧化物性质的应用。
(1)如图所示,向盛有红棕色二氧化氮气体的集气瓶里投入几小块烘烤过的木炭,红棕色消失,说明木炭具有 能力,其原因是木炭具有 的结构。
(2)在书写具有保存价值的档案时,规定应使用碳素墨水,原因是 。
(3)将一定质量的金刚石在足量的氧气中充分燃烧,固体全部消失,写出反应的化学方程式 ;将生成的产物用足量的氢氧化钠溶液来充分吸收并测定其质量,当金刚石的质量恰好等于 时,则可证明金刚石是由碳元素组成的单质。
(4)在实验室里,检验二氧化碳一般用澄清石灰水,而吸收二氧化碳常用氢氧化钠溶液,理由是 。
(5)写出碳在高温时还原氧化铜的化学方程式,并计算要使80g氧化铜完全还原,需要碳的质量至少是多少?(在答题卡上写出计算过程)
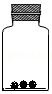
向160g硫酸铜溶液中,逐滴加入40g NaOH溶液,恰好完全反应,生成4.9g沉淀,回答下列问题:
(1)恰好完全反应后,溶液的质量为 g.
(2)将反应结束后的混合物过滤,滤液中溶质是 (填化学式).
(3)求原硫酸铜溶液中溶质的质量分数(写出计算过程)
H2SO4是一种重要的化工原料。
(1)H2SO4溶液的pH 7(填“>”、“<”或“=”),请写出用pH试纸测定稀硫酸pH的正确方法 ;
(2)浓硫酸有吸水性,常用作某些气体的干燥剂,下列气体不能用浓硫酸干燥的是 (填写序号);
①H2
②CO2
③NH3
④HCl
(3)实验室常用亚硫酸钠固体(Na2SO3)和70%左右的硫酸溶液发生复分解反应制取SO2,请写出该反应的化学方程式: ;
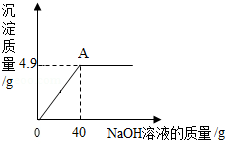
(4)向160g含有H2SO4和CuSO4的混合溶液中逐滴加入NaOH溶液至过量,产生的沉淀质量与加入NaOH溶液质量的关系如图所示,请写出b点对应溶液的溶质 (填写化学式),原混合溶液中CuSO4的质量分数是 。

为测定某溶液中氢氧化钠的质量分数。某同学取50g氢氧化钠溶液与50g硫酸铜溶液混合,恰好完全反应。过滤,所得滤液的质量为90.2g。
求(1)反应后生成沉淀的质量为 g
(2)50g氢氧化钠溶液中溶质的质量分数。
铁的冶炼与利用是学习和研究化学的重要课题。
Ⅰ.铁的冶炼。竖炉炼铁的工艺流程如图1所示。
4燃烧的作用是
(2)写出“还原反应室”中炼铁的一个反应的化学方程式 。
422242的质量(m)范围是 。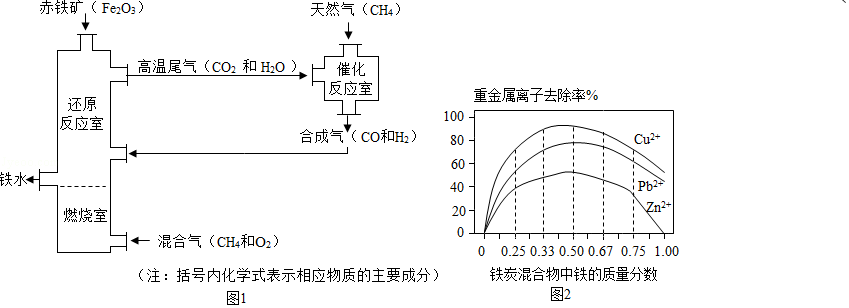
323232的铜冶炼废水。在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中重金属离子的去除率,实验结果如图2所示。
2+2+2+不能被除去,其原因是 。
(2)铁炭混合物中铁的质量分数为0时,也能除去水中少量的重金属离子,其原因是 。
(3)处理效果最好时,铁炭混合物中的铁的质量分数为 。
如图2为某钙片的商品标签,为测定钙片中钙元素的质量分数(假设钙片中其他物质不含钙元素,且不溶于水,也不与任何物质发生反应),某化学兴趣小组取20片钙片,进行如下实验:

(1)上述实验过程中发生反应的化学方程式为 。
(2)根据已知条件列出求解所加的稀盐酸中溶质质量(x)的比例式 。
(3)用36.5%的浓盐酸配制100g上述稀盐酸,所需浓盐酸的质量为 。
(4)钙片中钙元素的质量分数为 。
(5)若向滤液中加入5.4g水,所得溶液中溶质的质量分数为 。
(6)工厂生产钙片时若需碳酸钙120t,理论上需含氧化钙84%的生石灰的质量为 。
水是常用溶剂,某同学进行如图实验。
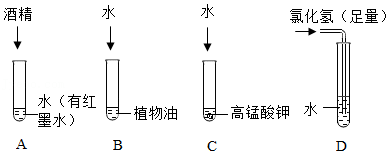
(1)倾斜A试管,沿内壁缓缓加入乙醇,不振荡,现象是 。
(2)实验可知,溶质状态可以是 。
(3)实验结束后,用洗涤剂洗净B试管,原理是 。
(4)C、D试管的废液倒入废液缸中产生了黄绿色气体,查阅资料可知:2KMnO4+16HCl(浓)═2KCl+2X+5Cl2↑+8H2O,X的化学式为 。
(5)询问老师得知用2NaOH+Cl2═NaCl+NaClO+H2O可处理Cl2。根据化学方程式计算,处理0.142g Cl2至少需NaOH的质量是多少?
戊二醛(C5H8O2)是新一代消毒剂,在防控新冠肺炎疫情的过程中被广泛使用。回答下列问题:
(1)戊二醛的相对分子质量为 。
(2)戊二醛中含碳的质量分数为 。
(3)10g戊二醛恰好完全燃烧需要 g氧气。
对金属材料的研究,在人类发展的历史长河中起着非常重要的作用。
(1)金属的化学性质。
完成下列反应的化学方程式:
①镁与氧气反应 。
②锌与盐酸反应 。
③铁与硫酸铜溶液反应 。
(2)金属的获得。
①金属氧化物加热分解。
加热氧化银得到银和氧气,写出该反应的化学方程式 。
②一定条件下,金属化合物与一些具有还原性的物质发生反应。在高炉内,把铁矿石冶炼成铁的主要反应原理是 。写出氢气还原氧化铜的化学方程式,并计算若80g氧化铜与氢气完全反应生成铜,理论上最多可得到铜的质量是多少?(在答题卡上写出计算过程)
③电解法冶炼。
工业上可以利用电解熔融氯化钠得到钠和氯气,该反应的基本反应类型是 。
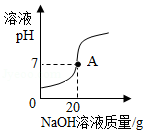
实验室中稀硫酸因标签破损,需测定其质量分数。某化学兴趣小组的同学取该稀硫酸样品50g,逐滴加入质量分数为16%的NaOH溶液,溶液的pH随加入NaOH溶液质量的变化如图所示。
(1)图中A点时溶液中溶质的化学式是 。
(2)求稀硫酸中溶质的质量分数(写出计算过程,计算结果精确到0.01%)。
为测定某工厂排放的废水中氢氧化钠的含量,化学兴趣小组将100g该废水与50g硫酸铜溶液混合恰好完全反应,得到4.9g沉淀。请计算这一废水中氢氧化钠的质量分数。