小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中碳酸钙的质量分数进行检测,采用如下办法:取用8g这种石灰石样品,把40g稀盐酸分4次加入,测量过程所得数据见下表(已知石灰石样品中含的杂质不溶于水,不与盐酸反应)。
| 序号 |
加入稀盐酸质量(g) |
剩余固体质量(g) |
| 第1次 |
10 |
5.5 |
| 第2次 |
10 |
m |
| 第3次 |
10 |
1.2 |
| 第4次 |
10 |
n |
请计算:(1)表中m的数值为 ;n的数值应该为 ;
(2)样品中碳酸钙的质量分数是 ;
(3)通过计算,求反应中生成二氧化碳气体的质量。
为了测定某纯碱样品中碳酸钠的质量分数,取该样品与足量稀盐酸在烧杯中反应,有关实验数据如下表。
| 反应前 |
反应后实验数据 |
||
| 烧杯和稀盐酸的质量/g |
120 |
烧杯和其中混合物的质量/g |
127.6 |
| 纯碱样品的质量/g |
12 |
请计算:(1)该反应生成二氧化碳的质量为 g。
(2)该纯碱样品中碳酸钠的质量分数为多少。(请写出计算过程)
为测定一瓶失去标签的过氧化氢溶液的溶质质量分数,某同学取50.0g过氧化氢溶液放入烧杯中,然后加入2.0g二氧化锰,等不再放出气体,称得烧杯中剩余物质的总质量为50.4g.计算:
(1)过氧化氢中氢元素和氧元素的质量比为 .(2分)
(2)此过氧化氢溶液的溶质质量分数.(写出计算过程)
某兴趣小组按下图所示装置制取二氧化碳,并检验二氧化碳的性质:
(1)若用装置B来证明二氧化碳能与水反应生成碳酸,B中除有少量水外,还应加入的试剂是 ,当①、②导管口连接时,B中看到的实验现象是 ,反应的化学方程式是 。
(2)他们从我市一古建筑维修现场搜集了一些旧墙灰,通过查阅资料得知:古建筑旧墙灰的主要成分是碳酸钙。他们称取了12.0g旧墙灰放入烧杯中,并加入足量稀盐酸(假设杂质不参与反应,不考虑H2O、HCl的逸出)。反应开始时,烧杯及所盛物质的总质量为300.0g。实验数据记录如下:
| 反应时间/min |
0 |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
16 |
18 |
| 烧杯及所盛物质的总质量/g |
300.0 |
299.0 |
298.0 |
297.2 |
296.5 |
296.0 |
295.7 |
295.6 |
M |
295.6 |
①以该小组因故没有记录反应时间为16min时的数据M,由表中数据推测,M=_______g
②反应生成二氧化碳的总质量为__________________(列出算式)。
③旧墙灰中碳酸钙的质量分数(写出计算过程)。
钙是维持人体正常功能所必需的元素。下图所示为“迪巧”钙片说明书的一部分。取1片钙片,放入盛有10g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应)。烧杯内物质质量变为11.56g。
试计算:
(1)除具有补钙作用,钙片中的CaCO3还有 作用。
(2)生成二氧化碳的质量为 ;
(3)所用稀盐酸中溶质的质量分数。
(5分)某工厂利用废铁屑与废硫酸起反应来制取硫酸亚铁。现有废硫酸49 t(H2SO4的质量分数为10%),与足量废铁屑起反应,可生产硫酸亚铁的质量是多少?(答卷纸上写清计算过程)
实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如下表:
| |
气体发生装置内物质的总质量/g |
| 反应前 |
35.6 |
| 反应后 |
34.8 |
(1)反应中二氧化锰的作用是_____________________。
(2)反应生成氧气的质量为_______________g(结果精确到0.1g,下同)。
(3)计算参加反应的过氧化氢的质量。
某兴趣小组为了验证质量守恒定律,在烧杯中盛有20g溶质质量分数为20%的氢氧化钠溶液试管内装有20g硫酸铜溶液,如图所示,放于天平上称量,此时天平平衡。然后将试管内药品倒入烧杯内(试管不取出),恰好完全反应,试根据要求,回答下列问题: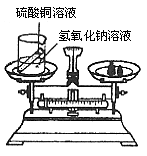
(1)写出实验过程中观察到的一项实验现象:________________________________________________。
(2)反应结束后,天平指针会__________ (填“偏左”“偏右”“不发生偏转”之一)。
(3)试计算恰好完全反应时所得不饱和溶液的质量。(精确到0.1g)
有一种石灰石样品的成分是CaCO3和SiO2(已知SiO2既不溶于水也不与盐酸反应)。课外小组为了测定该石灰石样品中碳酸钙的质量分数,将一定量的石灰石样品将其敲碎后放入烧杯中,再取100 g稀盐酸分4次加入烧杯中,每次均充分反应。实验数据记录如下:
| 次数 |
第1次 |
第2次 |
第3次 |
第4次 |
| 加入稀盐酸质量 /g |
25 |
25 |
25 |
25 |
| 反应后烧杯中物质的总质量 /g |
35.2 |
58.4 |
82.6 |
107.6 |
求:(1)将石灰石样品敲碎的主要目的是_______________________________________.
(2)第2次加入稀盐酸充分反应后,生成二氧化碳的质量是 g。(不包括第一次加
入稀盐酸充分反应生成的二氧化碳)
(3)该石灰石样品中碳酸钙的质量分数(结果保留一位小数)
(4分)100g的稀硫酸与13g的锌正好完全反应,请计算:
(1)生成氢气的质量(结果精确到0.1g)
(2)反应后所得溶液中溶质质量分数(结果精确到0.1%)。
下图是某厂生产的加钙食盐包装标签上的部分文字说明,请仔细阅读并计算:
为了测定此食盐中的钙元素含量,取10g这种食盐溶于水,加入足量的稀盐酸,生成0.132g二氧化碳,请计算此加钙食盐中钙元素的质量分数是否达标。(注:成分中只有碳酸钙与盐酸反应)
小明在实验室里加热31.6g高锰酸钾制取氧气,完全反应后剩余固体质量为28.4g。将剩余固体溶解、过滤、烘干、称量,回收二氧化锰。请计算:
(1)生成氧气的质量为 g。
(2)回收过程中溶解和过滤均用到玻璃棒,它们的作用分别是 、 。
(3)回收得到二氧化锰的质量。(写出计算过程)
将Cu﹣Zn合金样品20g放入足量稀硫酸中,所产生氢气的质量与反应时间的关系如图所示.试计算: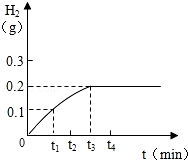
(1)原样品中所含锌的质量.
(2)实验测得20g该样品与154.7g某稀硫酸恰好完全反应,求此时所得溶液中溶质的质量分数.
有400 t含 质量分数为80%的赤铁矿石,最多可炼出含碳和其他杂质为3%的生铁多少吨?
质量分数为80%的赤铁矿石,最多可炼出含碳和其他杂质为3%的生铁多少吨?