实验室用过氧化氢溶液在二氧化锰催化下制取氧气,现已制得氧气64g,则消耗过氧化氢的质量为多少?
某工厂从1000kg铝土矿(主要成分是Al 2O 3)冶炼得到270kg铝。反应的化学方程式是:2Al 2O 3(熔融)  4Al+3O 2↑。请计算。
4Al+3O 2↑。请计算。
(1)Al 2O 3中,Al、O原子个数比是 。
(2)列式计算该铝土矿中Al 2O 3的质量分数。
将15.8 g高锰酸钾放入试管中加热制取氧气,充分反应至不再产生气体为止。
计算:剩余固体物质的总质量是多少克?(已知:2KMnO4 K2MnO4+MnO2+O2↑)
K2MnO4+MnO2+O2↑)
食用小苏打含有 NaHCO 3外还含有少量NaCl.为了测定某食用小苏打中NaHCO 3的质量分数,某同学做了如下实验:称取一定量该样品于烧杯中,加水使其完全溶解,得到104.4g溶液,再向其中滴加100g稀盐酸,恰好完全反应时得到200g溶质质量分数3.1%的不饱和溶液。(反应的化学方程式为:NaHCO 3+HCl═NaCl+H 2O+CO 2↑)请计算:
(1)NaHCO 3中碳、氧元素的质量比为 ,
(2)生成CO 2的质量为 g,
(3)该食用小苏打中 NaHCO 3的质量分数(写出计算过程)。
(3分)宇宙飞船内,宇航员所呼出的气体要通过盛有氢氧化锂(IJOH)的过滤网,以除去所含的二氧化碳,其反应方程式为:2LiOH+CO2 = Li2CO3 + H2O 。若过滤网内含有氢氧化锂96g,计算最多可吸收二氧化碳的质量。
氯可形成多种含氯酸盐,广泛应用于杀菌、消毒及化工领域。实验室中制备KClO3的化学反应方程式为3Cl2+6KOH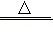 5KCl+KClO3+3H2O。若用Cl2与200g的KOH溶液恰好完全反应,反应后溶液质量为221.3g。计算:
5KCl+KClO3+3H2O。若用Cl2与200g的KOH溶液恰好完全反应,反应后溶液质量为221.3g。计算:
(1)参加反应的氯气的质量为 g。
(2)所用KOH溶液中溶质的质量分数是多少?
某盐酸中混有少量的MgCl 2,小明为了测定该盐酸混合液中HCl的质量分数,进行如图实验:

请结合如图实验数据,完成以下计算:
(1)HCl中氢、氯元素质量比为 (填最简整数比);
(2)坐标中a的数值为 ;
(3)所加NaOH溶液的溶质质量分数为 ;
(4)该盐酸混合液中HCl的质量分数(写出计算过程)。
某化学兴趣小组欲测定某石灰石样品中碳酸钙的质量分数,先将10g样品放入烧杯中,再把100g稀盐酸分5次加入该样品中(该实验条件下,杂质不与酸反应,也不溶解于水,忽略稀盐酸挥发),得实验数据如表格。
稀盐酸的质量 |
充分反应后剩固体的质量 |
第一次加入20g |
8g |
第二次加入20g |
6g |
第三次加入20g |
4g |
第四次加入20g |
2g |
第五次加入20g |
2g |
请计算;
(1)10g石灰石样品中碳酸钙的质量分数是 。
(2)求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)。
孔雀石的主要成分是Cu2(OH)2CO3,还含有Fe2O3、Al2O3、SiO2杂质,用该矿石制备Cu的流程如图所示(部分产物略去):
 (1)过程①中,操作a是溶解和 ,还有一种气体产物是 ,滤液X中含有的金属阳离子为 。
(1)过程①中,操作a是溶解和 ,还有一种气体产物是 ,滤液X中含有的金属阳离子为 。
(2)过程①中硫酸略过量,则过程②调pH除杂的最佳试剂是 (选填“CuO”或“Na2CO3”)。
(3)下列关于制取铜的两种方案的说法,正确的是 。
A.“方案一”得到的铜产品更纯
B.“方案一”不存在消耗能量的问题
C.“方案二”需考虑废气污染的问题
D.“方案二”得到纯铜的产率更高
(4)过程③发生的反应:2CuSO4+2H2O 2Cu+O2↑+ (补充完方程式),当收集到800t氧气时,产生Cu的质量是多少?(写出必要的计算过程)
2Cu+O2↑+ (补充完方程式),当收集到800t氧气时,产生Cu的质量是多少?(写出必要的计算过程)
某补钙片的主要成分为CaCO3,每片钙片重0.5g(假设钙片中其他成分不含钙元素,不溶于水且不与任何物质发生反应)。化学兴趣小组为测定钙片中钙元素的含量,进行了如图实验:
根据图示信息,完成下列各题:
(1)钙片中钙元素的质量分数为 。
(2)求恰好完全反应时所得溶液的溶质质量分数?(要求写出计算过程)
某造纸厂排放含NaOH的废水200吨,恰好需要含溶质4.9吨的硫酸溶液中和处理,求该废水中NaOH的溶质质量分数。
某同学用溶质质量分数为15%的稀盐酸和大理石反应来制取二氧化碳气体:
(1)用20.3g溶质质量分数为37%的浓盐酸能配制上述稀盐酸 g(结果精确到1g)。
(2)若需收集10瓶(每瓶以125mL计算)二氧化碳气体,同至少需要多少克上述稀盐酸与足量的大理石反应才能制得(实验条件下二氧化碳的密度为2g/L)?(写出计算过程,结果精确到0.01g)
生铁和钢都是铁和碳的合金,生铁含碳量为2%~4.3%,钢含碳量为0.03%~2%.化学兴趣小组的同学为确定该铁合金是生铁还是钢,他们取11.5g铁合金样品盛放到锥形瓶中,将100g稀盐酸分成5等份,分5次加入锥形瓶,每次待充分反应后记录实验数据。实验数据整理如下表所示:
| 次数 |
加盐酸前 |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
| 加入稀盐酸的质量(g) |
0 |
20 |
20 |
20 |
20 |
20 |
| 锥形瓶内物质的总质量(g) |
11.5 |
31.4 |
m |
71.2 |
91.1 |
111.1 |
【查阅资料】碳不与稀盐酸反应。
请回答下列问题:
(1)根据质量守恒定律,该反应中生成气体的总质量为 。
(2)实验数据表中m的值为 。
(3)请通过计算确定该铁合金是生铁还是钢(写出计算过程,计算结果保留到0.1%)。
徐州地区石灰石资源丰富。某化学兴趣小组称取4.0g石灰石样品,把40g稀盐酸分4次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
稀盐酸的用量 |
剩余固体的质量 |
第一次加入10g |
3.0g |
第二次加入10g |
2.0g |
第三次加入10g |
l.0g |
笫四次加入10g |
0.6g |
请计算:
(1)4.0g石灰石样品中碳酸钙的质量是 g。
(2)10g稀盐酸能与 g碳酸钙正好完全反应。
(3)求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1% )。
取50g碳酸钠和氯化钠的混合溶液。向其中逐滴加入稀盐酸。加入稀盐酸的质量和生成气体的质量见下表(气体的溶解度忽略不计)。
第一组 |
第二组 |
第三组 |
|
稀盐酸的质量/g |
20 |
40 |
60 |
生成气体的质量/g |
2.0 |
m |
5.5 |
另取该混合溶液50g加入上述浓度的稀盐酸至恰好完全反应,此时溶液的pH=7,然后再加入足量的硝酸银溶液得到白色沉淀57.4g。试分析计算:
(1)50g混合溶液中碳酸钠的质量为 g。
(2)50g混合溶液中氯化钠的质量分数是多少?(写出计算过程,计算结果精确至0.1%)