小芳同学采用如下方法测定石灰石中碳酸钙的质量分数:取该石灰石样品10g,把40g稀盐酸分四次加入,实验过程所得数据如表(石灰石样品中含有的二氧化硅等杂质不溶于水也不与稀盐酸反应)
| 实验次数 |
加入稀盐酸的质量/g |
剩余固体的质量/g |
| 1 |
10 |
7.5 |
| 2 |
10 |
5.0 |
| 3 |
10 |
3.2 |
| 4 |
10 |
a |
根据实验数据计算:
(1)表中a的数值为 ;
(2)样品中碳酸钙的质量分数是 ;
(3)求盐酸中溶质的质量分数。
向100克MgCl 2和HCl的混合溶液中,逐滴加入10%的氢氧化钠溶液,反应情况,如图所示。
(1)当滴加氢氧化钠溶液的质量至N点时所得溶液的pH值为 (填编号);
A.大于7 B.等于7 C.小于7
(2)通过计算,确定M点的值,写出计算过程。
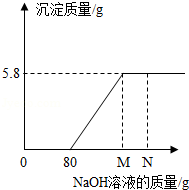
工业盐酸中通常溶有少量的FeCl 3而呈黄色,小红为测定某工业盐酸中HCl的含量进行如下实验:取某工业盐酸l00g,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示,FeCl 3与NaOH反应的化学方程式为FeCl 3+3NaOH═Fe(OH) 3↓+3NaCl.请回答下列问题:
(1)FeCl 3与NaOH恰好完全反应时,生成沉淀的质量是 g。
(2)该工业盐酸中HCl的质量分数是多少?(写出计算过程)
(3)取l00g该工业盐酸稀释成HCl质量分数为10%的稀盐酸,需加多少克水?(写出计算过程)

为了测定某石灰石样品中碳酸钙的含量,小敏同学取12.5g该样品进行实验,然后将100mL稀盐酸分五次加入该样品中,充分反应后测得每次生成气体的质量如下表所示(样品中的杂质不反应,生成的气体全部逸出)。
| |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
| 加入稀盐酸的体积/mL |
20 |
20 |
20 |
20 |
20 |
| 生成气体的质量/g |
1.1 |
1.1 |
1.1 |
1.1 |
0 |
请计算:
(1)生成气体的总质量是 g。
(2)碳酸钙(CaCO 3)的化学式量是 。
(3)该石灰石样品中碳酸钙的质量分数(写出计算过程)。
我市沿海地区大量养殖贝类海产品,贝壳中含有的碳酸钙是重要的工业原料。为了测定某种贝壳中碳酸钙的含量,取贝壳样品25.0g放入烧杯中,分五次加入稀盐酸,每次充分反应后称量(杂质不与稀盐酸反应),所加入稀盐酸的质量与烧杯中物质的质量的关系如下表:
| 加入稀盐酸的总质量(g) |
25.0 |
50.0 |
75.0 |
100.0 |
125.0 |
| 烧杯中物质的总质量(g) |
47.8 |
70.6 |
93.4 |
116.2 |
141.2 |
计算:
(1)当加入盐酸的总质量为50.0g时,充分反应后生成的气体质量是 g。
(2)该贝壳样品中碳酸钙的质量分数。
硫酸铜溶液对过氧化氢的分解有催化作用,取一定质量8.5%的过氧化氢溶液倒入烧杯中,加入一定质量15%的硫酸铜溶液,过氧化氢完全分解,有关实验数据如表所示(不考虑气体在水中的溶解).请计算:
|
反应前 |
反应后 |
||
实验数据 |
烧杯和过氧化氢溶液的质量/g |
硫酸铜溶液的质量/g |
烧杯和烧杯中溶液的质量/g |
|
60 |
3.3 |
62.5 |
||
(1)生成氧气的质量为 g.
(2)反应后烧杯中溶液溶质的质量分数.(写出计算过程,结果精确到0.1%).
实验室常用石灰石(主要成分的化学式:CaCO 3)与稀盐酸反应制取二氧化碳.某化学兴趣小组为了探究反应后废液中的成分,将废液过滤,取滤液40g于烧杯中,向其中滴加溶质质量分数为10.6%的碳酸钠溶液直到过量.有关变化如下图所示,根据题中有关信息和图象分析回答下列问题(石灰石中所含杂质不与稀盐酸反应,也不溶于水).
(1)CO 2由 种元素组成.
(2)每个CO 2分子中含有碳、氧原子的个数比为 .
(3)CO 2的相对分子质量是 .
(4)A点处生成沉淀的质量是 g.
(5)计算A点处溶液中溶质的质量分数(写出计算过程,结果精确到0.1%).

重质碳酸钙粉体产业为我市一大支柱产业,产品远销全国各地.某化学兴趣小组对粉体中碳酸钙含量进行了探究,小组成员从一包粉体产品中取出样品5.10g放入烧杯中,并逐滴加入相同浓度的稀盐酸(假设样品中的杂质不参与盐酸反应),实验测得烧杯中物质总质量与加入稀盐酸的总质量关系如表所示.
| 稀盐酸的总质量(g) |
10.00 |
20.00 |
30.00 |
40.00 |
50.00 |
60.00 |
70.00 |
| 烧杯中物质总质量(g) |
14.66 |
24.22 |
m |
43.34 |
52.90 |
62.90 |
72.90 |
(1)碳酸钙的相对分子质量为 .
(2)表中m= .
(3)求样品中碳酸钙的质量分数(结果保留两位小数).
根据如图所示的实验过程和所提供的数据计算(假设恰好完全反应)。

(反应的化学方程式为:K2CO3+CaCl2 ═CaCO3↓+2KCl)
(1)CaCl2中钙元素和氯元素的质量比为 。
(2)样品中碳酸钾的质量分数(写出计算过程)。
(3)反应后所得溶液中氯化钾的质量(写出计算过程)。
葡萄糖(C6H12O6)溶液与银氨溶液[主要成分是Ag(NH3)2OH]反应,可以在玻璃表面均匀地镀上一层银,工业上可用于制镜,该反应为:C6H12O6(葡萄糖)+2Ag(NH3)2OH C6H15O7N(葡萄糖酸铵)+2Ag↓+3NH3↑+H2O.请回答以下问题.
C6H15O7N(葡萄糖酸铵)+2Ag↓+3NH3↑+H2O.请回答以下问题.
(1)葡萄糖分子中碳、氢、氧三种原子个数比为 ,碳元素的质量分数为 .
(2)若制镜需要用银21.6g,列式计算需要葡萄糖的质量.
小黄同学为了测定某Cu﹣Ag合金中各金属的含量,取这种合金4.8 g与AgNO3溶液反应,加入AgNO3溶液的质量m与充分反应后所得固体的质量b的关系如图所示.请计算:
(1)AgNO3溶液中溶质的质量分数(结果精确 至0.1%);
(2)该合金中银和铜的质量比(结果精确至0.1).

某钢铁厂实验室为测定赤铁矿Fe 2O 3的含量,将矿石粉碎(其中杂质既不溶于水也不与酸反应),进行如下实验:

请回答下列问题:
(1)上述实验过程中发生反应的化学方程式为 ;
(2)样品中Fe 2O 3的质量分数是 ;
(3)根据已知条件列式求解200g稀硫酸中溶质质量(x)的比例式 ;
(4)若向最终滤液中加入16g水,所得不饱和溶液中溶质的质量分数为 ;
(5)该钢铁厂每天用上述赤铁矿石1900t来生产生铁,则理论上日产含杂质5%的生铁的质量为 .
某工厂从1000kg铝土矿(主要成分是Al 2O 3)冶炼得到270kg铝。反应的化学方程式是:2Al 2O 3(熔融)  4Al+3O 2↑。请计算。
4Al+3O 2↑。请计算。
(1)Al 2O 3中,Al、O原子个数比是 。
(2)列式计算该铝土矿中Al 2O 3的质量分数。
大理石是含杂质的碳酸钙,因具有美丽花纹而被广泛用于建筑物外墙、内壁的贴面和地面铺设。某同学想测出大理石样品中碳酸钙的含量,进行了如下实验和分析。

(1)取一定量的大理石样品置于图甲的发生装置中,用分液漏斗向下滴加盐酸(CaCO 3+2HCl=CaCl 2+H 2O+CO 2↑,杂质不参加反应),产生的气体用含有碱性物质的吸收装置充分吸收。分液漏斗中所加液体不选用硫酸,理由是 。
(2)反应前,测得图甲中锥形瓶内物质的总质量和吸收装置的总质量都为m克。实验后,根据实验数据绘制了图乙,曲线a、b分别表示锥形瓶内物质的总质量和吸收装置的总质量随反应时间变化的情况。请根据曲线b分析计算出大理石样品中碳酸钙的质量。
(3)请综合分析曲线a、b,计算出实验中所用盐酸的溶质质量分数。(结果精确到0.1%)
(4)计算后,该同学对上述实验进行了反思。他认为分液漏斗中选用的盐酸浓度偏大会对实验结果造成较大影响,其原因是 。
工业生产常用"苛化法"制取氢氧化钠。其原料为碳酸钠、石灰乳[由Ca(OH) 2和水组成的混合物],大致流程如图1。

科学兴趣小组模拟上述流程,在实验室中制备氢氧化钠。
(1)实验室进行"操作1"时,需要用到下列器材(图2)中的 (可多选)。
(2)制备氢氧化钠的化学方程式为,Na 2CO 3+Ca(OH) 2=2NaOH+CaCO 3↓.将53克溶质质量分数为20%的碳酸钠溶液与17克石灰乳混合,若二者恰好完全反应出计算所得氢氧化钠溶液的溶质质量分数。(写出计算过程,计算结果精确到0.1%)
