为测定某石灰石矿中碳酸钙的含量,现称取12.5g石灰石矿样品与足量的稀盐酸反应(杂质不溶于水,也不参与反应),得到二氧化碳气体4.4g(假设生成的气体全部逸出)。请计算:该石灰石样品含CaCO3的质量分数?
环保石头纸的主要成分为碳酸钙,加入适量聚乙烯和少量胶合剂。
【实验一】 探究影响石头纸与盐酸反应快慢的因素
(1)甲、乙两同学设计实验如下:
| |
甲 |
乙 |
| 实验过程 |
 |
 |
| 现象 |
试管①、②、③中产生气泡快慢的顺序为:①>②>③。 |
|
| 分析结论 |
Ⅰ 碳酸钙与稀盐酸反应的化学方程式为 ; Ⅱ 对比甲同学实验①②可知, ,化学反应的速度越快; Ⅲ 对比甲同学实验 (填实验序号)可知,反应物的接触面积越大,反应速率越 。 Ⅳ 乙同学的实验中,应该连续记录的实验数据是 和 。 |
【实验二】 测定石头纸中碳酸钙的质量分数 提示:石头纸中其他成分均不与盐酸反应,也不溶于水。
(2)甲组同学:图Ⅰ为石头纸与稀盐酸反应的装置,图Ⅱ用于测量通常状况下CO2的体积。

①实验前首先要 ;
② 图Ⅱ装置中油层的作用是 ;
③ 反应完成后,先 (填具体操作),然后才能准确读得量气管中的CO2的体积。
④根据V CO2和ρCO2计算出CO2的质量,计算碳酸钙质量。
(3)乙组同学:均匀称取四份样品分别和稀盐酸反应,用电子天平及有关装置,得出二氧化碳质量,实验数据记录如下表。
| |
第1份 |
第2份 |
第3份 |
第4份 |
| 取样品质量(g) |
6.25 |
6.25 |
6.25 |
6.25 |
| 取稀盐酸的体积(mL) |
10.0 |
20.0 |
30.0 |
40.0 |
| 产生气体的质量(g) |
0.88 |
1.76 |
2.20 |
m |
通过对数据的分析和比较,回答下列有关问题
①在第 份样品的实验中,样品中碳酸钙完全反应了; 。
② m的值为
③石头纸样品中碳酸钙的质量分数是多少?(请写出计算过程)
某化工厂利用海水资源进行联合生产,制备氢氧化钠和甲醇等物质。其化工流程如下:
已知:2H2+CO CH3OH
CH3OH
回答下列问题:
(1)电解食盐水的化学方程式为: ;在实验室进行电解水的实验中,为了增强导电性,往往向水中加入少量稀硫酸,而不能加入氯化钠,理由是 。
(2)若该工厂每天可生产80吨甲醇(CH3OH),需要提供 吨氢气。
(3)该工厂每生产80吨甲醇需要消耗多少吨26%的氯化钠溶液?(第3问写出计算过程)
某化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用2g石灰石样品,把20g稀盐酸(氯化氢的水溶液)分四次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶解于水)充分反应后经过过滤、干燥等操作,最后称量,得实验数据如下:
稀盐酸的用量 剩余固体的质量
第一次加入5g 1.5g
第二次加入5g 1.0g
第三次加入5g 0.5g
第四次加入5g 0.3g
(1)从以上数据可知,这四次实验中,第( )次石灰石样品中碳酸钙已完全反应。
(2)石灰石样品中碳酸钙的质量分数为 。
(3)求所用稀盐酸的溶质质量分数?(需要有解题步骤和过程)
根据如图所示的实验过程和提供的数据进行计算:

(1)原混合物中NaCl的质量。(要求写出计算过程)
(2)AgNO3溶液溶质质量分数为 (精确到0.1%)
化学兴趣小组为测定某石灰石样品中碳酸钙的质量分数,取26g石灰石样品放在烧杯中,然后 向其中逐渐加入稀盐酸,使之与样品充分反应,恰好完全反应(杂质不参加反应)时,加入稀盐酸的质量为90g,反应后烧杯中物质的总质量为105g。请计算:
(1)反应生成二氧化碳的质量
(2)样品中碳酸钙的质量分数(结果保留到0.1%)
鸡蛋壳的主要成分是碳酸钙,为了测定蛋壳中碳酸钙的质量分数,小刚和小勇同学进行了如下实验。实验过程和测定的相关实验数据如下所示:请回答相关问题:

(1)逸航同学根据“蛋壳残渣质量为4.3g”,求得蛋壳中碳酸钙的质量分数为 ;
(2)鑫烁同学根据“反应过程中减少的质量”,也求得了蛋壳中碳酸钙的质量分数,请你写出鑫烁的计算过程和结果。
(3)逸航和鑫烁根据不同的数据求得蛋壳中碳酸钙的质量分数有明显差别,请你分析其中可能的原因 。
新的一年,同学们的学习方式有了很大变化。下面是《气体制取与收集》学习的课堂片段:
【自主学习】仿照氧气制取的学习和气体制取的一般思路,阅读课本,老师提供了几组药品,让同学们交流并选出适宜实验室制取二氧化碳的一组。
【合作交流】围绕以上问题,各小组展开了激烈的交流,下面是老师从第二小组同学交流中听到的各位学生的发言:
1号:碳酸盐用块状石灰石(主要成分碳酸钙),为什么不用纯碱(碳酸钠)呢?
3号:碳酸钠是粉未状的,反应的速度太快,不易控制,
2号:同意3号同学的说法,那我们把碳酸钠压制成块状可以吗?
各位都在思考,问题未能解决。
【展示释疑】通过各个小组的展示,大家明白了实验室制取二氧化碳应该选择石灰石和稀盐酸。
实际实验中,所用的原料或产物一般都含有杂质,在计算用料和产量时,应考虑到杂质问题。
请你帮助二组学生解决2号学生提出的问题,实验室把碳酸钠压制成块状_______(选填“可以”或“不可以”)代替石灰石制取二氧化碳。
【能力提升】某小组想测定所用石灰石样品中碳酸钙的质量分数,取用了2g的石灰石样品,把20g稀盐酸(氯化氢的水溶液)分4次加入样品中,(样品中除碳酸钙外,其余成分既不与盐酸反应,也不溶解于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下:
| 稀盐酸的用量 |
剩余固体的质量 |
| 第一次加入5g |
1.5g |
| 第二次加入5g |
1.0g |
| 第三次加入5g |
0.5g |
| 第四次加入5g |
0.3g |
(1)从以上数据可知,这四次实验中,第______次石灰石样品中碳酸钙已完全反应。
(2)求石灰石中碳酸钙的质量分数?
(3)求检测过程中所产生二氧化碳的质量?
取25g某石灰石样品于一只烧杯中,并向烧杯中加入146g稀盐酸,恰好完全反应后测得烧杯内剩余物质的质量为162.2g,已知石灰石中的杂质不与稀盐酸发生反应
(1)反应中生成二氧化碳的质量为 ;
(2)计算所加稀盐酸中溶质质量分数.
某氯化钠溶液中含有氯化镁(MgCl2),学习小组为测定其中氯化镁的质量分数,在50.0g该溶液中加入50.0g氢氧化钠溶液恰好完全反应,经测定生成沉淀的质量为2.9g。请回答下列问题:
(1)反应后溶液的质量为 g;
(2)求原氯化钠溶液中氯化镁的质量分数(写出计算过程)。
某工厂化验室用20%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液20g,洗涤后的溶液呈中性。这一定量石油产品中含H2SO4的质量是多少?(写出计算过程)
某简易制氧装置的示意图如图,其原理是通过撞击火帽触发启动装置产生热量,使产氧药块分解而持续释放氧气。
(1)装置中过滤层的作用是 。
(2)若产氧药块由氯酸钾(KClO3)和二氧化锰等组成,为得到一个人呼吸2小时所需氧气的量(折算后质量为48g),计算产氧药块中至少含氯酸钾的质量(写出计算过程)。
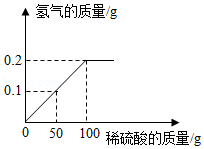
铜锌合金又称假黄金。向盛有30g铜锌合金粉末样品的烧杯中逐渐加入稀硫酸,生成氢气的质量与加入稀硫酸的质量关系如图所示,计算:
(1)充分反应后生成氢气的质量为 g。
(2)合金样品中锌的质量。
(3)恰好完全反应时,所得溶液溶质的质量分数。(结果保留一位小数)
科学兴趣小组同学在综合实践活动中了解到,某石灰厂有一批石灰石原料,其中含有的杂质二氧化硅(二氧化硅不溶于水,不能与盐酸反应,高温时不发生分解反应).为了测定该石灰石的纯度,兴趣小组同学取用2克这种石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸20克分4次加入,充分反应后,经过滤、干燥等操作后称量,每次盐酸用量及剩余固体的质量见表,利用实验数据绘制的图象见图.
| 稀盐酸的用量 |
剩余固体的质量 |
| 第一次加入5克 |
1.5克 |
| 第二次加入5克 |
克 |
| 第三次加入5克 |
0.5克 |
| 第四次加入5克 |
0.3克 |
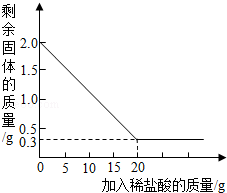
计算:
(1)分析上述图与表,第二次加入稀盐酸后,剩余固体的质量是 克;
(2)该石灰石样品中碳酸钙的质量分数;
(3)所用稀盐酸中溶质的质量分数是多少?