采用适当的试剂,从石灰石(主要成分为CaCO3)获得高纯度CaCO3的流程如下
①写出石灰石煅烧的化学方程式 (15) ;写出固体A 与试剂①反应的化学方程式 (16) ;
②上述流程中有的物质可以再利用,请在流程图上用箭头标示再利用的路线(箭头要求:从可利用的物质出发,指向利用该物质的环节); (17)
③为了测定某石灰石样品中碳酸钙的质量分数,取25g石灰石样品放入烧杯中,加入稀盐酸进行反应(杂质不参加反应)。随着反应进行,加入稀盐酸的质量与反应得到气体的质量变化关系如图所示:
计算:样品中碳酸钙的质量百分含量是多少?(18)(写出计算过程)

根据下图回答问题。
①仪器名称:a (10) 、b (11) 。
②实验室用大理石和稀盐酸制取二氧化碳,选用装置C优于B的原因是 (12) ;收集一瓶二氧化碳,将燃着的木条放在瓶口,若观察到 (13) ,说明已集满。
③取一朵用紫色石蕊试液染成紫色的干燥小花,将小花的一半用水喷湿,放入装置D中,观察到的实验现象是 (14) ,此现象说明CO2具有的化学性是 (15) (用化学方程式表示)。
④装置E中镁条能在CO2中剧烈燃烧,发出白光,放热,产生白色固体和黑色固体,反应的化学方程式
是 (16) 。
⑤欲测定鸡蛋壳中碳酸钙的质量分数。取12.5g干燥的碎鸡蛋壳放入烧杯中,向其中加入40g稀盐酸恰好完全反应(假设鸡蛋壳中除碳酸钙外其他成分均不与稀盐酸反应产生气体),反应后烧杯中物质的总质量为48.1g。计算:
Ⅰ.反应产生二氧化碳的质量为 (17) g;
Ⅱ.鸡蛋壳中碳酸钙的质量分数 (18) (通过化学方程式列式计算)。
小红同学在某化工厂进行社会实践,技术员与小红一起分析由氯化钡和氯化钠组成的产品中氯化钠的质量数。取16.25g固体样品,全部溶于143.6mL水中,向所得到的混合溶液中逐滴加入溶质质量分数为10.6%的碳酸钠溶液,记录了如图所示的曲线关系。技术员给小红的提示:反应的化学方程式BaCl2+Na2CO3===BaCO3↓+2NaCl
(1)当氯化钡与碳酸钠恰好完全反应时,消耗10.6%的碳酸钠溶液的质量是———g。
(2)产品中氯化钠的质量分数是多少?
(3)当氯化钡与碳酸钠恰好完全反应时,过滤,所得溶液中溶质的质量分数是多少?
某化工厂怀疑采购来的烧碱有部分变质,工厂技术员为了测定其变质情况,即测定烧碱的纯度(假设样品中只有氢氧化钠和碳酸钠这两种成分,且碳酸钠是变质产生的),做了如下实验:取烧碱样品20g,分四次加入到36.5g一定浓度的稀盐酸中,数据如下表所示
| 实验次数 |
1 |
2 |
3 |
4 |
| 每次加入样品的质量/g |
5 |
5 |
5 |
5 |
| 反应后剩余物质的总质量/g |
40.4 |
44.3 |
m |
54.3 |
请根据提供的数据,回答下列问题:
(1)表格中m的数值为 。
(2)请计算烧碱样品中烧碱的纯度。
为测定某大理石样品中碳酸钙的质量分数,取该样品10g,加入足量的10%盐酸,产生CO2 的物质的量与时间的关系如图所示(杂质不含碳元素)。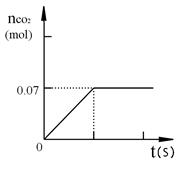

①该样品中碳酸钙的质量分数。(根据化学方程式列式计算)(19)
②若取该样品10g,充分煅烧,最多可以产生CO2 (20) g。
某兴趣小组要测定某石灰石样品中杂质的质量分数。他们进行了如图实验。
(杂质不发生反应)请计算:
(1)生成CO2气体的质量;
(2)样品中杂质的质量分数。
(4分)某补钙药剂的标签主要内容如图所示,现测定该钙片含量是否符合标注,做如下实验:取10片该钙片,放入干燥、洁净的烧杯中,再向烧杯中加入50g某浓度稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的质量为64.5g.
(1)反应中生成 g二氧化碳;
(2)通过计算说明实际钙含量是否与标注相符(写出计算过程).
小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中碳酸钙的质量分数进行检测,采用如下办法:取用8g这种石灰石样品,把40g稀盐酸分4次加入,测量过程所得数据见下表(已知石灰石样品中含的杂质不溶于水,不与盐酸反应)。
| 序号 |
加入稀盐酸质量(g) |
剩余固体质量(g) |
| 第1次 |
10 |
5.5 |
| 第2次 |
10 |
m |
| 第3次 |
10 |
1.2 |
| 第4次 |
10 |
n |
请计算:(1)表中m的数值为 ,n的数值应该为 ;
(2)样品中碳酸钙的质量分数是 ;
(3)通过计算,求反应中生成二氧化碳气体的质量。
某石灰水中含有氢氧化钙2.96g,要使该石灰水中的氢氧化钙全部转化为碳酸钙沉淀,至少需要二氧化碳的质量是多少?
钛(Ti)和钛合金被认为是21世纪的重要金属材料。钛可通过如下反应制得:
TiCl4 + 2Mg Ti + 2MgCl2,若要制得96 g钛,计算至少需要镁的质量。
Ti + 2MgCl2,若要制得96 g钛,计算至少需要镁的质量。
工业上常用电解饱和氯化钠水溶液的方法制备氢氧化钠,化学方程式为
2NaCl+2H2O 2NaOH+Cl2↑+H2↑。若制得16.0g氢氧化钠,可同时得到氯气的质量是多少?
2NaOH+Cl2↑+H2↑。若制得16.0g氢氧化钠,可同时得到氯气的质量是多少?
(6分)20g含杂质(杂质不溶于水,也不溶于酸)的锌样品,与一定质量的稀硫酸恰好完全反应,所得溶液质量为80.5g,同时生成氢气0.4g。试计算:
(1)样品中锌的质量分数;
(2)完全反应后生成溶液中溶质的质量分数;
(3)所用稀硫酸的质量分数 (计算结果保留到0.01%)。
为测定某地石灰石样品中碳酸钙的质量分数,进行了以下实验;向装有l0.0g石灰石样品的烧杯中,加入47.2g稀盐酸,恰好完全反应,烧杯中剩余物质的总质量随时间变化关系如下表:
(石灰石中的杂质不参加反应且难溶于水)
求:(1)最终生成二氧化碳的质量为 g:(2)样品中碳酸钙的质量分数。