工业上用甲、乙制备化学肥料丙,同时有丁生成。根据下列微观示意图得出的结论中,正确的是( ) 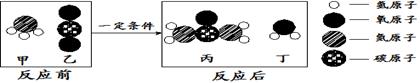
①甲的化学式为NH3 ②乙、丙、丁都是氧化物
③丙中氮、氢元素质量比为7:1 ④参加反应的甲、乙质量比为17:44
| A.① | B.①③ | C.①④ | D.②④ |
某化工企业生产流程示意图如图所示,下列说法中正确的是( )
| A.钛酸亚铁(FeTiO3)中钛元素为+3价 |
| B.① 中反应:2FeTiO3+6C+7Cl2一定条件2X+2TiCl4+6CO,则X为FeCl3 |
| C.② 中反应说明金属钛比金属镁的化学性质活泼,氩气起保护气的作用。 |
| D.③中反应要使原料全部转化为甲醇,理论上CO和H2投料的质量比是7:1 |
下列符合质量守恒定律是
| A.木炭燃烧后变成灰烬,质量减少 |
| B.一定条件下,SO2和O2生成SO3,反应前后分子总数不变 |
| C.100g水加入100g酒精,成为总质量为200g的溶液 |
| D.8g H2完全燃烧生成8g H2O |
根据乙炔气体完全燃烧时的反应:2C2H2+5O2 ="==" 4CO2+2H2O ,可以写出如下的符号式:
ν(C2H2) : ν(O2) : ν(CO2) : ν(H20)="=" 2 : 5 : 4 : 2。据此知识,下列说法错误的是
| A.参加反应的乙炔和氧气的化学计量数之比为2 : 5 |
| B.参加反应的乙炔和生成的二氧化碳的分子个数比为1 : 2 |
| C.参加反应的乙炔和氧气的质量比为2 : 5 |
| D.参加反应的乙炔和生成的二氧化碳的体积比为1 : 2 |
Zn + 2NH4Cl +2MnO2 ="==" ZnCl2 +2NH3 + X + H2O是手电筒中使用的锌-锰干电池在工作时反应的化学方程式,则X的化学式为
| A.MnO | B.Mn2O3 | C.Mn3O4 | D.HMnO4 |
为测定部分变质的氢氧化钠样品中变质的氢氧化钠的质量,某同学取该样品l3.3g于烧杯中,用滴管向其中慢慢滴加质量分数为7.3%的稀盐酸,当滴加稀盐酸lO0g,溶液中开始产生气泡,继续向其中滴加稀盐酸50g,恰好不再产生气泡,由此可知该样品中变质的氢氧化钠的质量是( )
| A.0.4g | B.0.8g | C.8g | D.4g |
煅烧碳酸钙可制得氧化钙。现有100 g含钙元素60%的碳酸钙和氧化钙的混合物.高温加热一段时间后,经实验测定已变成纯净物,则加热过程中产生二氧化碳的总质量为( )
| A.10 g | B.16 g | C.8 g | D.20 g |
某氢氧化钠样品长时间暴露在空气中,经测定其主要成分为 Na2CO3 和 NaOH。将 7.3g 该样品加入盛有 100g 质量分数为 7.3%稀盐酸的烧杯中,再向其中加入 20g 质量分数为 10%的氢氧化钠溶液使过量的盐酸恰好完全中和,最后将所得溶液蒸干,此时得到固体的质量是
| A.5.85g | B.2.925g | C.5g | D.11.7g |
逻辑推理是化学学习常用的思维方法,下列逻辑推理正确的是
| A.大多数物质燃烧需要氧气,所以氧气具有可燃性 |
| B.酸性溶液的pH都小于7,所以酸溶液的pH一定小于7 |
| C.氧化物都含有氧元素,所以含氧元素的物质都是氧化物 |
| D.反应前后物质质量守恒,所以10 g碳与10 g氧气反应生成20 g二氧化碳 |
向10g部分变质了的烧碱固体中,加入73g溶质质量分数为10%的稀盐酸,恰好完全反应,则反应后溶液中溶质的质量为
| A.11.7g | B.5.85g | C.10g | D.4g |
任何化学反应都要遵守质量守恒定律,下列说法符合质量守恒定律的是( )
| A.铁丝在氧气中燃烧生成固体的质量大于原来铁丝的质量 |
| B.2g氢气和8g氧气点燃,充分反应后,必然生成10g的水 |
| C.充分加热高锰酸钾后,残余固体的质量等于原来高锰酸钾的质量 |
| D.某物质在氧气中燃烧生成二氧化碳和水,说明该物质中一定含有碳、氢、氧三种元素 |
甲和乙反应可制备燃料丙,其微观示意图如下.下列说法错误的是( )
| A.该反应属于化合反应 | B.该反应中分子和原子的种类都发生了改变 |
| C.甲、丙是有机物,乙是氧化物 | D.甲、丙分别在氧气中完全燃烧,产物相同 |
由化学方程式CxHyOz + 5O2==4CO2+4H2O,可知x、y、z的值分别是 ( )
| A.1、2、3 | B.2、4、1 | C.4、8、2 | D.4、4、1 |