“●●”、“●○ ”“●○ ● ”分别表示A、B、C三种物质的分子,下图形象地表示了某化学反应前后反应物与生成物分子及其数目的变化。则关于该反应,下列有关说法错误的是
A. 该反应的化学方程式中A、B、C前的化学计量数之比为1:2:2
B.反应的本质是各原子进行了重新组合
C.该反应的生成物可能是氧化物
D. 该反应的可能是置换反应
氧化亚铜(Cu2O)是鲜红色粉末状固体,可用作杀菌剂、陶瓷和搪瓷的着色剂、红色玻璃染色剂等。现将 Cu2O 和 Cu 的固体混合物 6.8g 放入烧杯中,加入足量的稀硫酸,充分反应后,过滤、洗涤、干燥,得到 4.8g 固体。(已知Cu2O+H2SO4=CuSO4+Cu+H2O)。则原混合物中的 Cu2O 和 Cu 质量比为
| A.9∶8 | B.17∶12 | C.1∶1 | D.9∶4 |
“神舟”飞船内,用盛有LiOH的过滤网吸收航天员呼出的CO2气体,化学方程式为:CO2 + 2LiOH = Li2CO3 + H2O。计算吸收88gCO2,需要LiOH的质量。
工业上用侯氏制碱法制得的纯碱样品中含有一定量氯化钠,现称取只含氯化钠杂质的纯碱样品23.3g,放入盛有146g稀盐酸的烧杯中,恰好完全反应.反应后溶液的质量为160.5g,试计算:
(1)样品中碳酸钠的质量
(2)所用稀盐酸中溶质的质量分数
根据质量守恒定律,6g碳和32g氧气充分反应后,生成二氧化碳的质量为
| A.38g | B.22g | C.26g | D.14g |
用足量的CO还原4.0g某种铁的氧化物,生成的气体全部被足量的澄清石灰水吸收,得到沉淀7.5g,则这种铁的氧化物可能是
| A.FeO | B.Fe2O3 | C.Fe3O4 | D.FeO与Fe2O3的混合物 |
现有生石灰和碳酸钙的固体混合物9.5g,将其高温煅烧一段时间后,剩余固体8.4g,向剩余固体中加入150g溶质质量分数为7.3%的稀盐酸至恰好不再产生气泡为止,所得溶液恰好为中性,则原固体混合物中钙元素的质量分数约为( )
| A.50% | B.63.2% | C.84.5% | D.40% |
相同质量的下列物质①Zn②ZnO③Zn(OH)2④ZnCO3,分别跟质量分数都相同且适量的稀盐酸充分反应,所得溶液的溶质质量分数的关系正确的是 ( )
| A.①>②>③>④ | B.④>③>②>① |
| C.①>②=④>③ | D.④>①>②=③ |
一定条件下,在密闭容器中有甲、乙、丙、丁四种物质充分反应,测得反应前后各物质的质量分数如右图所示。下列说法正确的是
| A.在该反应中丁一定是催化剂 |
| B.该反应是化合反应 |
| C.反应前甲和乙的质量之和一定等于生成丙的质量 |
| D.由于未给出物质具体质量,以上说法均错误 |
煤的气化是将其转化为可燃性气体的过程,主要反应为:C+H2O CO+H2.若生产1t氢气,计算所需碳的质量.
CO+H2.若生产1t氢气,计算所需碳的质量.
现有6克碳和14克氧气完全反应,则生成物是()
| A. | B. | C. | 和 | D. | 无法确定 |
某不纯的铁5.6g与足量的稀硫酸充分反应,生成0.21g氢气,则铁中混有的金属可能是()
| A. | B. | C. | D. |
现将10 和足量 混合加热, 和 发生化学反应,10 完全反应后生成8 和4 ,则参加反应的 和 的质量比是( )
| A. | B. | C. | D. |
根据下图所示的实验过程和提供的数据,下列判断不正确的是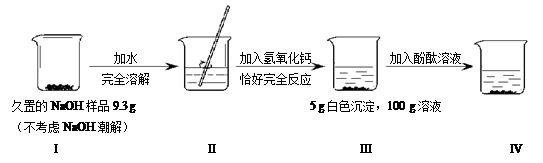
| A.I中未变质的NaOH质量为5.3 g | B.II中溶液有两种溶质 |
| C.III中溶液溶质的质量分数为8% | D.IV中溶液为红色 |