实验测成分
小伟同学在实验室中对某品牌除锈剂的有效成分及含量进行探究。
(1)定性检验:
小伟同学使用 、 分别与除锈剂反应,通过实验现象确定除锈剂的主要成分是硫酸。
(2)定量测定:
小伟同学利用碳酸钠溶液测定除锈剂中硫酸的质量分数,实验过程如下:
①向烧杯中加入50g除锈剂;
②向除锈剂中滴加碳酸钠溶液,边滴加边搅拌,至不再有气泡放出,共消耗碳酸钠溶液40g;
③反应后,烧杯中剩余物质的总质量为87.8g(除锈剂中其他成分不与碳酸钠反应,反应中产生的气体全部逸出)
根据上述实验数据计算除锈剂中硫酸的质量分数。
为了验证质量守恒定律。甲、乙、丙三位同学各做了一个实验。
(1)甲同学用实验测定的数据有:木炭和坩埚的总质量mg;其燃烧后灰烬和坩埚的总质量为ng。 m和n的关系为:m n(填“<”或“>”或“=”)。
(2)乙同学用实验测定的数据有:光亮的镁带的质量为x g;其在空气中完全燃烧之后生成的白色固体质量为了y g。 x和y的关系为:x y(填“<”或“>”或“=”)。
(3)丙同学实验测定的数据有:铁、硫酸铜溶液和烧杯的总质量为ag;其反应后的混合物和烧杯的总质量为bg。a与b的关系为:a b(填“<”或“>”或“=”)。
(4)通过对三个实验的分析,你认为用有气体参加或生成的化学反应来验证质量守恒定律时,应 ,才能判定参加化学反应的反应物总质量和生成物总质量是否相等。
实验室有一瓶失去标签的过氧化氢溶液,为测定其溶质质量分数,兴趣小组同学取l00g该溶液与1g二氧化锰混合,使其充分反应,产生气体的质量和反应时间关系如图。
(1)完全反应后,经过滤、烘干,得到固体的质量为 (不计操作过程中的损耗)
(2)产生气体的速度越来越慢的原因是 。
A.二氧化锰越来越少
B.过氧化氢溶液的溶质分数越来越小
C.温度越来越高
(3)计算所用过氧化氢溶液的溶质质量分数。(规范写出计算过程)

“诚信”是中华民族的优良传统,但目前有不法分子将炉甘石(ZnCO3)、赤铜(Cu2O)和木炭粉混合加热至约800℃得到一种外观酷似金子的铜锌合金,人称“伪黄金”,(其反应化学方程式为:ZnCO3+C+Cu2O高温Zn+2Cu+2CO2↑)然后加工成“黄金”饰品出售,非法牟取利益。作为当代中学生,请你利用所学知识揭露“伪黄金”的庐山真面目。
(1)列举一种鉴别真金与“伪黄金”的方法: ;
(2)按以上化学方程式计算,得到的铜锌合金中铜与锌的质量比 ;
(3)按以上化学方程式计算,若得到了26.4gCO2,消耗Cu2O的质量是多少? (要求写出计箅过程)
(4)请自拟一条标浯,倡导公民“诚信做人、合法经商”: 。
我国著名的化学家侯德榜发明了联合制碱法,大大提高了原料的利用率,其反应原理之一为NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl,某化工厂消耗117t氯化钠,理论上可生产碳酸氢钠的质量是多少?
(注:在20℃时,将二氧化碳通入含NH3的饱和NaCl溶液中能生成 NaHCO3晶体和NH4Cl溶液)
某化学兴趣小组欲测定某石灰石样品中碳酸钙的质量分数,先将10g样品放入烧杯中,再把100g稀盐酸分5次加入该样品中(该实验条件下,杂质不与酸反应,也不溶解于水,忽略稀盐酸挥发),得实验数据如表格。
稀盐酸的质量 |
充分反应后剩固体的质量 |
第一次加入20g |
8g |
第二次加入20g |
6g |
第三次加入20g |
4g |
第四次加入20g |
2g |
第五次加入20g |
2g |
请计算;
(1)10g石灰石样品中碳酸钙的质量分数是 。
(2)求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)。
孔雀石的主要成分是Cu2(OH)2CO3,还含有Fe2O3、Al2O3、SiO2杂质,用该矿石制备Cu的流程如图所示(部分产物略去):
 (1)过程①中,操作a是溶解和 ,还有一种气体产物是 ,滤液X中含有的金属阳离子为 。
(1)过程①中,操作a是溶解和 ,还有一种气体产物是 ,滤液X中含有的金属阳离子为 。
(2)过程①中硫酸略过量,则过程②调pH除杂的最佳试剂是 (选填“CuO”或“Na2CO3”)。
(3)下列关于制取铜的两种方案的说法,正确的是 。
A.“方案一”得到的铜产品更纯
B.“方案一”不存在消耗能量的问题
C.“方案二”需考虑废气污染的问题
D.“方案二”得到纯铜的产率更高
(4)过程③发生的反应:2CuSO4+2H2O 2Cu+O2↑+ (补充完方程式),当收集到800t氧气时,产生Cu的质量是多少?(写出必要的计算过程)
2Cu+O2↑+ (补充完方程式),当收集到800t氧气时,产生Cu的质量是多少?(写出必要的计算过程)
烧杯中盛有锌粉和铁粉的混合物mg,向其中逐渐加入一定浓度的稀盐酸,测得剩余固体的质量与加入稀盐酸的体积的关系如图所示。下列有关结论正确的是( )
①加入V1mL稀盐酸时,剩余固体中不含锌
②加入V2mL稀盐酸时,溶液中的溶质为FeCl3和ZnCl2
③整个过程中发生反应均为置换反应
④反应中产生氢气的质量一定小于 g
g
⑤剩余固体质量m、n与稀盐酸的体积V1、V2的数量关系为 =
=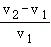

A.①②③④B.①③④C.①③⑤D.①③④⑤
钙是生物体骨骼的重要组成元素。鱼骨中含有碳酸钙,现设计图甲实验测定鱼骨中的碳酸钙含量,并将测得的数据绘制成图乙。

提示①食醋的主要成分是醋酸(HAc)。醋酸和碳酸钙反应的化学方程式为CaCO3+2HAc═CaAc2+H2O+CO2
②鱼骨中其它成分与食醋反应生成的气体可忽略不计
(1)该实验中浓硫酸的作用是 。
(2)由图乙中的AB曲线,可知锥形瓶中反应速率的变化情况是 (选填“变大”、“变小”或“不变)。
(3)根据图中的数据计算鱼骨中碳酸钙的质量分数。
(4)生活中,用喝醋的方法除去卡在咽上的鱼刺,这种做法是不科学的。请你结合实验结果加以说明 。
用沉淀法可测定食用碱样品中碳酸钠的质量分数。取11g食用碱样品(有少量的杂质氯化钠),加水完全溶解制成100g溶液,逐次滴加溶质质量分数相同的氯化钙溶液,实验数据如表:
实验次数 |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
第6次 |
加入CaCl2溶液的质量/g |
20.0 |
20.0 |
20.0 |
20.0 |
20.0 |
20.0 |
反应后溶液的总质量/g |
118.0 |
136.0 |
154.0 |
M |
191.0 |
211.0 |
请根据实验数据分析解答下列问题:
(1)表中数据M的值为 。
(2)请画出生成沉淀的质量随滴加氯化钙溶液质量的变化关系图(标明恰好反应时点的坐标)。
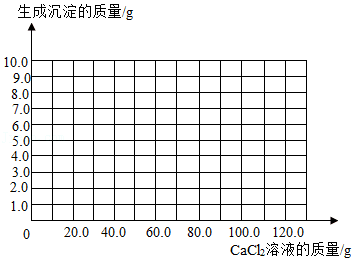
(3)计算该食用碱样品中碳酸钠的质量分数(写出过程,结果保留到0.1%)。
将50.0g盐酸、氯化镁和氯化铝的混合溶液置于烧杯中,逐滴加入质量分数为20.0%的氢氧化钠溶液,生成氢氧化铝沉淀的最大质量为7.8g。加入氢氧化钠溶液质量和生成沉淀质量的关系如图所示。请根据题意回答问题:
已知:Al(OH) 3+NaOH═NaAlO 2+2H 2O
(1)B点溶液中所含溶质是 (填化学式)。
(2)求图中A点的坐标: 。
(3)原混合溶液中MgCl 2的质量分数是多少?(写出计算过程,计算结果精确到0.1%)

工业上制作电路的一种反应原理是Cu+2HCl+H2O2 CuCl2+2H2O.若反应了6.4g Cu,计算需要10%的H2O2溶液的质量。
海水中蕴藏着丰富的资源,海水“晒盐”过程中可得到粗盐和卤水.粗盐中常含有多种杂质,必须对其分离和提纯,才能用于生产和生活;卤水经常用作工业制镁的原料.
(1)实验室除去粗盐中不溶性杂质的实验步骤为:溶解、过滤、蒸发结晶.在三步中都要用到的一种玻璃仪器是 .
(2)若要除去食盐固体中含有的少量CaCl2杂质,得到较为纯净的食盐晶体.请简述实验操作步骤: .
(3)在一烧杯中盛有Mg(OH)2和MgCl2的混合粉末6g,向其中加入20g水,经充分溶解后,再逐滴加入溶质质量分数为10%的稀盐酸.烧杯中溶液的溶液的总质量与加入稀盐酸的质量关系如图所示,请回答下列问题:
①当滴入稀盐酸30g时(即图中A点时),烧杯内溶液中的溶质是 (填写化学式).
②当滴入稀盐酸73g时(即图中B点时),试通过计算,求此温度时所得不饱和溶液中溶质的质量(计算结果精确至0.1g).

某Na 2CO 3样品中混有一定量的Na 2SO 4,小明想测定样品中Na 2CO 3的质量分数,取该样品20克放入烧杯,加入100克水使样品全部溶解,再向烧杯中滴加稀硫酸,当滴加的稀硫酸质量为50克时,恰好完全反应,称得烧杯中溶液的质量是165.6克.
请通过计算回答:
(1)滴加的稀硫酸中溶质的质量分数.
(2)该样品中Na 2CO 3的质量分数.
部分被氧化的铁片10g与200g的稀硫酸恰好完全反应,产生氢气0.3g,求该硫酸溶液的溶质质量分数?